 十一化学动力学Word下载.docx
十一化学动力学Word下载.docx
- 文档编号:14726998
- 上传时间:2022-10-24
- 格式:DOCX
- 页数:10
- 大小:119.48KB
十一化学动力学Word下载.docx
《十一化学动力学Word下载.docx》由会员分享,可在线阅读,更多相关《十一化学动力学Word下载.docx(10页珍藏版)》请在冰豆网上搜索。
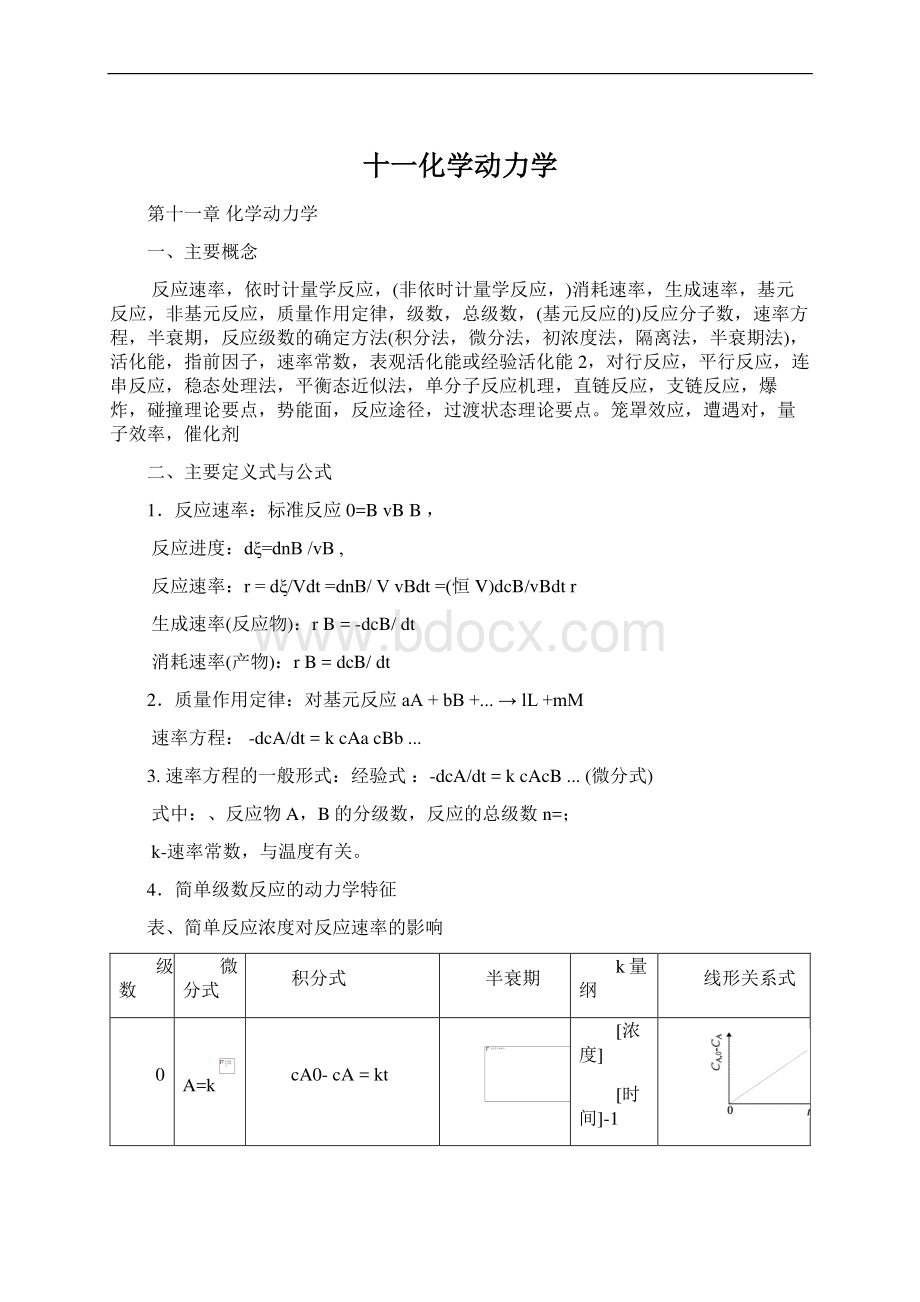
k-速率常数,与温度有关。
4简单级数反应的动力学特征表、简单反应浓度对反应速率的影响级数微分式积分式半衰期k量纲线形关系式0A=kcA0-cA=kt浓度时间-11A=kcAln(cA0/cA)=kt或ln1/(1-xA)=kt时间-12A=kcA2或浓度-1时间-1nA=kcAn注意:
n1浓度1-n时间-1注意:
用浓度表示的反应速率如dcA/dt=kccAn,则k指kc。
若用分压表示的反应速率dpA/dt=kppAn,则k指kp。
两者关系为kp=kc(RT)1-n5确定反应级数的方法
(1)积分法:
-dcA/cAcB.=kdt(积分式)把实验数据cAt关系代入各级数的反应积分式中求出k,若k为常数则为此级数,或作其线性关系图,若呈直线则为该级数。
此法适用于整数级反应。
(2)微分法:
对=kcAn形式的动力学方程,取对数ln(/)=ln(k/k)+nln(cA/c),作ln(/)ln(cA/c)图可求出斜率=n。
式中需从实验得的cAt图中求出dcA/dt。
此法适用于整数、分数级数。
用初浓度法还可避免产物的干扰。
(3)半衰期法:
或,作图可求n。
(4)隔离法:
对于有两种或两种以上反应物的反应,如=kcAacB当恒定cB(或cBcA,B浓度变化很小),=kcAa,可通过上述方法求出a。
同理恒定A浓度时,=k”cB,可通过上述方法求出。
6温度对反应速率的影响:
速率常数k与温度T的关系
(1)范特霍夫(VantHoff)规则:
或,=24称为温度系数。
(2)阿累尼乌斯(Arrhenius)方程:
(微分式,活化能Ea的定义式)i不定积分式:
或指数式:
以ln(k/k)或ln(k/k)对1/T作图为一直线,由直线斜率和截距可分别计算活化能Ea和指前因子k0。
ii定积分式:
iiiEa大则k小,反应难。
Ea大,(Ea/RT2)大,即k随T变化大,若有两个反应,活化能大的反应,升温时速率常数k增大。
7各类典型复合反应的主要公式及基本要求
(1)一级对行反应i.微分式:
dcA/dt=k1cA+k-1cBii.积分式:
iii.完成距平衡浓度一半的时间,与初浓度无关。
iv.平衡常数与正、逆速率常数关系Kc=k1/k-1v.反应焓与正、逆反应活化能关系rHrU=E正-E逆
(2)一级平行反应i.微分式-dcA/dt=(k1+k2)cAii.积分式:
ln(cA,0/cA)=(k1+k2)tiii.半衰期:
。
iv.产物分布:
cB/cC=k1/k2v.表观活化能与基元反应活化能关系(3)连串反应:
ABCi.微分式-dcA/dt=k1cA,dcB/dt=k1cA-k2cB,dcC/dt=k2cBii.积分式:
中间产物极大时的时间与浓度。
8.处理复杂反应动力学方程的方法:
(1)选取控制步骤法:
多个反应步骤中存在控制步骤。
(2)稳态近似法:
中间物B很难生成,但反应性很强,使其浓度很低,dcB/dt=0。
(3)平衡近似法:
反应能随时保持平衡。
9光化学定律
(1)光化学第一定律:
只有被系统吸收的光,才能有效地引起光化反应。
(2)光化学第二定律:
在初级过程中,系统每吸收一个光子活化一个分子或原子。
(3)1摩尔光子能量Em(即1爱因斯坦):
Em=Lhv=Lhc/式中:
光速c,普朗克常数h,L-阿佛加德罗常数,-波长(4)量子效率:
10催化作用
(1)催化剂:
存在较少量就能显著加速反应而本身最后并无损耗的物质。
减慢反应的物质称阻化剂。
(2)催化剂的基本特征i.催化剂参与催化反应,开辟一条更快的新途径,降低活化能,但反应前后催化剂的化学性质和数量不变。
ii.催化剂不能改变反应系统的始、末状态。
故不能改变反应的状态函数变如G、H。
iii.催化剂不能改变反应的平衡状态,只能加速平衡的到达。
即不能改变或平衡常数。
因K=k1/k-1,故催化剂同时催化正向和逆向反应。
iv.催化剂对反应的加速作用具有选择性。
三、主要题型:
确定反应级数、,计算活化能Ea及kT关系是本章的核心。
1解题时注意的问题:
(1)比较熟练0,1,2级反应的动力学特征(cA-t,k的单位,t1/2,线型图)。
为了避免记错,做题时最好用动力学方程的积分式或微分式进行推导助记。
(2)题目常常给出反应动力学特征:
cA-t关系,k的单位,t1/2,线型图等,应该马上想到对应的级数。
(3)若恒T、V,则pB=cBRT,动力学方程可用pB代替cB,即-dpA/dt=kppApB.其中kp=k(RT)1。
2给出cA-t关系,求级数、,活化能Ea及kT关系相关的计算。
3简单的一级复合反应(对行反应,平行反应,连串反应)相关的计算。
4给出复杂反应的机理推导动力学方程。
5综合例题例题1:
乙醛热分解CH3CHOCH4CO是不可逆反应,在518及恒容条件下,有数据:
初始压力(纯乙醛)0.400kPa0.200kPa100秒后系统总压0.500kPa0.229kPa求
(1)乙醛分解的反应级数;
(2)计算518时的速率常数;
(3)实验测得在538时的速率常数是518时的两倍,计算该反应的活化能。
(共12分)解:
本题与天津大学物理化学第四版教材11.33题基本相同。
设甲醛为A,因为是恒温恒容反应,可用压力代替浓度进行有关计算。
ACH4COt=0pA000总压p=pA0t=tpApA0pApA0pA总压p=2pA0pA所以pA=2pA0p
(1)可用多种方法求解。
比较简单的是积分法。
假设为级数n1,则k=ln(pA0/pA)/t=lnpA0/(2pA0p)/t代入数据:
k1=ln0.400/(20.4000.500)/100s=0.00288s1k2=ln0.200/(20.2000.229)/100s=0.00157s1速率常数相差太多,可否定为一级反应。
假设为二级反应,则k=(pA1pA01)t代入数据得:
k1=(20.400-0.500)-10.400-1kPa-1/100s0.00833kPa-1s1k2=(20.200-0.229)-10.200-1kPa-1/100s0.00848kPa-1s1速率常数非常接近,所以可认为是二级反应。
用n级反应的压力与时间式代入建立一个方程,用尝试法求n亦可。
(2)速率常数k=(k1+k2)/2=0.00841kPa-1s1。
(3)Ea=RT1T2ln(k/k)/(T2T1)(8.315793.15813.15ln2/20)Jmol1186kJmol1例题2:
有下列反应式中k1和k2分别是正向和逆向基元反应的速率常数,它们在不同温度时的数值如下:
温度/K300310k1/s-13.5010-37.0010-3k2/(sp)-17.0010-71.4010-6
(1)计算上述可逆反应在300K时的平衡常数Kp和K。
(2)分别计算正向反应与逆向反应的活化能E1和E2。
(3)计算可逆反应的反应焓H。
(4)在300K时,若反应容器中开始时只有A,其初始压力p0为p,问系统总压p,达到1.5p时所需时间为多少?
(可适当近似)(13分)。
解:
(1)Kp=k1/k2=3.50103s1/7.00107(sp)-15000pKKp/p=5000
(2)E1=RTTln(k1/k1)/(TT)=8.315300310ln(7.00/3.50)/(310300)Jmol153.6kJmol1E2=RTTln(k2/k2)/(TT)=8.315300310ln(1.40106/7.00107)/(310300)Jmol153.6kJmol1(3)H=E1E20(4)A(g)=B(g)+C(g)t=0pp=pt=tpAp-pAp-pAp=2p-pA即pA2pp速率方程-dpA/dt=k1pAk2(p-pA)2k1pA(pk2k1)积分得t=ln(pA0/pA)/k1=lnp/(2pp)/t=lnp/(2p1.5p)/3.5010-3s-1=198s例题3:
已知反应NO2(g)=NO(g)+(1/2)O2(g)以NO2的消耗速率表示的反应速率常数与温度的关系为ln(k/dm3mol1s1)12884K/T+20.2664
(1)试求反应的级数,活化能Ea及指前因子A。
(2)若在400时将压力为26664Pa的NO2(g)通入反应器中,使之发生分解反应,试计算反应器的压力达到31997Pa时所需时间。
(10分)解:
(1)速率常数k的单位为dm3mol1s1,所以反应为2级。
与阿累尼乌斯方程的对数式ln(k/dm3mol1s1)=Ea/RT+ln(A/dm3mol1s1)对比,可得Ea12884KR12884K8.315JK1mol1107.1kJmol1A=exp(20.2664)dm3mol1s1=6.33108dm3mol1s1注:
代入两种温度分别计算k,再算Ea亦可。
(2)400时的速率常数:
ln(k/dm3mol1s1)12884K/673.15K+20.2664=1.1265k=3.085dm3mol1s1设NO2(g)=A,对于二级反应,反应时间与浓度的关系如下t=(1/cA-1/cA0)/k需知道浓度,可通过压力进行计算:
NO2(g)=NO(g)+(1/2)O2(g)t=0p0=26664Pa00t=t26664Papxpx(1/2)px总压p=26664Pa+px/2=31997Pa所以px10666PacA=(26664-10666)Pa/RT=15998Pa/RT,cA0=26664Pa/RTt=(1/cA-1/cA0)/kRT(1/15998Pa1/26664Pa)/k=8.315JK1mol1673.15K(1/15998Pa1/26664Pa)/(3.085103m3mol1s1)45.37s例题4(:
有一平行反应在500K时,k1、k2分别为4.65s-1和3.74s-1。
求
(1)A转化90所需要的时间;
(2)求总反应的表观活化能。
已知两平行反应的活化能E1、E2分别为20kJmol-1和26kJmol-1。
本题需掌握一级平行反应的规律才容易做。
若没掌握,需自己推导。
(1)A的转化率x与时间的关系如下:
t=ln(1x)/(k1+k2)ln
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 十一 化学 动力学
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 12处方点评管理规范实施细则_精品文档.doc
12处方点评管理规范实施细则_精品文档.doc
 17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
