 高三复习原电池电解池Word格式.docx
高三复习原电池电解池Word格式.docx
- 文档编号:14710960
- 上传时间:2022-10-24
- 格式:DOCX
- 页数:17
- 大小:223.90KB
高三复习原电池电解池Word格式.docx
《高三复习原电池电解池Word格式.docx》由会员分享,可在线阅读,更多相关《高三复习原电池电解池Word格式.docx(17页珍藏版)》请在冰豆网上搜索。
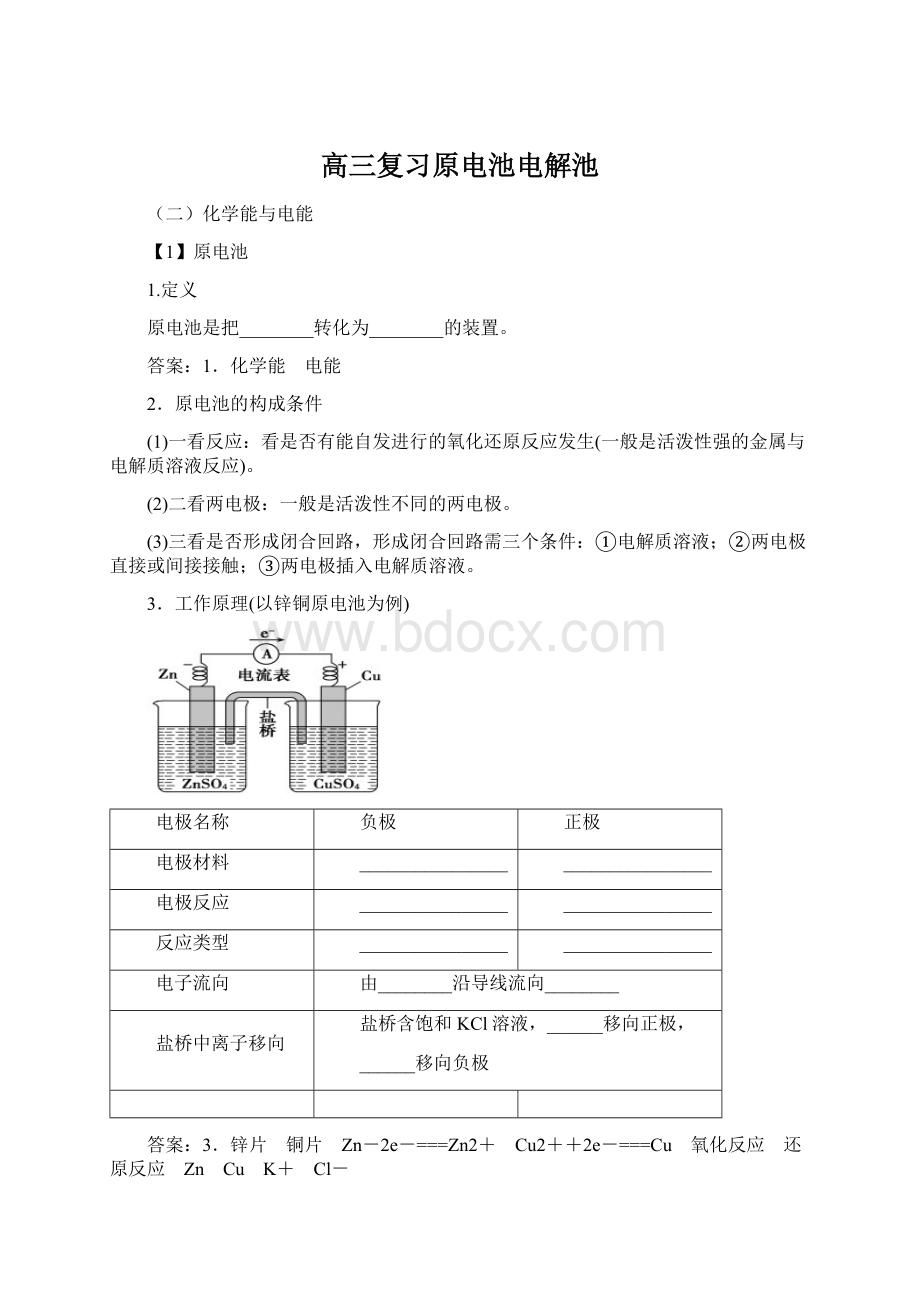
电极反应
反应类型
电子流向
由________沿导线流向________
盐桥中离子移向
盐桥含饱和KCl溶液,______移向正极,
______移向负极
3.锌片 铜片 Zn-2e-===Zn2+ Cu2++2e-===Cu 氧化反应 还原反应 Zn Cu K+ Cl-
3.种常见的化学电源
电池
负极反应
正极反应
总反应式
一次电池(锌锰干电池)
酸性锌锰
干电池
___________
2NH+2e-===2NH3↑+H2↑
碱性锌锰干电池
Zn+2OH--
2e-===Zn(OH)2
2MnO2+2H2O+2e-===2MnO(OH)+2OH-
__________________________________
二次电池(铅蓄电池)
______________________
______________________________________
Pb(s)+PbO2(s)+2H2SO4(aq)===2PbSO4(s)+2H2O(l)
燃料电池(氢氧燃料电池)
酸性氢氧燃料电池
2H2+O2===2H2O
碱性氢氧
燃料电池
Zn-2e-===Zn2+ Zn+2MnO2+2H2O===2MnO(OH)+Zn(OH)2 Pb+SO-2e-===PbSO4 PbO2+4H++SO+2e-===PbSO4+2H2O 2H2-4e-===4H+
O2+4e-+4H+===2H2O 2H2-4e-+4OH-===4H2O
O2+4e-+2H2O===4OH-
4.金属的腐蚀与防护
(1)腐蚀与电化学腐蚀
化学腐蚀
电化学腐蚀
定义
金属跟接触到的物质(如O2、Cl2、SO2等)________发生________反应而引起的腐蚀
不纯金属与电解质溶液接触时,发生______反应,________的金属失电子而被氧化
本质
______电流产生
________电流产生
现象
金属被________(氧化)
________金属被腐蚀(氧化)
实例
金属与Cl2、O2等物质直接发生化学反应
钢铁在潮湿的空气中生锈
实质与联系
实质都是金属原子________电子被________而损耗;
化学腐蚀与电化学腐蚀往往同时发生,但电化学腐蚀更普遍、危害性更大、腐蚀速率更快
1.直接 化学 原电池 比较活泼 无 有微弱 腐蚀 较活泼 失去 氧化
(2)铁的析氢腐蚀和吸氧腐蚀
析氢腐蚀
吸氧腐蚀
条件
水膜酸性较______
水膜酸性______
或______
__________________
2.强 很弱 呈中性 2H++2e-===H2↑ O2+2H2O+4e-===4OH- Fe-2e-===Fe2+ 2Fe-4e-===2Fe2+
(3)金属的防护
(1)改变金属的组成结构。
如铁中加入一定比例的铬炼制得铬钢,具有很高的耐腐蚀性。
(2)在金属表面覆盖一层________层,使金属与周围具有腐蚀性的气体和电解质溶液隔离,便可保护金属,防止金属腐蚀。
如在金属表面上喷漆、电镀或覆盖搪瓷,使表面钝化等。
(3)电化学保护法:
①牺牲阳极保护法:
使被保护的金属设备作原电池的____极。
②外加电流阴极保护法:
使被保护的金属设备作电解池____极,与外接电池的负极相连接,用废铁作____极。
3.
(2)保护 (3)①正 ②阴 阳
例1:
判断正误正确的打“√”,错误的打“×
”。
1.锂水电池以金属锂和钢板为电极材料,以KOH为电解质,使用时加入水即可放电;
放电时OH-向正极移动
( )
2.镀锌层破损后对铁制品失去保护作用( )
3.铅蓄电池放电时的负极和充电时的阳极均发生还原反应( )
4.铜的金属活泼性比铁的差,可在海轮外壳上装若干铜块以减缓其腐蚀( )
5.碘也可用作心脏起搏器电源——锂碘电池的材料。
该电池反应为:
2Li(s)+I2(s)===2LiI(s),碘电极作为该电池的正极( )
6.浸入海水中的铁棒,越靠近底端腐蚀越严重( )
7.原电池中盐桥的作用是传导电子( )
8.原电池中负极金属的活泼性一定比正极金属的活泼性强( )
9.可逆电池充电时,可逆电池的负极与外接电池的正极相连,其正极与外接电源的负极相连( )
10.钢铁在吸氧腐蚀过程中,Fe最终变成了Fe(OH)2( )
1.×
2.×
3.×
4.×
5.√ 6.×
7.×
8.×
9.×
10.×
1.(2013·
江苏卷)Mg-H2O2电池可用于驱动无人驾驶的潜航器。
该电池以海水为电解质溶液,示意图如下。
该电池工作时,下列说法正确的是( )
A.Mg电极是该电池的正极
B.H2O2在石墨电极上发生氧化反应
C.石墨电极附近溶液的pH增大
D.溶液中Cl-向正极移动
解析:
Mg电极是该电池的负极,A错误;
H2O2在石墨电极上得电子,发生还原反应,B错误;
石墨电极上发生的电极反应式为:
H2O2+2e-===2OH-,从电极反应式可以判断出,石墨电极附近溶液的pH增大,C正确;
溶液中的阴离子移向负极,D错误。
C
2.下列反应没有涉及原电池的是( )
A.生铁投入稀盐酸中
B.铜片与银片用导线连接后,同时插入FeCl3溶液中
C.纯锌投入硫酸铜溶液中
D.含铜的铝片投入浓硫酸中
A项生铁中含碳,投入稀盐酸中时构成原电池。
B项构成原电池。
C项置换出铜后,构成锌铜原电池。
D项浓硫酸不导电,不能构成原电池。
D
3.一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为:
CH3CH2OH-4e-+H2O===CH3COOH+4H+。
下列有关说法正确的是( )
A.检测时,电解质溶液中的H+向负极移动
B.若有0.4mol电子转移,则在标准状况下消耗4.48L氧气
C.电池反应的化学方程式为:
CH3CH2OH+O2===CH3COOH+H2O
D.正极上发生的反应为:
本题考查新型燃料电池,意在考查学生能否正确书写电极反应式。
结合题意,该电池总反应即是乙醇的氧化反应,不消耗H+,故负极产生的H+应向正极移动,A项错误;
酸性溶液中,正极电极反应式为:
O2+4e-+4H+===2H2O,D项错误,结合D项,转移0.4mol电子时,消耗0.1molO2,即标况下的体积为2.24L,B项错误;
C项符合题目要求,正确。
4.(双选)如图所示的原电池,下列说法正确的是( )
A.电子从锌电极通过电流表流向铜电极
B.盐桥中的阴离子向硫酸锌溶液中迁移
C.锌电极发生还原反应,铜电极发生氧化反应
D.铜电极上发生的电极反应是:
2H++2e-===H2↑
由原电池装置图可知,负极为Zn,发生氧化反应:
Zn-2e-===Zn2+;
正极为Cu,发生还原反应:
Cu2++2e-===Cu。
盐桥中的阴离子向ZnSO4溶液中迁移;
阳离子向CuSO4溶液中迁移。
故选A、B两项。
AB
5.(2013·
广东卷)能量之间可以相互转化:
电解食盐水制备Cl2是将电能转化为化学能,而原电池可将化学能转化为电能。
(1)设计两种类型的原电池,探究其能量转化效率。
限选材料:
ZnSO4(aq),FeSO4(aq),CuSO4(aq);
铜片,铁片,锌片和导线。
①完成原电池的甲装置示意图(见下图),并作相应标注。
要求:
在同一烧杯中,电极与溶液含相同的金属元素。
②以铜片为电极之一,CuSO4(aq)为电解质溶液,只在一个烧杯中组装原电池乙,工作一段时间后,可观察到负极________。
③甲乙两种原电池中可更有效地将化学能转化为电能的是________,其原因是_____________________________。
(2)根据牺牲阳极的阴极保护法原理,为减缓电解质溶液中铁片的腐蚀,在
(1)的材料中应选________作阳极。
(1)由题给试剂,结合原电池的形成条件可知可以组合的原电池可以是:
锌铜、锌铁、铁铜原电池。
由图示所给电子移动方向可知左边为负极(活泼金属)、右边为正极(不活泼金属),则组装的原电池可以如下:
由所给的电极材料可知,当铜片做电极时,铜片一定是正极,则负极是活泼的金属(失电子发生氧化反应),反应的现象是电极逐渐溶解。
以Zn和Cu做电极为例,如果不用盐桥则Zn与CuSO4反应,置换出的Cu附着在Zn表面,阻碍了Zn与CuSO4的接触,不能提供稳定电流。
(2)根据牺牲阳极的阴极保护法,可知被保护的金属作阴极,即锌片作为阳极。
(1)①(装置图如下) ②电极逐渐溶解 ③甲 可以避免活泼金属如Zn和CuSO4的接触,从而提供稳定电流
(2)锌片
【2】电解池
1.概念
把______能转化为________能的装置。
1.电 化学
2.电解原理
(1)电解:
使______通过电解质溶液(或熔融的电解质)而在______引起______的过程。
(2)电极名称与电极反应。
与电源正极相连的为______,发生________反应;
与电源负极相连的为______,发生________反应。
(3)电极材料
惰性电极:
如_____________。
活性电极:
(4)工作原理:
(以石墨为电极电解CuCl2溶液为例)
电极反应式
阳极:
________________________
阴极:
总式:
________________________________
电源________→导线→电解池________
电解池________→导线→电源________
离子移动方向
电解质溶液中的阳离子移向________
电解质溶液中的阴离子移向________
2.
(1)电流 阴、阳两极 氧化还原反应
(2)阳极 氧化 阴极 还原 (3)石墨、铂 Cu、Zn、Fe (4)2Cl--2e-===Cl2↑ Cu2++2e-===Cu CuCl2Cu+Cl2↑ 负极 阴极 阳极 正极 阴极 阳极
3.电解池的应用
1.
电解食盐水制备烧碱、氢气和氯气。
阴极反应式:
__
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 复习 原电池 电解池
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 12处方点评管理规范实施细则_精品文档.doc
12处方点评管理规范实施细则_精品文档.doc
 17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
