 甘肃省高三第一次高考诊断考试Word格式文档下载.docx
甘肃省高三第一次高考诊断考试Word格式文档下载.docx
- 文档编号:14673215
- 上传时间:2022-10-23
- 格式:DOCX
- 页数:12
- 大小:878.86KB
甘肃省高三第一次高考诊断考试Word格式文档下载.docx
《甘肃省高三第一次高考诊断考试Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《甘肃省高三第一次高考诊断考试Word格式文档下载.docx(12页珍藏版)》请在冰豆网上搜索。
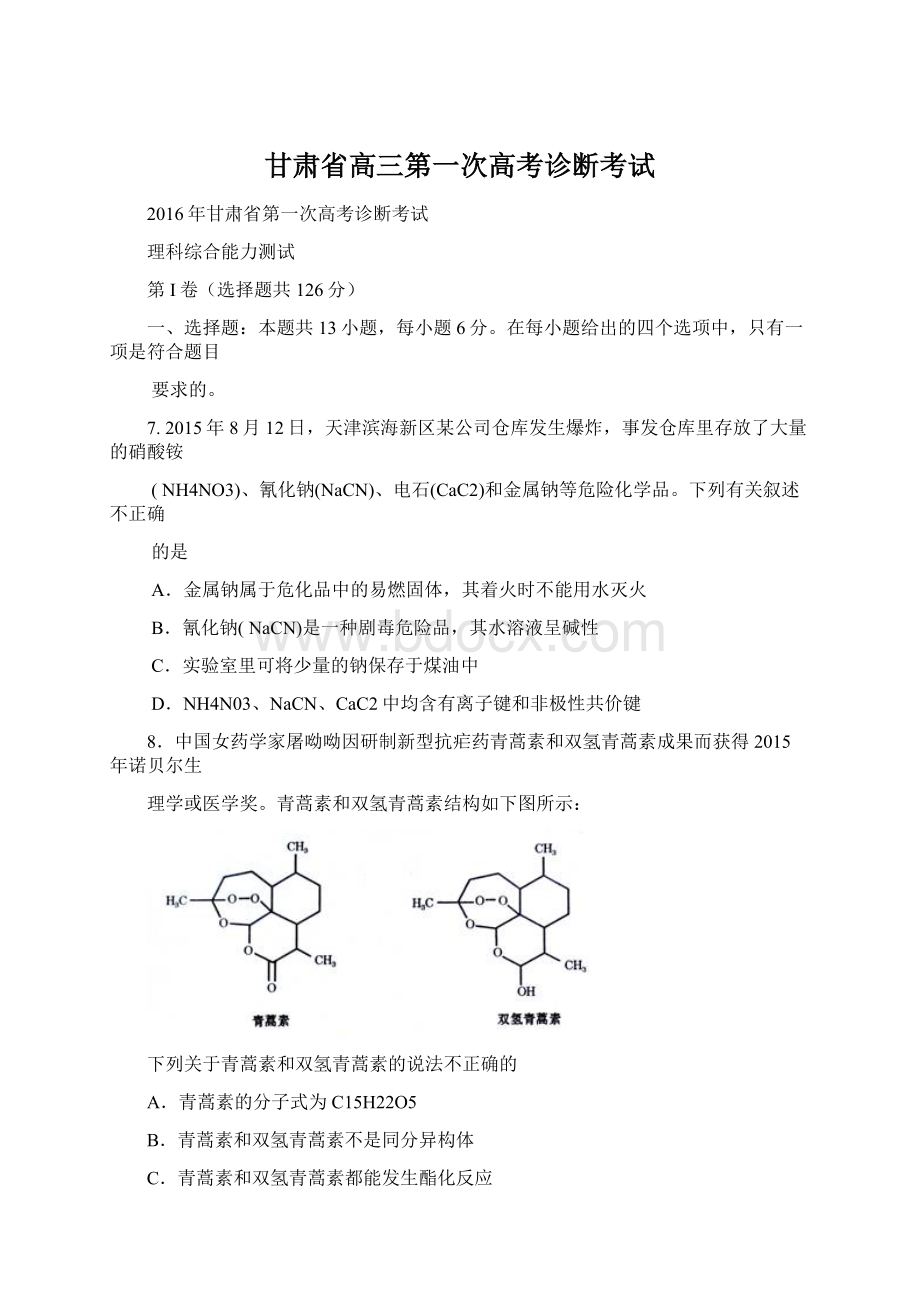
C.青蒿素和双氢青蒿素都能发生酯化反应
D.青蒿素在稀硫酸催化条件下能发生水解反应
9.下列有关电解质溶液的说法正确的是
A.在蒸馏水中滴加浓H2S04,Kw不变
B.CaC03不易溶于稀硫酸,也不易溶于醋酸
C.NaCI溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同
D.在Na2S稀溶液中,c(H+)=c(OH-)-2c(H2S)-c(HS-)
10.用NA表示阿伏加德罗常数的值,则下列叙述正确的是
A.常温常压下,46g有机物C2H60中含有极性键的数目一定为7NA
B.标准状况下,22.4L四氯化碳中所含有的共价键数目一定为4NA
C.常温常压下,14g乙烯和丙烯的混合气体中含有的原子总数一定为3NA
D.标准状况下,22.4L甲烷与22.4L氯气在光照时充分反应,生成的CH3Cl分子数一定为NA
11.据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)
和H2O2作原料的燃料电池,其负极材料采用Pt/C,正极
材料采用MnO2,可用作空军通信卫星电源,其工作原理
如右图所示。
下列说法正确的是
A.该电池的负极反应为BH4+8OH--8e-=BO2-+6H2O
B.电池放电时Na+从b极区移向a极区
C.每消耗3molH2O2,转移的电子为3mol
D.电极a采用Mn02作电极材料
12.短周期主族元素X、Y、Z、W、M的原子序数依次增大,X的气态氢化物极易溶于Y的氢化
物中,常温下,z的单质能溶于w的最高价氧化物的水化物的稀溶液,却不溶于其浓溶液。
下列说法不正确的是
A.元素W的气态氢化物与M的单质可发生置换反应
B.离子半径的大小顺序为W>
M>
Z>
X>
Y
C.元素Z、M的单质在一定条件下均能和强碱溶液反应
D.元素X与Y可以形成5种以上的化合物
13.某无色溶液中可能含有①Na+②Ba2+③Cl-④Br-⑤S042-⑥SO32-中的若干种,依次进行下
列实验,且每步所加试剂均过量,观察到的现象如下:
下列结论正确的是
A.不能确定的离子是①B.不能确定的离子是②③
C.肯定含有的离子是①④⑥D.肯定没有的离子是②⑤
26.(14分)铬及其化合物在工业上有着广泛的用途,但在生产和使用过程中易产生有毒害的
含铬工业废水。
I.处理含铬工业废水的常用方法是还原沉淀法,该方法的工艺流程如下:
(l)上述流程的步骤①中存在如下平衡:
2CrO42-(黄色)+2H+-Cr2072一(橙色)+H20。
若平衡体系的pH=0时,溶液的颜色为____色。
(2)第②步反应的离子方程式为,步骤③可通过调节第二步反应后溶液的pH
使Cr3+沉淀完全,请通过计算判断当pH>
6时,溶液中Cr3+是否沉淀完全:
。
(简要写出计算过程。
已知常温下,Cr(OH)3的溶度积Ksp=6.0x10一31,且
当溶液中离子浓度小于10-5mol.L-l时可视作该离子不存在。
)
(3)以石墨为电极电解Na2CrO4溶液制取Na2Cr207,电解装置如下图所示。
直流电源M
极的电极名称是____,和N相连的一极的电极反应式为
Ⅱ.Cr03俗称铬酸酐,常用于制备铬的化合物。
Cr03具有
强氧化性,热稳定性较差。
(4)Cr03具有强氧化性,遇到有机物(如酒精)时,猛烈反
应以至着火。
在硫酸酸化时Cr203可将乙醇氧化成乙
酸,而Cr03被还原成绿色的硫酸铬[Cr2(S04)3]。
则
该反应的化学方程式为。
(5)Cr03的热稳定性较差,加热时逐步分解,其固体残留
率随温度的变化如右图所示。
请根据图示信息写出从开始加热到750K时总反应的
化学方程式____。
27.(14分)二氧化碳是一种宝贵的碳氧资源。
以C02和NH3
为原料合成尿素是固定和利用C02的成功范例。
在尿素合成塔中的主要反应可表示
如下:
反应I:
反应Ⅱ:
总反应:
请回答下列问题:
(1)反应I的△H1=____kJ.mol-1(用具体数据表示)。
(2)反应Ⅱ的△S____(填“>
”或“<
”)0,一般在____(填“高温”或“低
温”)情况下有利于该反应的进行。
(3)-定温度下在体积为VL的容器中进行反应I,下列能说明反应达到平衡状态的是
____(填字母序号)。
A.混合气体的平均相对分子质量不再变化
B.容器内气体总压强不再变化
C.2v正(NH3)=v逆(CO2)
D.容器内混合气体的密度不再变化
(4)25℃时,将体积比为2:
1的NH3和CO2混合气体充人一个容积不变的真空密闭容
器中,在恒定温度下使其发生反应I并达到平衡。
测得平衡时混合气体的总浓度为
4.8×
10-3mol.L-1。
则此温度下,反应I的平衡常数为。
(5)总反应中影响CO:
平衡转化率的因素很多,下图为某特定条件下,不同水碳比n(H2O)/
n(CO2)和温度影响CO2平衡转化率变化的曲线。
①其它条件相同时,为提高CO2的平衡转化率,生产中可以采取的措施是
(填“提高”或“降低”)水碳比。
②当温度高于190℃后,CO2平衡转化率出现如
右图所示变化趋势的原因是____。
③不同的氨碳比()对C02的转化率也
有影响,若开始以氨碳比等于3进行总反应,达
平衡时NH3的转化率为40%,则C02的平衡转化
率为。
28.(15分)氯化亚铜广泛应用于有机合成、染料、颜料、催化剂等工业。
氯化亚铜(CuCl)是一
种白色粉末,微溶于水、不溶于乙醇、稀硝酸及稀硫酸;
可溶于氨水、浓盐酸,并生成配合物
NH4[CuCI2];
能在空气中迅速被氧化成绿色;
见光则分解,变成褐色。
下图是实验室制备
氯化亚铜的流程图及实验装置图。
实验药品:
铜丝20g、氯化铵20g、65%硝酸l0mL、36qo盐酸15mL、水。
(1)反应①的化学方程式为____,用95%乙醇代替蒸馏水洗涤的主要目的是
。
(2)本实验中通入O2的速率不宜过大,为便于观察和控制产生02的速率,宜选择下图中
的(填字母序号)方案。
(3)实验开始时,温度计显示反应液温度低于室温,主要原因是;
电炉加热升
温至50℃时停止加热,反应快速进行,烧瓶上方气体颜色逐渐由无色变为红棕色;
当
时停止通入氧气,打开瓶塞,沿(填字母)口倾出棕色反应
液于l000mL大烧杯中,加水500mL,即刻有大量白色沉淀析出。
(4)在CuCl的生成过程中除环境问题、安全问题外,你认为还应该注意的关键问题有
(5)氯化亚铜的定量分析:
①称取样品0.25g置于预先放入玻璃珠30粒和l0mL过量的FeCl3溶液的250mL锥
形瓶中,不断摇动;
玻璃珠的作用是。
②待样品溶解后,加水50mL,邻菲罗啉指示剂2滴;
③立即用0.l0mol.L-1硫酸铈标准溶液滴至绿色出现为终点并记录读数,再重复实
验二次,测得数据如下表。
④数据处理:
计算得CuCI的纯度为(平行实验结果相差不能超过0.3%)
36.【化学—选修2:
化学与技术】
(15分)
硅是带来人类文明的重要元素之一,从传统材料到信息材料的发展过程中创造了许
多奇迹。
(l)新型陶瓷Si3N4的熔点高、硬度大、化学性质稳定。
工业上可以采用化学气相沉积法,
在H2的保护下,使SiCI4与N2反应生成Si3N4沉积在石墨表面,写出该反应的化学方
程式____。
(2)已知硅的熔点是1420℃,高温下氧气及水蒸气能明显腐蚀氮化硅。
一种用工业硅(含
少量钾、钠、铁、铜的氧化物)合成氮化硅的主要工艺流程如下:
①净化N2和H2时,铜屑的作用是;
硅胶的作用是____。
②在氮化炉中3Si(s)+2N2(g)=Si3N4(S)△H=-727.5kJ.mol-l,开始时为什么要严
格控制氮气的流速以控制温度?
;
体系中要通人适量的氢气是为了____。
③X可能是(选填“盐酸”、“硝酸”、“硫酸”或“氢氟酸”)。
(3)工业上可以通过如下图所示的流程制取纯硅:
①整个制备过程必须严格控制无水无氧。
SiHCl3遇水能发生剧烈反应,写出该反应的
②假设每一轮次制备1mol纯硅,且生产过程中硅元素没有损失,反应I中HCI的利用
率为90%,反应II中H2的利用率为93.750/0。
则在第二轮次的生产中,补充投入HC1
和H:
的物质的量之比是一。
37.【化学—选修3:
物质结构与性质】
E、G、M、Q、T是五种原子序数依次增大的前四周期元素。
E、G、M是位于p区的同一周
期的元素,M的价层电子排布为ns2np2n,E与M原子核外的未成对电子数相等;
QM2与GM2-
具有相等的价电子总数;
T为过渡元素,其原子核外没有未成对电子。
(1)T元素原子的价电子排布式是____。
(2)E、G、M三种元素的第一电离能由大到小的顺序为__(用元素符号表
示),其原因为________。
(3)E、G、M的最简单氢化物中,键角由大到小的顺序为(用分子式表示),
其中G的最简单氢化物的分子立体构型名称为________,M的最简单
氢化物的分子中中心原子的杂化类型为。
M和Q的最简单氢化物的
沸点大小顺序为____(写化学式)。
(4)EM、CM+、G2互为等电子体,EM的结构式为(若有配位键,请用“→”表示)
E、M电负性相差1.0,由此可以判断EM应该为极性较强的分子,
但实际上EM分子的极性极弱,请解释其原因:
____
-。
(5)TQ在荧光体、光导体材料、涂料、颜料等行业中应用广泛。
立方TQ晶体结构如右图所示,该晶体的密度为pg·
cm-3。
如果TQ的摩尔质量为Mg.mol-1,阿伏加德罗常数为
NAmol-1,则a、b之间的距离为____cm。
38.【化学—选修5:
有机化学基础】
芳香酯I的合成路线如下:
巳知以下信息:
①A-I均为芳香族化合物,A的苯环上只有一个取代基,B能发生银镜反应,D的相对分
子质量比C大4,E的核磁共振氢谱有3组峰。
(I)A→B的反应类型为,G所含官能团的名称为。
(2)步骤E→F与F→G的顺序能否颠倒?
(填“能”或“否”),理由:
(3)B与银氨溶液反应的化学方程式为。
(4)I的结构简式为____。
(5)符合下列要求的A的同分异构体有种。
①遇氯化铁溶液显紫
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 甘肃省 第一次 高考 诊断 考试
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 (完整word版)信息论与编码期末考试题----学生复习用.doc
(完整word版)信息论与编码期末考试题----学生复习用.doc
 (完整版)固定资产盘点表.xls
(完整版)固定资产盘点表.xls
