 气体的摩尔体积 阿伏伽德罗定律解析版Word格式文档下载.docx
气体的摩尔体积 阿伏伽德罗定律解析版Word格式文档下载.docx
- 文档编号:14394774
- 上传时间:2022-10-22
- 格式:DOCX
- 页数:11
- 大小:534.15KB
气体的摩尔体积 阿伏伽德罗定律解析版Word格式文档下载.docx
《气体的摩尔体积 阿伏伽德罗定律解析版Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《气体的摩尔体积 阿伏伽德罗定律解析版Word格式文档下载.docx(11页珍藏版)》请在冰豆网上搜索。
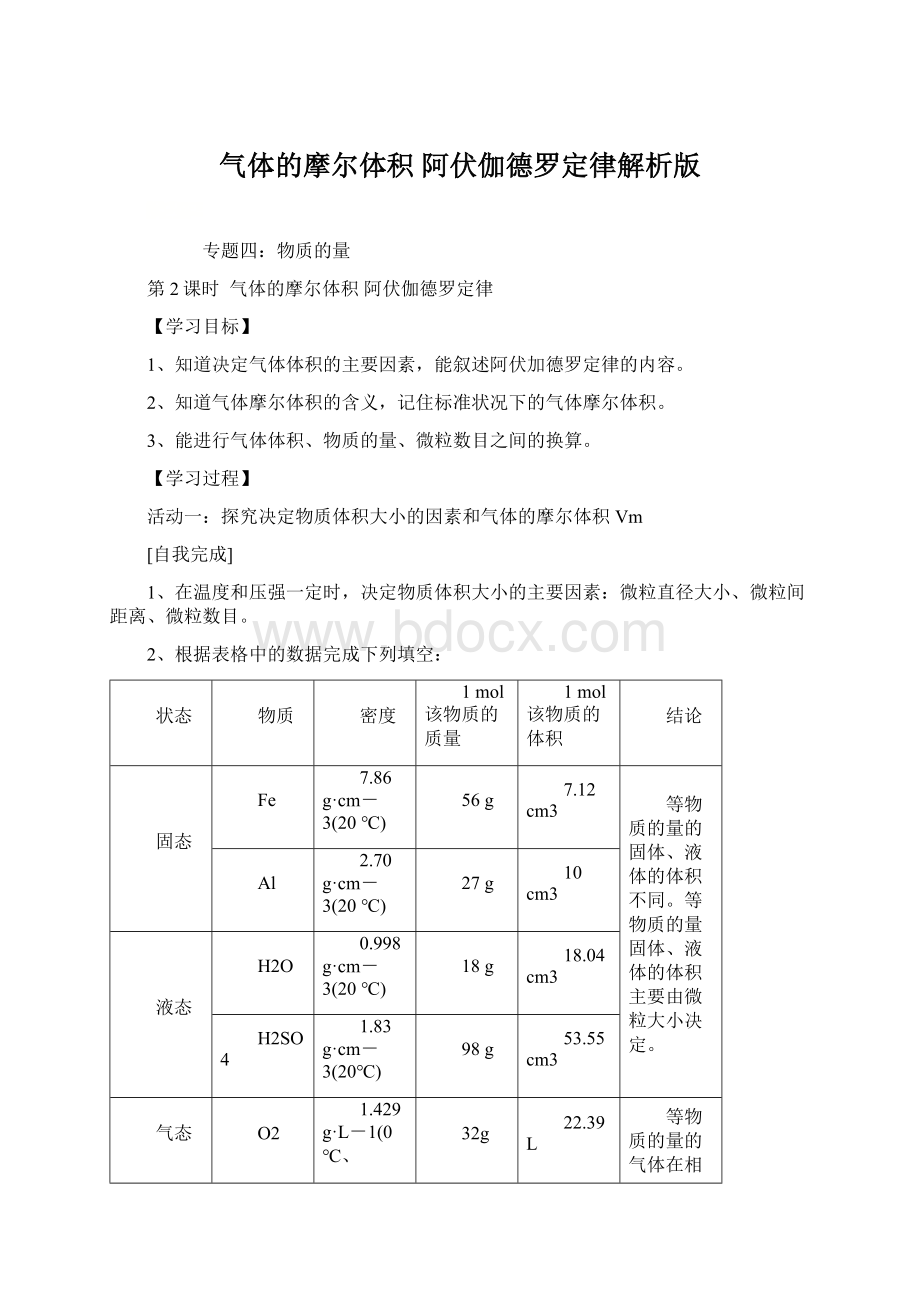
固态
Fe
7.86g·
cm-3(20℃)
56g
7.12cm3
等物质的量的固体、液体的体积不同。
等物质的量固体、液体的体积主要由微粒大小决定。
Al
2.70g·
27g
10cm3
液态
H2O
0.998g·
18g
18.04cm3
H2SO4
1.83g·
cm-3(20℃)
98g
53.55cm3
气态
O2
1.429g·
L-1(0℃、
101kPa)(标准状况)
32g
22.39L
等物质的量的气体在相同条件下的体积相同,标准状况下,1mol任何气体的体积约为22.4L。
H2
0.0899g·
2.016g
22.42L
分析出现上述结论的原因:
(1)在温度和压强一定时,任何1mol固态物质或液态物质所含微粒数目相同。
微粒之间的距离几乎相同,但微粒本身大小不同,所以1mol固态物质或液态物质的体积往往是不同的。
(2)对气态物质来说:
通常情况下微粒之间的距离要比微粒本身的直径大很多倍,因此,当微粒数相同时,气态物质体积的大小则主要取决于微粒间距离。
(3)在温度和压强一定时,气体微粒间的距离相同,因此,在相同温度和压强下,任何具有相同微粒数的气体都具有相同的体积。
一、气体的摩尔体积相关概念:
(1)定义:
单位物质的量的气体所占的体积叫做气体摩尔体积,用Vm表示
(2)数学表达式:
Vm=V/n
(3)单位:
L/mol(或L·
mol-1)和m3/mol(或m3·
mol-1)
(4)适用对象:
所有的气体(纯净气体或混合气体)
(5)气体摩尔体积的数值:
①气体摩尔体积的数值决定于气体所处的温度和压强
②标准状况(0℃,101kPa)下,1mol任何气体(纯净或混合物气体)的体积都约是22.4L。
即在标准状况下Vm=22.4L/mol。
针对性练习:
下列说法中正确的是( )
A.1molO2和1molN2所占的体积约为22.4L
B.标准状况下,H2的气体摩尔体积约为22.4L
C.在标准状况下,1molH2和1molH2O所占的体积都约为22.4L
D.0℃、101kPa,22.4LCO2和18gH2O所含的分子数相等,但是所占体积不等
【答案】D
【解析】A:
未指明状态,无法确定气体的体积,A错。
B:
气体摩尔体积的单位是L/mol,B错。
标准状况,H2O为液体,体积远小于22.4L,C错。
D:
.0℃、101kPa,即为标况,22.4LCO2和18gH2O的物质的量均为1mol,故所含的分子数相同,但它们的状态不同,故占有的体积不同,D正确。
二、标准状况下,气体摩尔体积的有关计算:
n===(标准状况)
1、在标准状况下,4gO2的体积为0.125L。
2、标况下,6.02×
1022个N2分子的体积为2.24L,质量为2.8g。
3、标况下,672mLNH3的物质的量为0.03mol,质量为0.51g,分子数目为0.03NA。
4、右图为电解水的装置图,A试管中收集的气体是H2。
若有3.6gH2O发生了电解,则B试管中收集的气体体积为2.24L(标准状况下)。
活动二:
探究阿伏伽德罗定律及其推论
一、阿伏伽德罗定律:
1、内容:
同温同压下相同体积的任何气体都含有相同数目的粒子——三同定一同
2、适用范围:
阿伏加德罗定律及其推论仅仅适用于气体,可以是单一气体,也可以是混合气体,对固体和液体不适用。
3、“三同定一同”规律:
温度、压强、体积、分子数中只要有“三同”则必有第“四同”。
二、[拓宽视野]:
关于阿伏伽德罗定律及其推论我们可以从“理想气体状态方程”来理解更易懂。
1、理想气体状态方程,又称理想气体定律、普适气体定律,是描述理想气体在处于平衡态时,压强、体积、物质的量、温度间关系的状态方程。
2、方程式为:
PV=nRT。
这个方程有4个变量:
P:
理想气体的压强;
V:
理想气体的体积,n:
气体物质的量;
T:
理想气体的热力学温度R:
理想气体常数。
3、PV=nRT的妙处——帮助理解阿伏伽德罗定律及其推论。
对于A、B两种气体:
A、同温同压同体积,一定同物质的量(阿伏伽德罗定律)
B、同温同压,V与n成正比,即:
C、同温同体积,P与n成正比,即
D、同压同体积,n与T成反比,即:
E、同温同物质的量,P与V成反比,即
F、同温同压下,,即密度之比等于摩尔质量之比。
(写出推导过程)。
*G、同温同压下,气体的密度ρ====M/22.4(标准状况下)
1、下列条件中,两种气体所含原子数一定相等的是( )
A.同质量、不同密度的N2和COB.同温度、同体积的H2和N2
C.同体积、同密度的C2H6和NOD.同压强、同体积的N2O和CO2
【答案】A
【解析】同质量的N2和CO的物质的量相同,故所含原子数一定相同。
其余选项均可用气态方程解释,选A。
2、同温同压下,同体积的氨气和硫化氢(H2S)气体的质量比为1:
2;
同质量的氨气和硫化氢气体体积比为2:
1,其中含有的氢原子数目比为3:
1;
若二者氢原子数相等,则它们的体积比为2:
3。
3、标准状况下,
(1)Cl2的密度为71/22.4=3.17g/L,
(2)100mL某气体的质量为0.286g,计算这种气体的相对分子质量。
答案:
《课时形成性练习》
1.下列叙述中,正确的是
A.1molH2的质量只有在标准状况下才约为2g
B.某气体的体积是22.4L,则可认为该气体的物质的量约为1mol
C.在20℃时,1mol的任何气体的体积总比22.4L大
D.1molH2和O2的混合气体,在标准状况下的体积约为22.4L
【解析】1molH2的质量无论在什么情况下都是2g,A错。
B中,未告知条件,无法计算气体的物质的量,B错。
气体的体积大小除了与温度有关外,还与压强有关,C错。
在标准状况下,无论是混合气体还是纯净气体,体积均约为22.4L,D正确。
选D。
2.两个体积相同的密闭容器一个盛有HCl,另个盛有H2和C12的混合气体(未发生化学反应),在同温同压下,两个容器内的气体一定具有相同的
A.质量B.密度C.分子总数D.原子总数
【答案】CD
【解析】同温同压同体积,则气体的物质的量一定相同,所以分子总数相同,C正确。
假设HCl的物质的量为1mol,原子数2NA,H2和Cl2的混合气体的物质的量也为1mol,设H2为xmol,Cl2为(1-x)mol,原子的物质的量为:
2x+2(1-x)=2mol,即原子总数为2NA,所以两个容器中的原子总数相同,D正确。
选C、D。
3.在一定体积的容器中加入1.5mol氙气(Xe)和7.5mol氟气(F2),于400℃和2633kPa压强下加热数小时,然后迅速冷却至25℃,容器内除得到一种无色晶体外,还余下4.5mol氟气,则所得无色晶体产物中,氙与氟的原子个数之比
A.1:
2B.1:
3C.1:
4D.1:
6
【答案】C
【解析】由题意可知,1.5molXe与3mol(7.5-4.5)F2反应生成无色晶体,故Xe原子个数与F原子个数之比是1.5:
6=1:
4,选C。
4.下列说法中,正确的是
A.lmol任何物质的体积都约是22.4LB.标准状况下,相同物质的量的H2与O2的体积都约为22.4L
C.0℃,101kPa,l6gO2的体积约是22.4LD.标准状况下,l8g水的体积远小于22.4L
【解析】H2O的密度为1g/mL,18gH2O即18mL,其体积远小于22.4L,选D。
5.等质量的下列物质在常温常压下体积最大的是
A.浓硫酸B.CO2C.铁粉D.冰水混合物
【答案】B
【解析】CO2在常温下是气体,其余为非气体,当质量相同时,CO2的体积最大,选B。
6.amolH2和2amol氦气具有相同的
A.分子数B.原子数C.体积D.质量
【解析】氦气分子是单原子分子(He),amolH2和2amolHe含有的原子数为2aNA,选B。
7.如图所示,两瓶体积相等的气体,在同温同压时瓶内气体(N2O和CO2不发生化学反应)的关系不一定正确的是
A.所含氧原子数相等B.气体的总质量相等C.气体所含电子总数相等D.气体的密度相等
【解析】同温同压下,气体体积之比等于物质的量之比,两瓶气体的物质的量相等。
N2O和CO2含有的O原子数目不同,则两个集气瓶中含有O原子的物质的量不同,含有氧原子数不同,A错误;
N2O和CO2的摩尔质量都是44g·
mol-1,两瓶气体的物质的量相等,根据m=nM可知气体的总质量相等,B正确;
N2O和CO2都含有22个电子,两瓶气体的物质的量相等,含有电子数相等,C正确;
N2O和CO2的摩尔质量相同,根据ρ=可知相同条件下两瓶气体的密度相等,D正确。
8.在标准状况下,mgA气体与ngB气体分子数相等,下列说法不正确的是
A.标准状况下,同体积的气体A和气体B的质量比m∶n
B.25℃时,1kg气体A与1kg气体B的分子数之比为n∶m
C.同温同压下,气体A与气体B的密度之比为m∶n
D.标准状况下,等质量的A与B的体积比为m∶n
【解析】在标准状况下,mgA气体与ngB气体分子数相等,则A气体与B气体的摩尔质量之比为m∶n。
A项,同温同压,同体积的气体质量之比等于摩尔质量之比,所以同体积的气体A和气体B的质量比为m∶n,正确;
B项,相同质量,分子数与摩尔质量成反比,所以1kg气体A与1kg气体B的分子数之比为n∶m,正确;
C项,同温同压下,气体A与气体B的密度之比等于摩尔质量之比,所以气体A与气体B的密度之比为m∶n,正确;
D项,同温同压下,相同质量的气体体积与摩尔质量成反比,所以标准状况下,等质量的A与B的体积比为n∶m,错误。
9.同温同压下,下列气体的密度最大的是( )
A.F2B.Cl2C.HClD.CO2
【解析】同温同压下,气体摩尔体积相等。
氟的摩尔质量是38g·
mol-1,氯气的摩尔质量是71g·
mol-1,氯化氢的摩尔质量是36.5g·
mol-1,二氧化碳的摩尔质量是44g·
mol-1;
根据ρ=知,气体密度大小与其摩尔质量成正比,所以摩尔质量越大,其密度越大,所以密度最大的是氯气,B正确。
10.一定温度和压强下,2体积AB2气体和1体积B2气体化合生成2体积气态化合物,则该化合物的化学式为
A.AB3B.AB2C.A3BD.A2B3
【解析】令生成的气体的化学式为X,同温同压下,气体的体积之比等于物质的量之比,2体积AB2气体和1体积B2气体化合生成2体积气态化合物X,则反应方程式为2AB2+B2===2X,根据原子守恒,所以X为
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 气体的摩尔体积 阿伏伽德罗定律解析版 气体 摩尔 体积 阿伏伽德 罗定 解析
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 转基因粮食的危害资料摘编Word下载.docx
转基因粮食的危害资料摘编Word下载.docx
