 第三章 专题复习晶体类型的判断及晶体结构的分析与计算分类训练Word格式文档下载.docx
第三章 专题复习晶体类型的判断及晶体结构的分析与计算分类训练Word格式文档下载.docx
- 文档编号:14333443
- 上传时间:2022-10-22
- 格式:DOCX
- 页数:7
- 大小:48.62KB
第三章 专题复习晶体类型的判断及晶体结构的分析与计算分类训练Word格式文档下载.docx
《第三章 专题复习晶体类型的判断及晶体结构的分析与计算分类训练Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《第三章 专题复习晶体类型的判断及晶体结构的分析与计算分类训练Word格式文档下载.docx(7页珍藏版)》请在冰豆网上搜索。
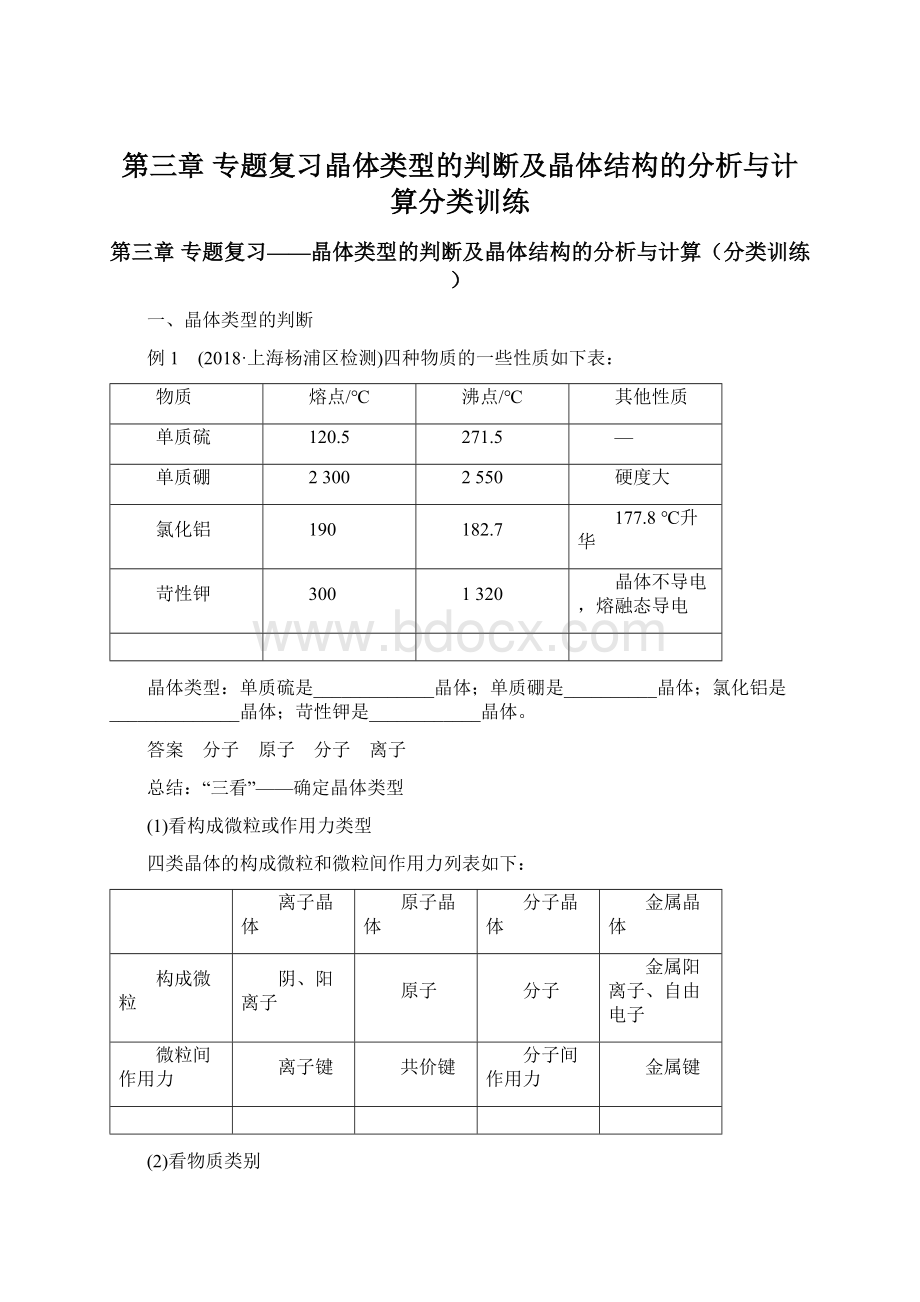
苛性钾
300
1320
晶体不导电,熔融态导电
晶体类型:
单质硫是_____________晶体;
单质硼是__________晶体;
氯化铝是______________晶体;
苛性钾是____________晶体。
答案 分子 原子 分子 离子
总结:
“三看”——确定晶体类型
(1)看构成微粒或作用力类型
四类晶体的构成微粒和微粒间作用力列表如下:
离子晶体
原子晶体
分子晶体
金属晶体
构成微粒
阴、阳离子
原子
分子
金属阳离子、自由电子
微粒间作用力
离子键
共价键
分子间作用力
金属键
(2)看物质类别
①单质类:
a.金属单质和合金属于金属晶体;
b.大多数非金属单质(金刚石、石墨、晶体硅、晶体硼等除外)属于分子晶体。
②化合物类:
a.离子化合物一定为离子晶体;
b.共价化合物绝大多数为分子晶体,但SiO2、SiC等为原子晶体。
(3)看物理性质
四类晶体的物理性质对比如下:
晶体类型
熔、沸点
一般较高、但差异大
较高
较低
高
硬度
一般较大,但差异大
较大
较小
大
导电性
固态能导电
固态不导电,熔融态或溶于水时能导电
固态不导电,某些溶于水后能导电
一般不导电,个别为半导体
二、晶体熔、沸点的比较
例2 下列各组物质的沸点按由低到高的顺序排列的是( )
A.NH3、CH4、NaCl、NaB.H2O、H2S、MgSO4、SO2
C.CH4、H2O、NaCl、SiO2D.Li、Na、K、Rb、Cs
答案 C
总结归纳:
比较不同晶体熔、沸点的基本思路
首先看物质的状态,一般情况下是固体>
液体>
气体;
二看物质所属类型,一般是原子晶体>
离子晶体>
分子晶体(注意:
不是绝对的,如氧化铝的熔点大于晶体硅),结构类型相同时再根据相应规律进行判断。
同类晶体熔、沸点比较思路:
原子晶体→共价键键能→键长→原子半径;
分子晶体→分子间作用力→相对分子质量;
离子晶体→离子键强弱→离子所带电荷数、离子半径;
金属晶体→金属键→金属阳离子所带电荷、金属阳离子半径。
三、关于晶胞结构的分析与计算
例3
(1)镧系合金是稀土系储氢合金的典型代表,由荷兰菲利浦实验室首先研制出来。
它的最大优点是容易活化。
其晶胞结构如图所示:
则它的化学式为____________。
(2)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,下图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);
B为(,0,);
C为(,,0)。
则D原子的坐标参数为________。
②晶胞参数,描述晶胞的大小和形状,已知Ge单晶的晶胞参数a=565.76pm,其密度为________g·
cm-3(列出计算式即可)。
(3)GaAs的熔点为1238℃,密度为ρg·
cm-3,其晶胞结构如图所示。
该晶体的类型为________,Ga与As以________键结合。
Ga和As的摩尔质量分别为MGag·
mol-1和MAsg·
mol-1,原子半径分别为rGapm和rAspm,阿伏加德罗常数值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为_____________________________。
答案
(1)LaNi5
(2)①(,,) ②×
107
(3)原子晶体 共价 ×
100%
归纳总结:
1.晶胞计算的类型
(1)根据晶胞的结构,计算其组成微粒间的距离。
(2)根据晶胞的质量和晶体有关的摩尔质量间的关系,计算微粒个数、微粒间距、ρ等。
(3)计算晶体(晶胞)的空间利用率。
2.晶胞计算的原理与步骤
(1)首先确定晶胞的组成
利用均摊法计算一个晶胞所含微粒的数目。
(2)计算晶体的密度或体积
①关系式ρ=(V表示晶胞体积,ρ表示晶体的密度,NA表示阿伏加德罗常数,N表示一个晶胞实际含有的微粒数,M表示微粒的摩尔质量)。
②计算模式
晶体的密度
③晶胞空间利用率(占有率)的计算表达式
晶胞的空间利用率=×
100%。
强化训练:
1.AB型化合物形成的晶体结构多种多样。
下图所示的几种结构所表示的物质最有可能是分子晶体的是( )
A.①③B.②⑤C.⑤⑥D.③④⑤⑥
答案 B
2. 在解释下列物质的变化规律与物质结构间的因果关系时,与化学键的强弱无关的是( )
A.钠、镁、铝的熔点和沸点逐渐升高,硬度逐渐增大
B.金刚石的硬度大于晶体硅的硬度,其熔点也高于晶体硅的熔点
C.KF、KCl、KBr、KI的熔点依次降低
D.F2、Cl2、Br2、I2的熔点和沸点逐渐升高
答案 D
3.(2019·
南京高二期末)下列各组物质中都属于原子晶体的是( )
A.干冰、二氧化硅、金刚石
B.氧化钠、金刚石、氯化氢
C.碘、石墨、氯化钠
D.二氧化硅、金刚石、晶体硼
4.列有关晶体性质的比较正确的是( )
A.熔点:
金刚石>晶体硅>碳化硅
B.沸点:
NH3>H2O>HF
C.硬度:
白磷>冰>二氧化硅
D.熔点:
SiI4>SiBr4>SiCl4
5.如图是CaF2晶胞的结构图。
下列说法正确的是( )
A.一个CaF2晶胞中含有8个Ca2+
B.一个CaF2晶胞中含有8个F-
C.在CaF2晶胞中Ca2+的配位数为4
D.在CaF2晶胞中F-的配位数为8
6.(2019·
福州高二期末)下列有关晶体结构的叙述正确的是( )
A.SiO2晶体中最小环上的原子个数为6
B.在晶体中只要有阳离子就一定有阴离子
C.12g石墨烯(如图1)中含有六元环的个数为0.5×
6.02×
1023
D.720gC60晶体中含有0.5×
1023个晶胞(如图2)
7.有一种蓝色晶体[可表示为:
MFey(CN)6],经研究发现,它的结构特征是Fe3+和Fe2+互相占据立方体互不相邻的顶点,而CN-位于立方体的棱上。
其晶体中阴离子的最小结构单元如图所示。
下列说法错误的是( )
A.该晶体的化学式为MFe2(CN)6
B.该晶体熔融可导电,且属于化学变化
C.该晶体属于离子晶体,M呈+2价
D.晶体中与每个Fe3+距离最近且等距离的CN-有6个
8.F2和Xe在一定条件下可生成XeF2、XeF4和XeF6三种氟化氙,它们都是极强的氧化剂(其氧化性依次增强),都极易与水反应。
已知6XeF4+12H2O===2XeO3+4Xe↑+24HF+3O2↑,下列推测正确的是( )
A.XeF2分子中各原子均达到8电子的稳定结构
B.某种氟化氙晶体的基本结构单元如图所示,可推知其化学式为XeF6
C.XeF4与水反应时,每生成2molXe转移8mol电子
D.XeF2加入水中,在水的作用下,将生成Xe和F2
9、
(1)Cu的一种氯化物晶胞结构如图所示(黑球表示铜原子,白球表示氯原子),该氯化物的化学式是_______________________________________________________________。
若该晶体的密度为ρg·
cm-3,以NA表示阿伏加德罗常数的值,则该晶胞的边长a=_____nm。
(2)用晶体的X射线衍射法对Cu的测定得到以下结果:
Cu的晶胞为面心立方最密堆积(如图),已知该晶体的密度为9.00g·
cm-3,Cu的原子半径为________cm(阿伏加德罗常数的值为NA,只要求列式表示)。
(3)一种铜金合金晶胞如图所示(Au原子位于顶点,Cu原子位于面心),则该合金中Au原子与Cu原子个数之比为________,若该晶胞的边长为apm,则合金的密度为____g·
cm-3(只要求列算式,不必计算出数值,阿伏加德罗常数的值为NA)。
答案
(1)CuCl
(2)×
(3)1∶3
10.(2019·
合肥高二月考)
(1)①KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。
K与O间的最短距离为______nm,与K紧邻的O个数为________。
②在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于________位置,O处于________位置。
(2)MgO具有NaCl型结构(如图),其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得MgO的晶胞参数为a=0.420nm,则r(O2-)为________nm。
MnO也属于NaCl型结构,晶胞参数为a′=0.448nm,则r(Mn2+)为________nm。
答案
(1)①0.315 12 ②体心 棱心
(2)0.148 0.076
11氮元素可形成丰富多彩的物质。
(1)光化学烟雾易在PM2.5的催化作用下形成,其中含有NOx、O3、CH2==CHCHO、HCOOH等二次污染物。
下列说法正确的是________(填字母)。
A.不能用排空气法收集NO
B.O3的沸点高于O2的沸点
C.CH2==CHCHO分子中碳原子采取sp2和sp3杂化
D.HCOOH在水中的溶解度大,与氢键有关
(2)在配合物中,微粒NH3、NH、NH2OH中不能作为配体的是__________。
(3)图a为六方氮化硼晶体的结构示意图,该晶体中存在的作用力有______________。
(4)六方氮化硼在高温高压下可转化为立方氮化硼,立方氮化硼的晶胞结构如图b所示,晶胞边长为dcm,该晶胞中含有________个氮原子、________个硼原子,立方氮化硼晶体的密度为________g·
cm-3(设阿伏加德罗常数的值为NA)。
答案
(1)ABD
(2)NH (3)共价键、范德华力
(4)4 4
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 第三章 专题复习晶体类型的判断及晶体结构的分析与计算分类训练 第三 专题 复习 晶体 类型 判断 晶体结构 分析 计算 分类 训练
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《雷雨》中的蘩漪人物形象分析 1.docx
《雷雨》中的蘩漪人物形象分析 1.docx
