 华东师大版版九年级上学期第一次月考科学试题II卷Word文档下载推荐.docx
华东师大版版九年级上学期第一次月考科学试题II卷Word文档下载推荐.docx
- 文档编号:14324478
- 上传时间:2022-10-22
- 格式:DOCX
- 页数:15
- 大小:327.39KB
华东师大版版九年级上学期第一次月考科学试题II卷Word文档下载推荐.docx
《华东师大版版九年级上学期第一次月考科学试题II卷Word文档下载推荐.docx》由会员分享,可在线阅读,更多相关《华东师大版版九年级上学期第一次月考科学试题II卷Word文档下载推荐.docx(15页珍藏版)》请在冰豆网上搜索。
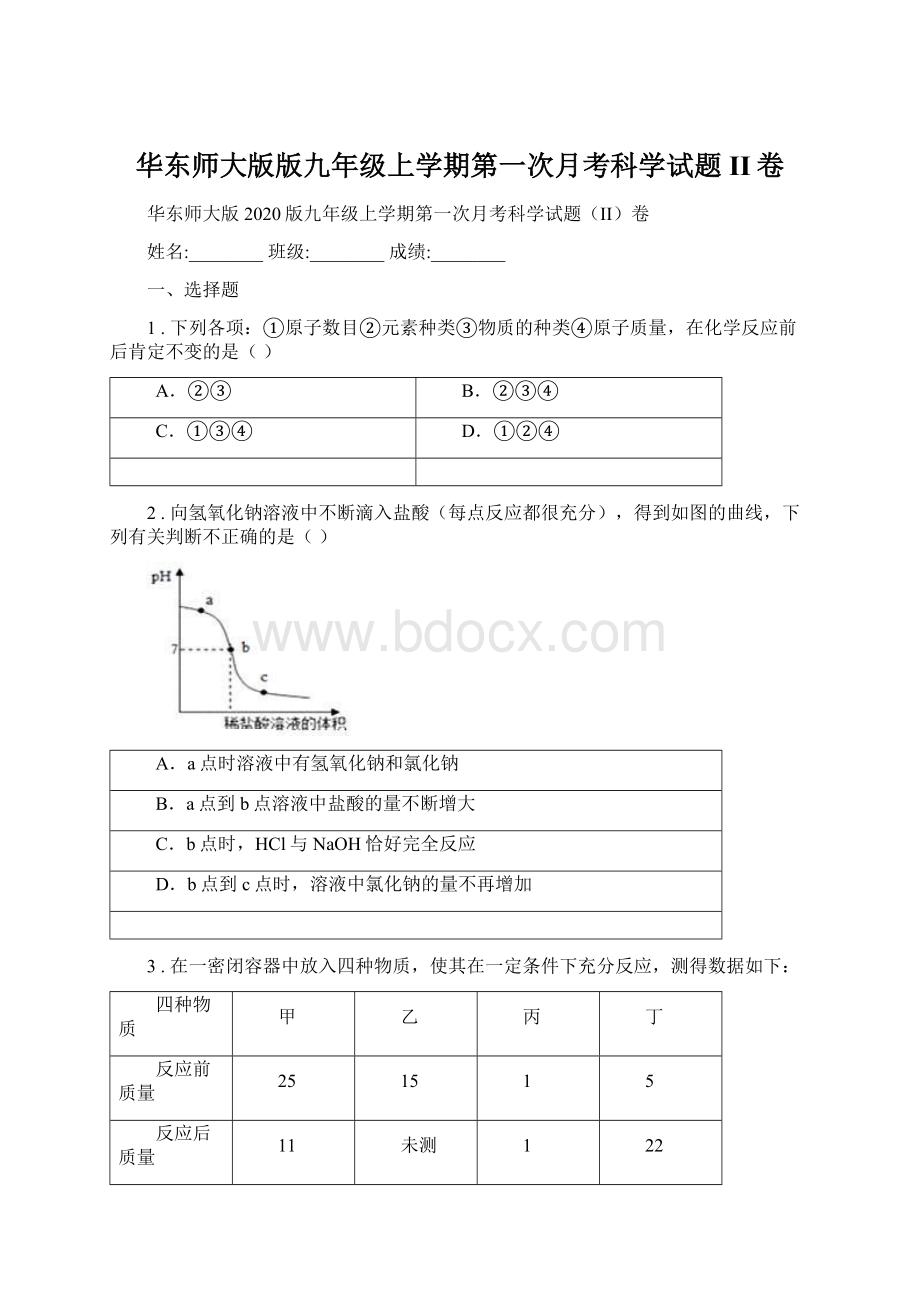
丁
反应前质量
25
15
1
5
反应后质量
11
未测
22
对于下列叙述正确的是()
A.未测值为3g
B.丙一定是催化剂
C.乙全部参加了反应
D.甲与乙反应的质量比为14:
3
4.下列除去杂质的方法中,错误的是()
选项
物质
杂质
除杂质的方法
A.
稀硫酸
铜
过滤
B.
CaSO4溶液
过量CaCO3、过滤
C.
FeCl2溶液
CuCl2
过量铁粉、过滤
D.
二氧化碳
一氧化碳
点燃
A.A
B.B
C.C
D.D
5.t℃时,向一只盛有0.15g熟石灰的烧杯中加入50g水,充分振荡后静置,烧杯底部仍有未溶解的白色固体。
下列相关叙述正确的是()
A.烧杯中溶液的质量小于50.15g
B.t℃时,熟石灰的溶解度为0.3g
C.降低温度后,未溶解的白色固体会增加
D.升高温度后,溶液变为不饱和溶液
6.下图是制作临时装片的四个步骤,这四个步骤的正确顺序应该是:
()
A.④②①③
B.②③④①
C.①②③④
D.②④③①
7.下列实验方案设计合理的是()
实验目的
实验方案
A
除去氢氧化钠溶液中少量碳酸钠
加过量的氢氧化钙溶液后过滤
B
除去氧化钙中少量碳酸钙
加适量的稀盐酸
C
除去氯化钾中的碳酸钾
D
除去稀盐酸中的氯化钠溶液
加适量的硝酸银溶液后过滤
A.A
B.B
C.C
D.D
8.向一定质量的稀盐酸中加入镁粉至过量,若下图中横坐标表示镁粉的质量,则纵坐标表示()
A.溶液的质量
B.稀盐酸的质量
C.氯化镁的质量
D.生成气体的质量
9.把6.5g含杂质的锌放入足量稀硫酸中,完全反应后放出0.19g氢气,则锌中可能含有的杂质为(只含有一种杂质)()
A.Mg
B.A1
C.Fe
D.Cu
10.用如图所示装置(图中夹持仪器已略去)测定某牙膏样品中碳酸钙的质量分数。
实验中,通过测定丙装置质量的改变值,就能达到目的(样品中其他成分遇盐酸不产生气体)。
下列措施能提高测定准确度的是()
A.省去装置甲和丁
B.将丙中的NaOH溶液换成Ca(OH)2溶液
C.装置乙不再产生气泡时,立即停止抽气
D.滴加稀盐酸之前,先抽气一段时间,除去装置内原有的CO2
11.二氧化硫气体是造成酸雨的主要气体,其水溶液叫亚硫酸(H2SO3)。
硫化氢(H2S)是一种具有臭鸡蛋气味的剧毒气体,其水溶液叫氢硫酸。
已知相同的条件下,氢硫酸的酸性弱于亚硫酸。
现在室温下向饱和的亚硫酸溶液中通入过量的硫化氢气体,反应的化学方程式为:
2H2S+H2SO3="
="
3S↓+3H2O。
则下图中溶液的pH随通入硫化氢体积的变化曲线示意图正确的是()
12.关于酸、碱、盐及氧化物,下列说法正确的是()
A.pH为3的盐酸溶液加水稀释,可以配制成pH为2的盐酸溶液
B.酸和碱一定含有氢元素,盐可能含有氢元素
C.固体氢氧化钠需密封保存的一个原因是为了避免它与空气中的水蒸气发生化学反应而潮解
D.酸、碱、盐在水溶液里都可以离解成自由移动的离子,如氢氧化铁可以使紫色石蕊变蓝
13.下列物质的名称、俗名与化学式完全正确对应的是()
A.氢氧化钠
纯碱
NaOH
B.碳酸氢钠、纯碱、NaHCO3
C.氢氧化钙
熟石灰
Ca(OH)2
D.氯化钠、食盐、NaCl2
14.下列物质露置在空气中一段时间后。
因为发生化学变化而质量增加的是()
A.浓硫酸
B.氢氧化钠
C.浓盐酸
D.石灰石
15.某电镀厂排出的废水中含有较多的硫酸铜(CuSO4)。
若要从硫酸铜中获得金属铜,可选择下列物质中的()
A.稀盐酸
C.银粉
D.铁粉
二、填空题
16.纯净物可以分为____和______________,单质按照性质又可分为_______________和_______________,化合物根据组成和性质又可分为___________________和
______________________,无机化合物根据组成和性质又可以分为_____________、____、____、____。
17.亚硝酸钠是实验室常用的试剂,实验室一般用亚硝酸钠溶液与氯化铵溶液反应来制取N2。
N2的化学性质十分稳定,但在一定条件下能与H2部分化合生成NH3。
如图为制取少量NH3的装置(制取H2的装置已略去):
(1)请写出图中仪器B名称:
___________________;
(2)写出C装置的硬质试管中发生反应的化学方程式:
_______________________;
(3)结合本实验装置,证明确实有NH3生成的简单方法以及实验现象__________;
(4)归纳与演绎是重要的科学方法,也是常用的学习方法。
我们已经学过实验室制取气体的反应原理、制取与收集方法。
请你归纳出实验室制取气体反应的共同点:
___________(填序号)。
①需要加热
②使用催化剂
③没有气体参加反应
④原料为纯净物
⑤只生成一种气体
18.铝是一种银白色的金属,是制造各种轻质结构的重要材料。
铝有良好的导电性,可以用来做导线。
铝粉或铝箔在氧气中燃烧时,会发出耀眼的白光,常用于制造燃烧弹、照明弹。
铝还有良好的导热性,因此大量用于制造炊具。
仔细阅读上述材料,回答:
(1)物质的用途一般由该物质具有的______决定;
(2)铝的物理性质有_____________________________________________;
(3)铝的化学性质有_____________________________________________;
(4)物理变化和化学变化的根本区别在于___________________________。
19.用毛笔蘸取溶质质量分数为5%的稀硫酸在竹片上画花,然后把竹片放在小火上烘干,再用水洗净,在竹片上就得到黑色或褐色的花样,一幅精美的竹片画就制成了。
(1)稀硫酸在烘干的过程中成为浓硫酸,浓硫酸使富含纤维素的竹片呈现黑色或褐色,在这个过程中竹片发生了________________________(选填“物理变化”或“化学变化”)。
(2)直接用浓硫酸在竹片上画花具有危险性,必须将浓硫酸进行稀释,稀释时切不可把_________倒入_________中。
20.藻类和草履虫在光下生活于同一溶液中。
已知草履虫每星期消耗18g葡萄糖,藻类每星期消耗21.6g葡萄糖。
现在该溶液中每星期葡萄糖的净产量为0.54g。
这一溶液中每星期氧的净产量是
g。
21.铝元素与人类关系密切。
(1)铝是地壳中含量最高的________________元素;
(2)元素周期表中铝元素的信息如图所示,其原子的核外电子数为_____________;
(3)
铝元素在自然界中主要以Al2O3存在,Al2O3属于___________(填字母序号);
A.单质
B.氧化物
C.碱
D.盐
(4)工业用电解熔融Al2O3的方法冶炼铝,化学方程式为2Al2O34Al+3O2↑,该反应属于基本反应类型中的___________反应;
(5)铝可制成蒸锅,主要利用铝的延展性和__________性;
(6)药品氢氧化铝片剂能与胃酸(主要成分为盐酸)发生中和反应,治疗胃酸过多症,
该反应的化学方程式为___________________________________。
三、探究题
22.某研究性学习小组查阅资料得知,宇宙飞船中可用超氧化钾(KO2)作为氧气再生剂。
超氧化钾是一种固体,它与人呼出的二氧化碳反应生成氧气:
4KO2+2CO2==2K2CO3+3O2为了验证这个反应能够产生氧气,该小组同学以大理石和盐酸反应生成的CO2来与KO2反应制取O2,设计了如下实验装置:
(1)C处应从A、B两种装置中选择____________作CO2发生装置。
(2)已知CO2不溶于饱和碳酸氢钠溶液,D装置作用是为了除去CO2气体中可能混有的____________。
(3)有同学提出,CO2中混有的水蒸气可能会对实验产生影响。
若要检验干燥的CO2能否与超氧化钾反应生成氧气,你对实验装置的改进方法是__________。
23.有一包白色粉末A,由CuSO4、CaCO3、BaCl2、Na2SO4、NaOH中的两种或两种以上的物质混合而成。
为探究其组成,进行如下实验(实验流程如图):
(1)取白色粉末A,向其中加入足量水,充分搅拌后过滤,得到白色沉淀B和无色滤液C。
由此可判断,原白色粉末中一定不含有_____。
(2)向白色沉淀B中加入足量稀盐酸,沉淀全部溶解,并产生无色气体。
由此可判断,原白色粉末中一定含有_____。
(3)向无色滤液C中通入一定量二氧化碳,充分反应后过滤,得到白色沉淀D和无色滤液E,由此可判断,原白色粉末中一定还含有_____。
(4)若流程图中白色粉末A为20g,白色沉淀D为9.85g,无色滤液E中只含一种溶质。
①无色滤液E中的溶质为_____;
②通过计算确定20g白色粉末A中所含各物质的质量。
_____(请写出计算及推理过程)
24.在一次科学实验中,同学们将饱和CuSO4溶液逐滴加到5mL饱和NaOH溶液中,观察到以下异常实验现象:
实验序号
滴加CuSO4溶液的量
实验现象
①
第1﹣6滴
产生蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液
②
第7﹣9滴
产生蓝色沉淀,且沉淀逐渐增多。
振荡后沉淀不消失,
很快沉淀逐渐变黑色
在实验①中同学们根据所学初中化学知识判断蓝色沉淀是Cu(OH)2
,蓝色沉淀为什么消失?
同学们继续进行如下探究。
(查阅资料)Ⅰ.Cu(OH)2在室温下稳定,70℃﹣80℃时可分解生成CuO和水
Ⅱ.酮酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色
(猜想与讨论)小陶认为蓝色沉淀消失可能是Cu(OH)2发生了分解。
其他同学一致否定了他的猜测,理由是同学们交流讨论后,提出以下两种猜想。
猜想一:
少许Cu(OH)2可溶于足量水中。
猜想二:
Cu(OH)2可在足量NaOH浓溶液中溶解,溶液呈亮蓝色
(1)(实验探究)为验证猜
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 华东师大 九年级 上学 第一次 月考 科学 试题 II
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《雷雨》中的蘩漪人物形象分析 1.docx
《雷雨》中的蘩漪人物形象分析 1.docx
