 初三化学用语及常见物质的化学式Word下载.doc
初三化学用语及常见物质的化学式Word下载.doc
- 文档编号:14227831
- 上传时间:2022-10-20
- 格式:DOC
- 页数:4
- 大小:104.50KB
初三化学用语及常见物质的化学式Word下载.doc
《初三化学用语及常见物质的化学式Word下载.doc》由会员分享,可在线阅读,更多相关《初三化学用语及常见物质的化学式Word下载.doc(4页珍藏版)》请在冰豆网上搜索。
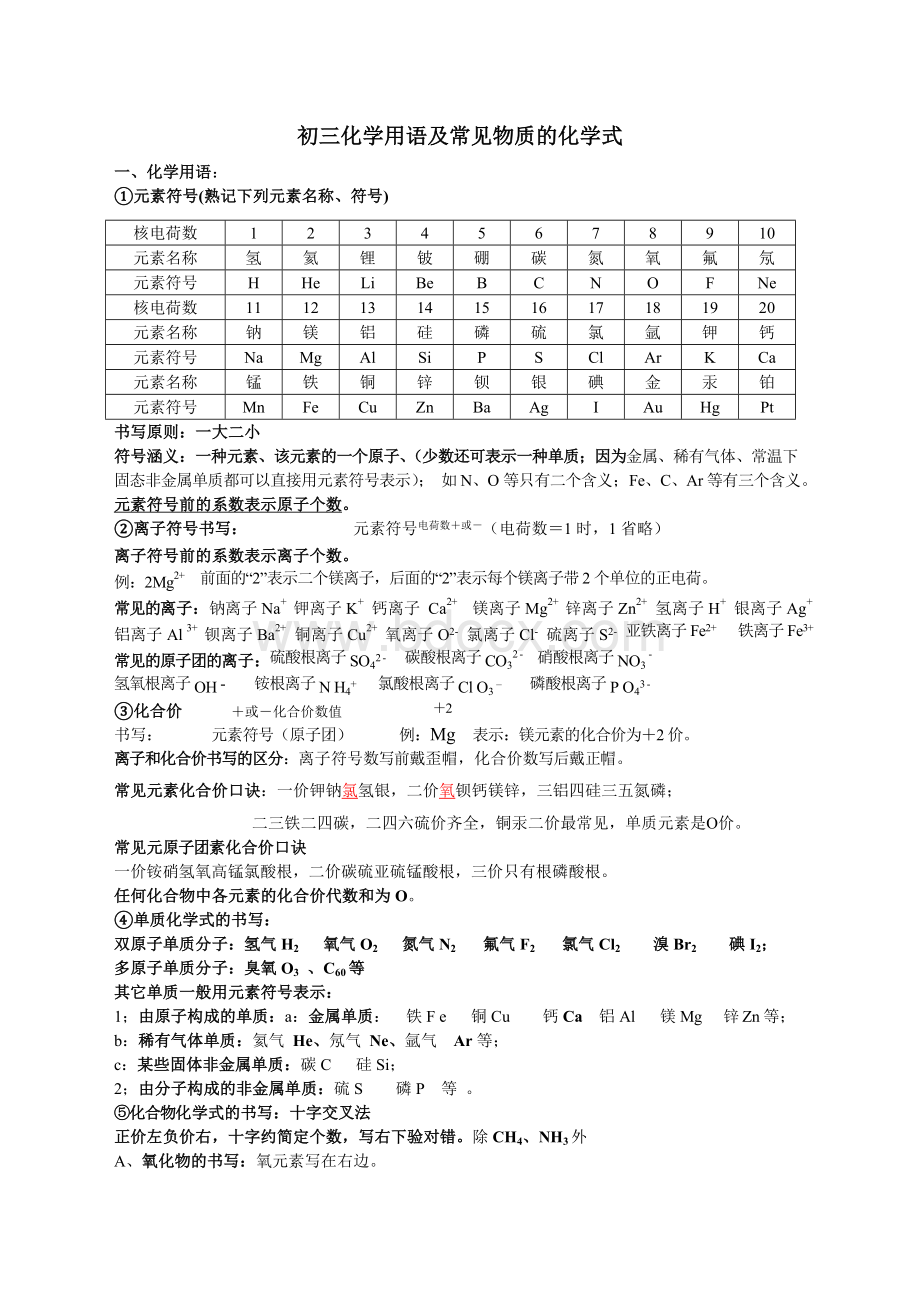
12
13
14
15
16
17
18
19
20
钠
镁
铝
硅
磷
硫
氯
氩
钾
钙
Na
Mg
Al
Si
P
S
Cl
Ar
K
Ca
锰
铁
铜
锌
钡
银
碘
金
汞
铂
Mn
Fe
Cu
Zn
Ba
Ag
I
Au
Hg
Pt
书写原则:
一大二小
符号涵义:
一种元素、该元素的一个原子、(少数还可表示一种单质;
因为金属、稀有气体、常温下
固态非金属单质都可以直接用元素符号表示);
如N、O等只有二个含义;
Fe、C、Ar等有三个含义。
元素符号前的系数表示原子个数。
②离子符号书写:
元素符号电荷数+或-(电荷数=1时,1省略)
离子符号前的系数表示离子个数。
例:
2Mg2+ 前面的“2”表示二个镁离子,后面的“2”表示每个镁离子带2个单位的正电荷。
常见的离子:
钠离子Na+钾离子K+钙离子Ca2+镁离子Mg2+锌离子Zn2+氢离子H+银离子Ag+
铝离子Al3+钡离子Ba2+铜离子Cu2+氧离子O2-氯离子Cl-硫离子S2-亚铁离子Fe2+铁离子Fe3+
常见的原子团的离子:
硫酸根离子SO42-碳酸根离子CO32-硝酸根离子NO3-
氢氧根离子OH-铵根离子NH4+氯酸根离子ClO3–磷酸根离子PO43-
③化合价 +或-化合价数值 +2
书写:
元素符号(原子团) 例:
Mg 表示:
镁元素的化合价为+2价。
离子和化合价书写的区分:
离子符号数写前戴歪帽,化合价数写后戴正帽。
常见元素化合价口诀:
一价钾钠氯氢银,二价氧钡钙镁锌,三铝四硅三五氮磷;
二三铁二四碳,二四六硫价齐全,铜汞二价最常见,单质元素是O价。
常见元原子团素化合价口诀
一价铵硝氢氧高锰氯酸根,二价碳硫亚硫锰酸根,三价只有根磷酸根。
任何化合物中各元素的化合价代数和为O。
④单质化学式的书写:
双原子单质分子:
氢气H2氧气O2氮气N2氟气F2氯气Cl2溴Br2碘I2;
多原子单质分子:
臭氧O3、C60等
其它单质一般用元素符号表示:
1;
由原子构成的单质:
a:
金属单质:
铁Fe铜Cu钙Ca铝Al镁Mg锌Zn等;
b:
稀有气体单质:
氦气He、氖气Ne、氩气Ar等;
c:
某些固体非金属单质:
碳C硅Si;
2;
由分子构成的非金属单质:
硫S磷P等。
⑤化合物化学式的书写:
十字交叉法
正价左负价右,十字约简定个数,写右下验对错。
除CH4、NH3外
A、氧化物的书写:
氧元素写在右边。
水H2O二氧化碳CO2一氧化碳CO二氧化硫SO2三氧化硫SO3五氧化二磷P2O5氧化铁Fe2O3
四氧化三铁Fe3O4氧化亚铁FeO氧化钙CaO氧化镁MgO氧化铜CuO氧化锌ZnO二氧化锰MnO2
B、酸的书写:
H+酸根(酸根不一定是原子团如盐酸根Cl–不是)
盐酸HCl硫酸H2SO4硝酸HNO3碳酸H2CO3亚硫酸H2SO3磷酸H3PO4
C、碱的书写:
金属元素+OH-(氨水NH3·
H2O除外)
氢氧化钠NaOH氢氧化钾KOH氢氧化钙Ca(OH)2氢氧化钡Ba(OH)2氢氧化铜Cu(OH)2
氢氧化铁Fe(OH)3氢氧化亚铁Fe(OH)2氢氧化铝Al(OH)3氢氧化镁Mg(OH)2
D、盐的书写:
金属元素或铵根+酸根
氯化钠NaCl氯化锌ZnCl2氯化钙CaCl2氯化钾KCl氯化银AgCl氯化铝AlCl3
氯化铁FeCl3氯化亚铁FeCl2氯化钡BaCl2
硫酸钠Na2SO4硫酸铜CuSO4硫酸亚铁FeSO4硫酸铁Fe2(SO4)3硫酸锌ZnSO4硫酸钡BaSO4
碳酸钠Na2CO3碳酸钙CaCO3碳酸钡BaCO3
硝酸钾KNO3硝酸钠NaNO3硝酸银AgNO3硝酸汞Hg(NO3)2
硝酸铵NH4NO3硫酸铵(NH4)2SO4氯化铵NH4Cl碳酸氢铵(碳铵)NH4HCO3
碳酸氢钠(酸式碳酸钠)NaHCO3氯酸钾KClO3高锰酸钾KMnO4锰酸钾K2MnO4
E、有机物:
甲烷CH4乙醇(酒精)C2H5OH醋酸CH3COOH尿素CO(NH2)2,
葡萄糖:
C6H12O6淀粉:
(C6H10O5)n
⑥化学式的涵义:
表示一种物质、元素组成、一个分子、一个分子的原子构成个数。
*化学式中元素符号右下角的数字表示一个分子中该原子个的数。
*化学式前系数表示分子个数。
⑦化学方程式:
必记的化学方程式:
(见专题部分)
客观事实和质量守恒定律。
写好化学式,分清反应物、生成物,条件要居中、状态要写清,系数要配平,不要忘等号。
涵义:
①表示反应中的反应物、生成物、反应条件及状态。
②表示反应中的反应物和生成物的质量比=物质的相对分子质量×
计量数之比
③表示反应中的粒子数之比=计量数之比
二、常见物质的学名、俗名及化学式
名称
俗称
化学式
名称
水银
氧化钙
生石灰
CaO
硫黄
氢氧化钙
熟石灰、消石灰
Ca(OH)2
二氧化碳
固态干冰碳酸气
CO2
氧化氢
水
H2O
氢氧化钠
苛性钠、火碱、烧碱
NaOH
过氧化氢
双氧水
H2O2
碳酸钠
纯碱、苏打
Na2CO3
碳酸氢铵
碳铵
NH4HCO3
碳酸氢钠、
酸式碳酸钠
小苏打
NaHCO3
硫酸铜晶体、
五水合硫酸铜
胆矾、蓝矾
CuSO4·
5H2O
乙醇
酒精
C2H5OH
乙酸
醋酸
CH3COOH
一些混合物的主要成分:
氢氯酸(俗称盐酸)
HCl
食盐
NaCl
双吸剂
Fe粉
天然气、沼气、坑气
CH4
煤
C元素
*碱石灰
CaO、Ca(OH)2
石灰石、大理石
CaCO3
石油
C、H元素
*煤气
CO、CH4、H2
石灰水(乳或浆)
铁锈
Fe2O3
*水煤气
CO、H2
三、常见物质的颜色和状态
1、白色固体:
MgO、P2O5、CaO、NaOH、Ca(OH)2、KClO3、KCl、Na2CO3、NaCl、无水CuSO4;
铁、镁为银白色(汞为银白色液态)
2、黑色固体:
石墨、炭粉、铁粉、CuO、MnO2、Fe3O4▲KMnO4为紫(红)黑色
3、红色固体:
Cu、Fe2O3、HgO、红磷▲硫:
淡黄色
4、溶液的颜色:
凡含Cu2+的溶液呈蓝色(如:
CuSO4溶液、CuCl2溶液等);
凡含Fe2+的溶液呈浅绿色(如:
FeSO4溶液、FeCl2溶液等);
凡含Fe3+的溶液呈黄色(如:
Fe2(SO4)3溶液、FeCl3溶液等),
其余溶液一般为无色。
(高锰酸钾溶液为紫红色)
5、①Cu(OH)2:
蓝色↓Fe(OH)3:
红褐色↓其余不溶性碱为白色沉淀(能溶于酸)
②绝大多数盐沉淀是白色的;
且CaCO3、BaCO3(能溶于酸)AgCl、BaSO4(不溶于稀HNO3)。
四、物质的溶解性:
1、气体:
溶的:
CO2、HCl、SO2、NH3等。
不溶(或不易溶):
O2、H2、CH4、CO、N2等。
2、金属氧化物:
除CaO、Na2O、K2O、BaO溶外,大多数不溶
3、酸:
大多数溶
4、碱:
除氢氧化钠、氢氧化钾、氢氧化钙、氢氧化钡和氨水溶外,其他碱不溶于水
5、盐:
含有钾、钠、硝酸根、铵根的盐都溶于水,含Cl-的盐只有AgCl不溶于水,其他都溶于水;
含SO42-的盐只有BaSO4不溶于水,其他都溶于水;
含CO32-的盐只有含K+、Na+、NH4+溶于水,其他都不溶于水。
6、沉淀物中只有AgCl和BaSO4不溶于稀硝酸,Fe(OH)3是红褐色沉淀,Cu(OH)2是蓝色沉淀,
其他沉淀是白色[包括Fe(OH)2];
有以下常见的沉淀:
Mg(OH)2、Al(OH)3、CaCO3、BaCO3等都溶于酸。
推断题中,往沉淀物加稀硝酸:
若讲沉淀不溶解,则沉淀中一定有AgCl或BaSO4;
若讲沉淀全部溶解,则沉淀中一定没有AgCl或BaSO4;
若讲沉淀部分溶解,则沉淀中一定有AgCl或BaSO4中
的一种,且还有另一种可溶于稀硝酸的沉淀。
五、1.三大还原剂:
在化学反应中得到氧的物质。
常用的还原剂有H2、CO、C等具有还原性
2.氧化剂:
在化学反应中失去氧的物质。
常用的氧化剂有O2(CO2、浓硫酸、硝酸)等具有氧化性。
3.具有可燃性的物质有:
C、H2、CO、CH4、C2H5OH、CH3OH。
4.干燥剂:
易吸收或与水反应的物质。
常用的干燥剂有固体氢氧化钠、氧化钙(但不能干燥酸性气体如CO2、SO2等)、浓硫酸(但不能干燥碱性气体如NH3等)(碱石灰、固体CaCl2、固体MgCl2、无水CuSO4)
5.具有挥发性的物质有:
盐酸、硝酸、乙醇(酒精)、醋酸、浓氨水。
6.催化剂(触媒):
一变(在化学反应里能改变其他物质的化学反应速率)二不变(而本身的质量和化学性质在化学反应前后都没有改变的物质)。
催化作用:
催化剂在化学反应里所起的作用叫催化作用。
注意:
二氧化锰只是在氯酸钾或过氧化氢分解的反应里作催化剂,在其他反应里可能不是催化剂。
六、初中化学中有毒的物质
类别
物质
中毒原因或后果
措施或其它
固
体
亚硝酸钠:
NaNO3
致癌
不食用工业盐
重金属盐
使蛋白质变性
口服大量鸡蛋清或牛奶
气
CO
与血红蛋白结合,使人因缺O2而死亡
通风,送医院输O2治疗
氮的氧化物、SO2
造成大气污染
处理后排放
液
甲醇
使人眼睛失明
不食用工业酒精
重金属盐溶液
含Cu2+、Ba2+、Hg2+、Pb2+等离子
除钡餐BaSO4外
七、初中化学敞口置于空气中质量改变的
1、质量增加的:
(1)由于吸水而增加的:
氢氧化钠固体,氯化钙,浓硫酸;
(2)由于跟水反应而增加的:
氧化钙、硫酸铜;
(3)由于跟二氧化碳反应而增加的:
氢氧化钠,氢氧化钙;
2、质量减少的:
(1)由于挥发而减少的:
浓盐酸,浓硝酸,酒精,汽油,浓氨水;
(2)由于发生分解反应而减少的:
NH4HCO3碳酸氢铵。
*露置在空气中质量减少或变质的东西应密封保存,如NaOH固体
*凡在空气中易吸水的物质,可作干燥剂,常用的有NaOH固体、CaO、无水CaCl2、浓H2SO4。
*无水CuSO4可检测物质(液体)是否含H2O。
八、有热量变化的情况
(一)物质溶于水中的热效应:
1、溶于水中放热的有:
氧化钙、氢氧化钠固体、浓硫酸
2、溶于水中吸热的有:
NH4NO3等铵盐、干冰
(二)化学反应中的热效应:
1、反应放热的有:
①所有的燃烧及氧化反
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 初三化学 用语 常见 物质 化学式
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 12处方点评管理规范实施细则_精品文档.doc
12处方点评管理规范实施细则_精品文档.doc
 17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
