 实用参考质量体系内部审核计划表Word文档格式.docx
实用参考质量体系内部审核计划表Word文档格式.docx
- 文档编号:14047920
- 上传时间:2022-10-17
- 格式:DOCX
- 页数:23
- 大小:25.98KB
实用参考质量体系内部审核计划表Word文档格式.docx
《实用参考质量体系内部审核计划表Word文档格式.docx》由会员分享,可在线阅读,更多相关《实用参考质量体系内部审核计划表Word文档格式.docx(23页珍藏版)》请在冰豆网上搜索。
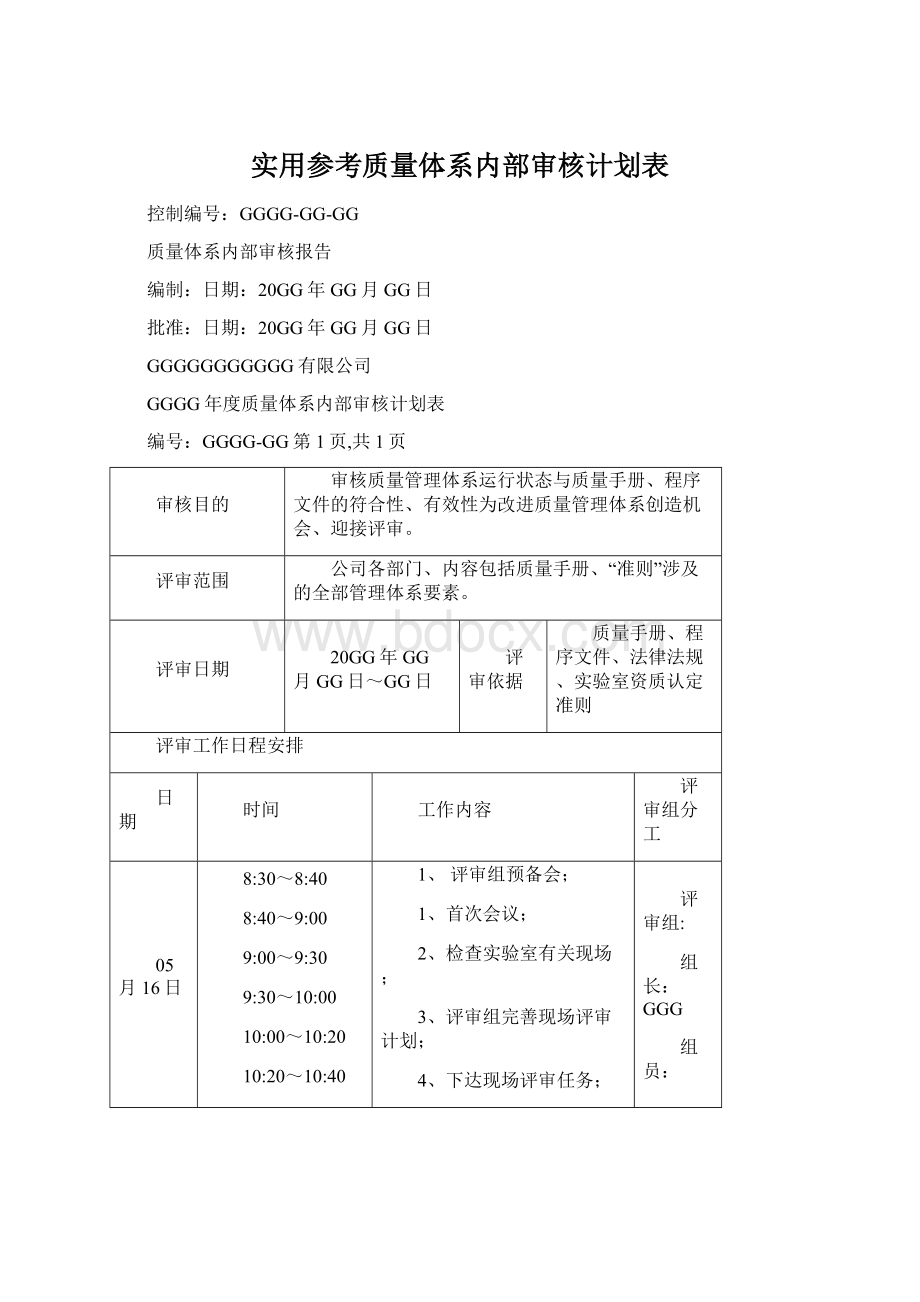
工作内容
评审组分工
05月16日
8:
30~8:
40
40~9:
00
9:
00~9:
30
30~10:
10:
00~10:
20
20~10:
1、评审组预备会;
1、首次会议;
2、检查实验室有关现场;
3、评审组完善现场评审计划;
4、下达现场评审任务;
5、软件组进行评审和审阅、硬件组进行评审和现场试验;
评审组:
组长:
GGG
组员:
GGG、GGG
GGG:
4.1、4.2、4.7、4.8、4.10
GGGG、GG:
4.3、4.5、4.6、5.1、5.7、4.11
GGG、GGG:
4.4、4.9、5.8、5.2、5.3、5.4、5.5、5.6
05月17日
30~9:
30~11:
14:
00~15:
15:
00~16:
16:
30~16:
50
17:
00~17:
1、软、硬件评审组继续进行现场评审;
2、试验人员考核;
3、按评审表评审;
4、软硬件评审组整理资料,并开碰头会;
5、现场试验和软、硬件评审工作补遗;
6、起草评审意见
7、评审组与实验室负责人交换意见
8、末次会议,宣布评审组意见,并在评审报告上签名
评审组长:
GGG20GG年GG月GG日
20GG年度内部审核工作计划
200G-G第1页共2页
一、审核目的
为验证实验室管理体系的适应性和有效性,保证实验室的管理体系运行符合《实验室资质认定评审准则》的要求,进行本次内部审核工作。
二、受审核部门
GG试验室、GG试验室、GG业务办公室
三、审核范围
涉及实验室资质认定评审准则的全部要素。
四、审核依据
(一)实验室资质认定评审准则。
(二)实验室《质量手册》、《程序文件》。
五、审核组成员
GGGGGG
六、工作时间安排
(一)20GG年GG月GG日
30----9:
00首次会议(GGG室主任及相关人员)
00----11:
00GG试验室(GGG、GGG)
11:
30---13:
00午休
13:
00---15:
30GG试验室(GGG、GGG)
30---16:
00审核组内部会议
200G-G第2页共2页
(二)20GG年10月19日
30----10:
00GGG办公室(GGG、GGG)
00---10:
30审核组内部会议
30---11:
00末次会议
内部审核组
二0GG年GG月GG日
关于进行20GG年度内部审核的通知
200G-G第1页共1页
公司各部门:
经公司质量负责人与各科室沟通后,决定于20GG年GG月GG日、GG月GG日依据实验室资质认定评审准则和公司《质量手册》、《程序文件》等要求进行20GG年度公司管理体系内部审核工作。
希望各部门接到通知后,认真做好迎接内部审核的准备工作,配合内部审核组进行审核工作。
具体工作安排见20GG年度内部审核工作计划。
内部审核组成员:
GGG办公室
质量体系内部审核签到表
第G页,共G页
会议类别
首次会议□末次会议□
序号
姓名
职务
部门
备注
内审首末次会议签到表
20GG-G
20GG年月日
质量体系内部检查表
被审核部门
GGGGG
审核日期
GGGG年G月G日
被审核部门负责人
审核员
条款号
审核内容
检查记录
标记
4.1.1
实验室是否具有独立法人资格。
实验室是独立法人,有独立帐目,独立核算。
P
4.1.2
实验室是否具备固定的工作场所,是否具备正确进行检测所需要的并且能够独立调配使用的固定、临时和可移动检测和/或校准设备设施。
实验室有固定的工作场所,
拥有独立调配使用的固定检测的设备设施。
但设备尚未检定
O
4.1.3
实验室管理体系是否覆盖其所有场所进行的工作。
实验室只有一个场所,能够全部覆盖。
4.1.4
实验室是否有与其从事检测活动相适应的专业技术人员和管理人员。
专业技术人员和管理人员数量已经达到要求。
4.1.5
实验室及其人员是否有与其从事的检测活动以及出具的数据和结果存在利益关系;
是否参与任何有损于检测判断的独立性和诚信度的活动;
是否参与和检测项目或者类似的竞争性项目有关系的产品设计、研制、生产、供应、安装、使用或者维护活动。
实验室是否有措施确保其人员不受任何来自内外部的不正当的商业、财务和其他方面的压力和影响,并防止商业贿赂
实验室及其人员没有从事与其出具的数据和结果存在利益关系的活动;
没有参与任何有损于检测判断的独立性和诚信度的活动;
没有参与检测项目或者类似竞争性项目有关系的产品设计、研制等活动。
实验室有措施保证其人员不受任何来自内外部的不正当商业、财务和其他方面的压力和影响。
审核组长
GGGG
年G月G日
标记:
P为合格,N为不合格,O为待验证.
GG年G月G日
4.1.6
实验室及其人员是否对其在检测活动中所知悉的国家秘密、商业秘密和技术秘密负有保密义务,并有相应措施。
检查发现个别检测员对保密职责掌握不好,回答不清楚,需认真学习《质量手册》中的相关条款
N
4.1.7
实验室是否明确其组织和管理结构、在母体组织中的地位,以及质量管理、技术运作和支持服务之间的关系。
实验室为独立法人机构,没有母体组织。
4.1.8
实验室最高管理者、技术管理者、质量主管及各部门主管是否有任命文件,独立法人实验室最高管理者是否由其上级单位任命;
最高管理者和技术管理者的变更是否报发证机关或其授权的部门确认。
最高管理者、技术管理者、质量主管及各部门主管都有任命文件。
4.1.9
实验室是否有规定对检测质量有影响的所有管理、操作和核查人员的职责、权力和相互关系。
必要时,指定关键管理人员的代理人。
所有管理、操作和核查人员的职责、权力和相互关系都已经明确规定。
4.1.10
实验室是否由熟悉各项检测方法、程序、目的和结果评价的人员对检测的关键环节进行监督
有质量监督员负责本条款规定的各项活动。
年月日
4.1.11
实验室是否由技术管理者全面负责技术运作,并指定一名质量主管,赋予其能够保证管理体系有效运行的职责和权力。
实验室由技术负责人全面负责技术运作,并任命了质量负责人,并授权以保证管理体系的有效运行。
4.1.12
对政府下达的指令性检验任务,是否进行编制计划并保质保量按时完成(适用于授权/验收的实验室)。
因我实验室没有指令性的检验任务,故本次内审不审核此条款。
/
4.2
实验室是否按照本准则建立和保持能够保证其公正性、独立性并与其检测活动相适应的管理体系。
管理体系是否形成文件,阐明与质量有关的政策,包括质量方针、目标和承诺,使所有相关人员理解并有效实施。
实验室已按照评审准则建立了质量管理体系,并建立了《质量手册》、《程序文件》、《作业指导书》等相关文件。
并建立了质量方针、质量目标。
4.3
实验室是否建立并保持文件编制、审核、批准、标识、发放、保管、修订和废止等的控制程序,确保文件现行有效。
实验室已经建立了文件的控制程序,确保使用的文件现行有效。
4.4
接受分包的实验室是否符合本准则的要求;
分包比例是否予以控制(限仪器设备使用频次低、价格昂贵及特种项目)。
实验室是否确保并证实分包方有能力完成分包任务。
实验室是否将分包事项以书面形式征得客户同意后方可分包。
因我实验室规模较小,没有将检测任务分包,所以此次内部审查不包括此项条款。
4.5
实验室是否建立并保持对检测质量有影响的服务和供应品的选择、购买、验收和储存等的程序,以确保服务和供应品的质量。
实验室已经建立了供应商品的选择、购买、验收和储存等相关的程序文件。
4.6
实验室是否建立并保持评审客户要求、标书和合同的程序,明确客户的要求。
实验室已建立条款中要求的相关程序文件。
4.7
实验室是否建立完善的申诉和投诉处理机制,处理相关方对其检测结论提出的异议。
是否保存所有申诉和投诉及处理结果的记录。
实验室已经建立完善的申诉和投诉处理的相关程序文件。
4.8
实验室在确认了不符合工作时,应采取纠正措施;
在确定了潜在不符合的原因时,应采取预防措施,以减少类似不符合工作发生的可能性。
实验室应通过实施纠正措施、预防措施等持续改进其管理体系。
实验室已经建立了不符合工作时的纠正措施、预防措施的相关程序文件。
4.9
实验室是否有适合自身具体情况并符合现行质量体系的记录制度。
实验室质量记录的
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 实用 参考 质量体系 内部 审核 计划
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《雷雨》中的蘩漪人物形象分析 1.docx
《雷雨》中的蘩漪人物形象分析 1.docx
