 人教版九年级中考第一次全真模拟理综化学试题Word下载.docx
人教版九年级中考第一次全真模拟理综化学试题Word下载.docx
- 文档编号:13801846
- 上传时间:2022-10-13
- 格式:DOCX
- 页数:10
- 大小:236.98KB
人教版九年级中考第一次全真模拟理综化学试题Word下载.docx
《人教版九年级中考第一次全真模拟理综化学试题Word下载.docx》由会员分享,可在线阅读,更多相关《人教版九年级中考第一次全真模拟理综化学试题Word下载.docx(10页珍藏版)》请在冰豆网上搜索。
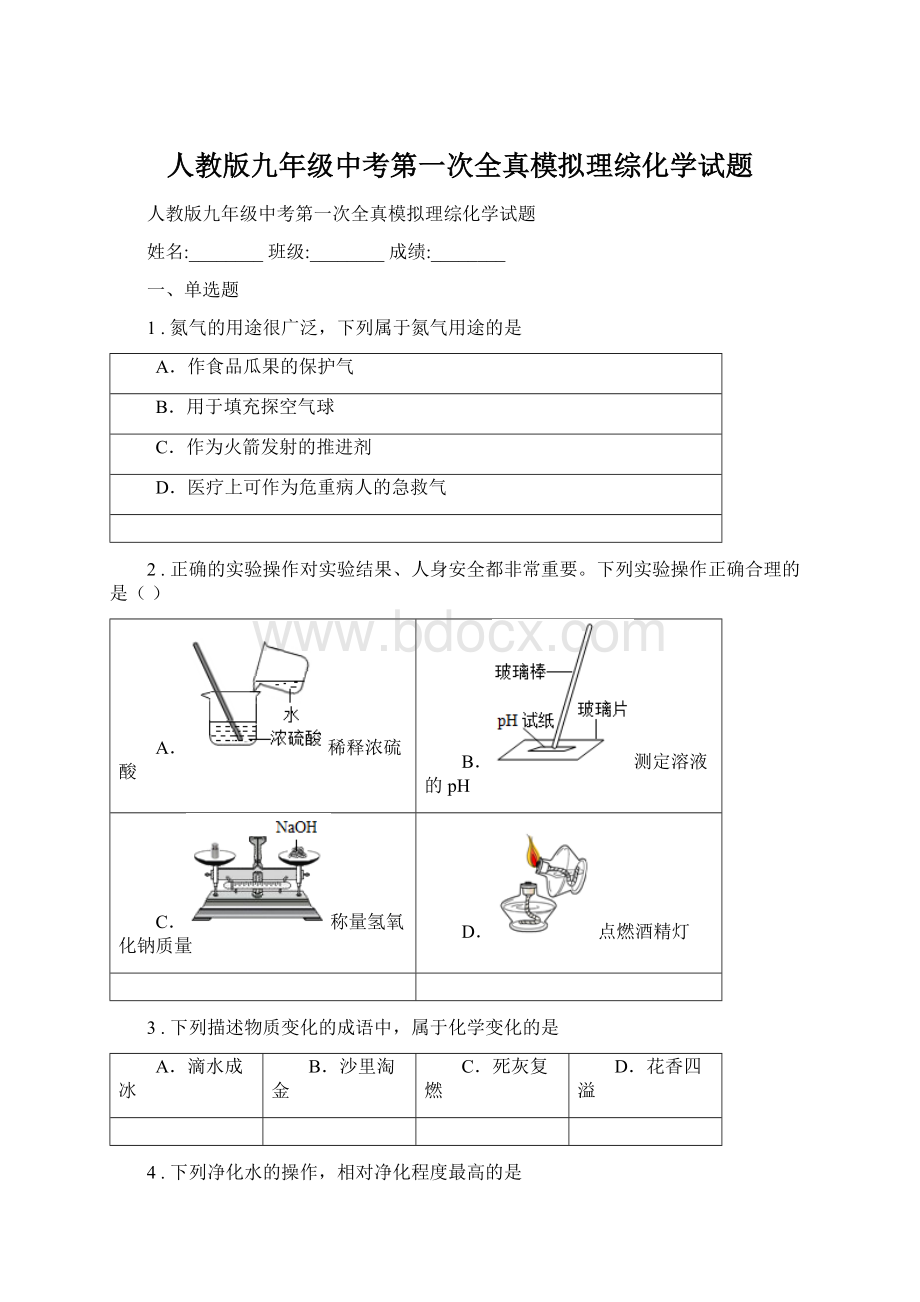
D.花香四溢
4.下列净化水的操作,相对净化程度最高的是
A.过滤
B.静置沉淀
C.蒸馏
D.吸附沉淀
5.下列各组物质能够在pH=1的溶液中大量共存,且为无色透明溶液的是:
A.KCl、NaCl、Na2CO3
B.KNO3、Ca(NO3)2、NH4Cl
C.CuSO4、H2SO4、MgCl2
D.AgNO3、NaNO3、HCl
6.下列根据实验目的所设计的实验方案中,不正确的是
A.分离CO2和CO混合气体----先通入NaOH溶液再加稀硫酸
B.区分铁粉、碳粉、氧化铜粉末----加入稀盐酸
C.除去部分变质的NaOH中的杂质----加水溶解,滴加适量的CaCl2溶液
D.除去CuSO4溶液中少量的H2SO4----加过量的氧化铜,再过滤
7.世界地球日的主题“珍惜地球资源,转换发展方式”下列做法违背该主题的是()
A.大力开采使用石化燃料
B.利用秸秆垃圾变电
C.回收利用废旧金属
D.发展太阳能等清洁能源
8.下列节约行为中合理可行的是
A.直接用工厂排出的废水灌溉农田
B.霉变的大米蒸煮后食用
C.把用剩的药品放回原试剂瓶
D.用淘米水浇花
9.下图是A、B、C三种物质的溶解度曲线,下列说法错误的是()
A.将t2℃时A、B、C的饱和溶液同时降温至t1℃后,所得溶液中溶质的质量分数由大到小的顺序是C>B>A
B.当A中含有少量B时,可以通过降温结晶的方法提纯A
C.升高温度可使接近饱和的C溶液变为饱和
D.t1℃时,A、B、C三种物质的溶解度由大到小的顺序是C>B>A
10.某同学在学习酸的化学性质后,做了甲、乙二个实验,实验结束后,把甲乙试管中的废液依次缓慢倒入同一洁净的废液缸中,下列对废液缸中废液成分的分析正确的是
A.废液中除氯化钠外,一定有氯化钙
B.如果废液呈碱性,则一定有氢氧化钙
C.如果废液呈酸性,则一定有氯化钙、氯化钠
D.废液中一定有氯化钠,还有氢氧化钙或碳酸钠或盐酸中的一种物质
11.下列有关金属和金属材料的说法不正确的是()
A.铁有良好的导热性,常用来制作炊具
B.黄铜属于合金,它的硬度比铜小
C.废旧电池中汞的回收可减少对环境的污染
D.铝表面易形成致密的氧化膜可阻止铝进一步被氧化
12.下列物质由离子构成的是
A.汞
B.硫酸铜
C.氮气
D.水
13.今年西安大街小巷的“小龙虾”很受吃货青睐。
据报道,用于清洗小龙虾的“洗虾粉”中含有柠檬酸钠和亚硫酸钠(化学式Na2SO3)等物质,可能对人体的健康产生危害。
下列有关说法正确的是()
A.Na2SO3是由Na2S和O3组成的
B.Na2SO3中钠、硫、氧元素的质量比为2:
1:
3
C.Na2SO3中硫元素的化合价为+4
D.Na2SO3是由钠、硫、氧三种原子构成的纯净物
14.下列关于实验现象的描述正确的是
A.磷在氧气中燃烧,产生大量白色烟雾
B.木炭在氧气中燃烧,发出白光,生成使澄清石灰水变浑浊的气体
C.硫粉在氧气中燃烧时,发出蓝紫色火焰,闻到刺激性气味
D.铁丝在氧气中剧烈燃烧,火星四射,生成黑色的四氧化三铁
15.下列有关碳和碳的氧化物的说法,错误的是()
A.《清明上河图》至今图案清晰可见,是因为在常温下碳单质的化学性质稳定
B.石墨变成金刚石属于物理变化
C.3克碳和7克氧气充分燃烧,生成物既有CO又有CO2
D.CO可用于冶炼金属,作气体燃料,CO2可用于人工降雨、灭火
二、填空题
16.用化学符号填写:
(要求书写规范)
氢气_____;
保持水的化学性质最小微粒是_____;
氧气分子_____;
铵根_____;
硫酸根_____;
碳酸根_____;
氢氧根_____;
硝酸根_____。
17.新型食品保鲜剂还原性铁粉被称为“双吸剂”。
(1)“双吸剂”的工作原理是利用了铁生锈的原理,铁生锈实质是铁与_____和_____等物质发生化学反应的结果,过一段时间由灰黑色变成红色,红色物质的主要成分是_____(填化学式)。
(2)若用化学方法检验使用一段时间的还原性铁粉是否完全失效,可选用_____
检验,若出现_____的现象,说明该种“双吸剂”仍可继续使用。
18.如下图所示,电子秤上的量筒中分别盛有蒸馏水、浓硫酸,放置一段时间。
(1)A中示数变小,从微粒的角度解释其原因是
。
(2)B中示数
(填“变大”“不变”或“变小”),其原因是
19.请结合如下图实验常用装置,回答有关问题.
(1)写出图中a仪器的名称:
________________。
(2)若用高锰酸钾制取氧气,应选用的发生装置是____(填装置序号),在加入药品前,应首先检查___,在正确选择的发生装置中还存在第一个缺陷,改进的方法是___,反应的化学方程式是__。
(3)若要制取二氧化碳,反应装置可选取_________。
(4)甲烷是一种密度比空气小,难溶于水的气体,实验室常用无水醋酸钠固体和碱石灰固体共热制取甲烷,应选择的发生装置是___(填装置序号),若选用E装置用于排空气法收集甲烷,甲烷应从_____(填“b”或“C”)端通入,若选用D装置用于排水法收集甲烷,瓶中先装满水,甲烷应从_______(填“左”或“右”)端通入。
20..工业上常利用石灰石、水、纯碱为原料来制备烧碱,请你写出相关的化学方程式。
(1)_____;
(2)_____;
(3)_____。
三、推断题
21.已知A、B为两种黑色粉末,D为红色单质。
A、B、C、D、E、F五种物质之间的转化关系如图所示。
(部分生成物已省略)。
请回答
(1)A为_____(填化学式,下同),B为_____,C为_____,D为_____,F与B发生反应的化学方程式为_____。
(2)在上述反应中A、F都具有_____性。
(3)将两只用于医学研究的小白鼠分别放入盛放C、F的两个瓶中,拧紧瓶盖,结果两只小白鼠很快都死了。
造成小白鼠死亡的主要原因_____(填“相同”或“不同”)。
四、流程题
22.某工厂的工业废水中含有大量的FeSO4以及一定量的CuSO4和Na2SO4。
为减少污染并将其变废为宝,某学习小组设计以下流程,拟从该废水中回收硫酸亚铁、金属铜,并利用氨碱法原理“制碱”。
(除标注外,其余所加药品或试剂均过量,部分产物及反应条件略去)请根据图示回答下列问题:
(1)由步骤①可知的金属活动性Fe比Cu___(选填“强”或“弱”)。
在步骤①中向废水中加入过量的铁粉,过量的目的是______________。
(2)若向步骤②所得滤液a中滴加几滴紫色石蕊试液,溶液呈____色。
(3)步骤⑤中加入Na2CO3溶液的作用是___________________。
(4)“NaCl+CO2+NH3+H2O=NaHCO3+NH4Cl”是氨碱法制纯碱中重要的反应。
①将氨气通入饱和食盐水中,可制成饱和氨盐水(氨气极易溶于水)。
氨盐水比食盐水更容易吸收二氧化碳的原因是:
_________________。
②氨盐水吸收二氧化碳生成碳酸氢钠和氯化铵两种物质,更易析出的是NaHCO3,原因是_____________。
五、科学探究题
23.化学研究小组在开展了“过氧化氢制取氧气的反应中二氧化锰的作用”之后,又进行了“寻找新的催化剂”的探究实验。
(提出问题1)寻找“氧化铁能否用于过氧化氢溶液分解的催化剂”的证据?
如果能,它的催化效果如何?
(实验设计1)
实
验
现
象
Ⅰ、分别量取5毫升5%的过氧化氢溶液于A、B两支试管中,向A中加入a克氧化铁粉末,并分别在A、B两支试管中伸入带火星的木条,观察现象,
A试管中产生气泡,带火星的木条复燃,B试管中无明显现象
Ⅱ、将“实验Ⅰ”中A试管的剩余物质分离,将所得固体进行洗涤、干燥、称量
所得固体质量为______
克
Ⅲ、将“实验Ⅱ”______
______
Ⅳ、分别量取5毫升5%的过氧化氢溶液放入C、D两支试管中,向C试管中加入a克氧化铁粉末,向D试管中加入a克二氧化锰粉末
(实验结论)
(1)A中产生的气体是______;
(2)氧化铁可以作过氧化氢分解的催化剂,寻找该结论的证据主要是设计了实验______(选填Ⅰ、Ⅱ、Ⅲ或Ⅳ)展开的。
(实验评价)
(1)设计实验Ⅲ的目的是______;
(2)可以用下列方法作出判断,从而达到实验Ⅳ的设计目的。
a、定性判断:
观察C、D两支试管中产生气泡的快慢;
b、定量判断:
______。
(资料信息)过氧化氢分解除了用二氧化锰还可用氧化铜等物质作为催化剂
(提出问题2)氧化铜(黑色粉末)是否也能作氯酸钾分解的催化剂?
它是否比二氧化锰效果更好?
(设计实验2)某同学以生成等体积的氧气为标准,设计了下列三组实验
(其它可能影响实验的因素均忽略)。
实验序号
氯酸钾质量
其他物质质量
待测数据
①
1.2克
X
②
氧化铜0.5克
Y
③
m
二氧化锰0.5克
Z
(1)写出氯酸钾在二氧化锰的催化作用下发生的反应的化学方程式:
(2)上述实验应测量的“待测数据”是指______,从数学描述角度,X、Y、Z在数值上的大小关系是______。
(3)若实验②比实验①的“待测数据”更______(填“大”、“小”、“不确定”),说明氧化铜能加快氧酸钾的分解速率,表中“m”的数值应该为______。
(4)将实验②反应后的固体经过过滤、洗涤、干燥处理后,称量得到0.5克黑色粉末,再将黑色粉末放入______(简述操作)。
(评价设计)
(5)你认为该小组同学设计实验③和实验②对比的目的是______。
六、计算题
24.有一含有纯碱的食盐样品,为了测定其中碳酸钠的含量,某同学称取10g的样品放入烧杯中,向烧杯中加入100g足量的稀盐酸,充分反应后气体全部逸出,烧杯中剩余物的总质量为109.56g(假设产生的气体全部逸出。
以下计算结果保留一位小数)
(1)样品中碳酸钠的含量是___
(2)NaCl中氯元素质量分数是____
(3)反应后溶液中溶质质量分数是___?
参考答案
1、
2、
3、
4、
5、
6、
7、
8、
9、
10、
11、
12、
13、
14、
15、
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 人教版 九年级 中考 第一次 模拟 化学试题
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 转基因粮食的危害资料摘编Word下载.docx
转基因粮食的危害资料摘编Word下载.docx
