 氧气的教学设计和流程图知识讲解Word文档格式.docx
氧气的教学设计和流程图知识讲解Word文档格式.docx
- 文档编号:13769056
- 上传时间:2022-10-13
- 格式:DOCX
- 页数:13
- 大小:103.70KB
氧气的教学设计和流程图知识讲解Word文档格式.docx
《氧气的教学设计和流程图知识讲解Word文档格式.docx》由会员分享,可在线阅读,更多相关《氧气的教学设计和流程图知识讲解Word文档格式.docx(13页珍藏版)》请在冰豆网上搜索。
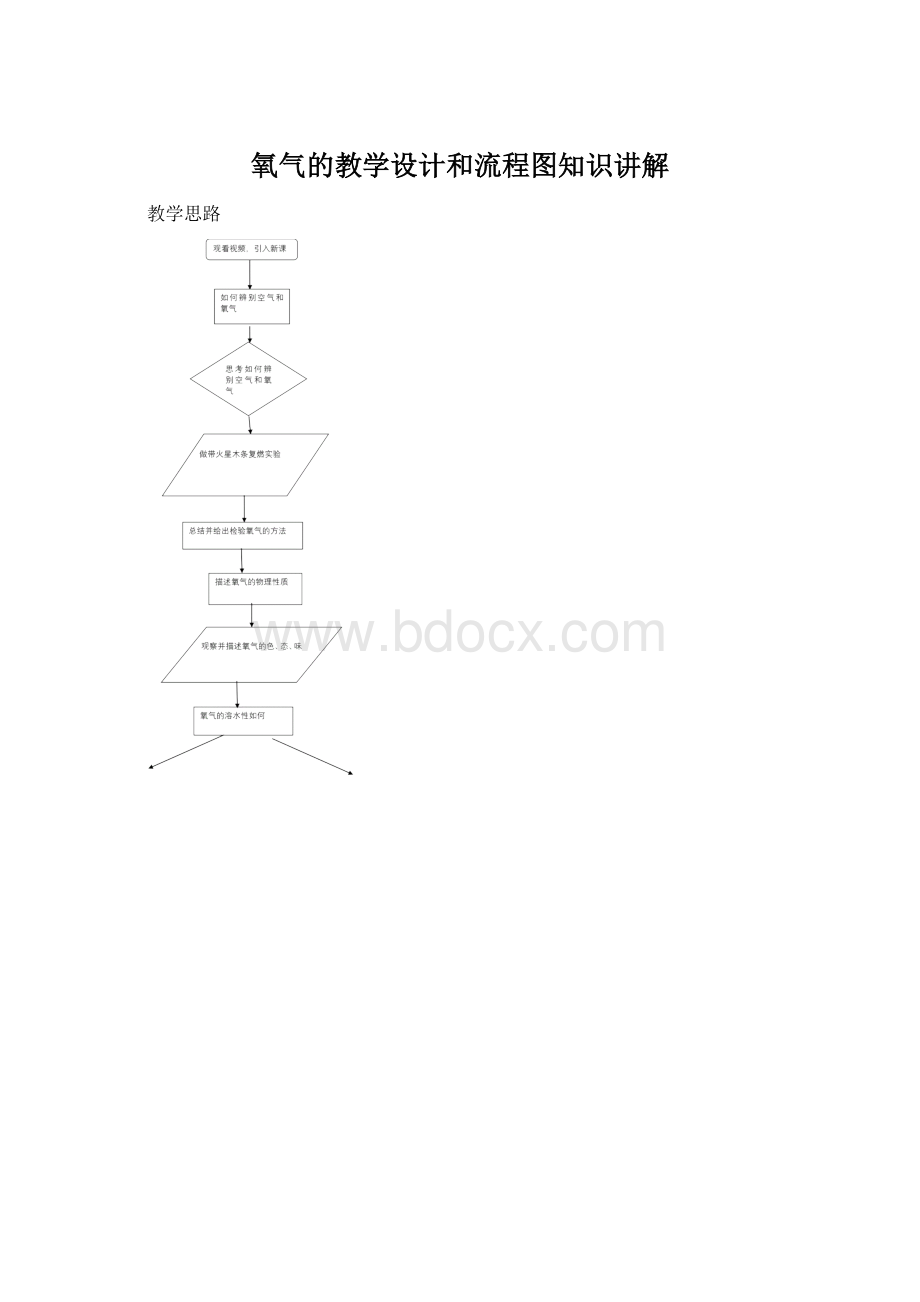
教学过程
1、初识氧气
观看影片,引入课题
教师活动
学生活动
教学意图
先播放有关氧气的影片。
提问:
看了这段影片,大家联想到什么物质?
讲述:
影片介绍的是有关氧气用途,我们知道氧气的用途是由其性质决定的,这节课我们就来研究氧气的性质。
[板书]课题2氧气
纷纷带着好奇心观看
思考并回答:
氧气。
引导学生从熟悉的生活走进课堂,激发学生的学习兴趣。
2、检验氧气
通过实验检验氧气
上节课我们学习了空气,我们知道氧气是空气组成成分之一,现在你们的桌上放有两个分别装有氧气和空气的未贴标签的集气瓶,你们能分辨出哪一瓶是氧气吗?
不能直观的看出哪一瓶是氧气,我们来做个实验,大家分别用一根带火星的木条伸入集气瓶,看看有什么实验现象
现在知道哪瓶是氧气了吗?
在刚才的实验中,氧气可使带火星木条复燃,但它在空气中则会熄灭,而将在空气中正在燃烧的木条插在氧气瓶中又会怎么样呢?
下面你们就用燃着的木条来检验氧气。
[板书]实验方案:
1.用两支带火星木条分别插入两瓶中;
2.用两支燃着木条分别插入两瓶中。
现象:
1.其中一瓶气体使带火星的木条复燃,另一瓶熄灭;
2.两个集气瓶相比,燃着的木条在使带火星木条复燃的那瓶气体中燃烧更旺
结论:
1.氧气可使带火星木条复燃;
2.木条燃烧越旺,说明氧气越多。
我们就用这瓶氧气来研究它的性质;
首先我们来研究它的物理性质。
思考并认识到不能简单的通过用眼睛看或鼻子闻来辨别
实验,并观察到有一个集气瓶内的气体使带火星的木条复燃
使带火星的木条复燃的那瓶是氧气
实验并得出结论:
使带火星木条复燃的是氧气或使木条燃烧更旺的是氧气。
让学生学会如何检验氧气,并通过实验激起学生对氧气性质探究的兴趣
3、探究氧气的物理性质
1.直接观察色、态、味
2.通过实验探究氧气的溶水性
物理性质包括哪些方面呢?
这些都是不经过化学变化而表现出来的性质。
现在你们桌上的集气瓶内装的就是氧气,一起先来描述氧气的色、态、味。
[板书]一、氧气的性质
1.物理性质(通常状态下)
颜色(无色)、状态(气体)、气味(无味)、密度(1.429g/L)、熔点(-218℃)、沸点(-183℃)、溶水性(?
)
[多媒体]展示氧气的三态图及氧气瓶
提问:
氧气能不能溶于水?
肯定:
能,并加以分析,然后设问:
这样描述你们是不是觉得范围太大,不太确切?
我们可不可以用是否易溶于水来描述它?
[板书]探究程序
1.氧气是否易溶于水?
(提出问题)
2.氧气不易溶于水?
氧气易溶于水(作出假设)
3.将大量水倒入氧气瓶中并振荡,用带火星木条插入瓶中,看是否复燃。
(设计方案,进行探究)
4.复燃──不易溶;
不复燃──易溶(得出结论)
演示实验,并提醒学生注意观察、分析以得出结论。
[板书]氧气不易溶于水
补充说明:
氧气不易溶于水,但不是绝对不溶于水,在室温下,1L水中只能溶解30mL氧气,这对水中动物生存有着重要意义
回忆并回答:
色、态、味、密度、熔、沸点和溶水性
描述:
无色、无味的气体。
观看并对氧气物理性质有一定的感性认识。
学生各抒己见:
能,因为鱼儿要生存需要氧气。
学生思考并认同
学生初步掌握科学的实验探究步骤。
学生通过对实验的观察得出结果:
现象:
复燃
结论:
氧气不易溶于水。
引导学生研究物质从物理性质入手,从简单开始,让学生逐步形成认识物质的方法;
培养学生树立科学研究的严谨态度。
使学生加深对实验探究的意识,熟悉探究程序,使学生养成从实验到分析再到结论的习惯。
4、氧气的化学性质
1.探究硫在空气和氧气中的燃烧
2.探究铝箔加热后在氧气中的燃烧
3.总结氧气的化学性质
刚刚我们学习的是氧气的物理性质,现在我们来探究氧气的化学性质。
我们知道氧气能支持燃烧,那除了小木条能不能支持其他的物质燃烧?
[板书]实验:
硫加热后在空气中、纯氧中反应的现象。
现在我来演示这个实验,大家注意看实验步骤和实验现象,之后我会让同学来描述实验现象的。
演示实验
提问学生观察到的实验现象
肯定并讲解:
硫燃烧生成的气体叫做二氧化硫(化学式为SO2),它是污染空气的主要气体之一,烟花爆竹里面的主要成分就有硫,燃放时就会产生二氧化硫,我们每次闻到的那种刺激性气味就是二氧化硫。
[板书]现象:
硫在空气中燃烧发出微弱的淡兰色火焰,在纯氧中发生明亮蓝紫色火焰,同时生成一种有剌激气味气体,放出热量。
讲述:
前面我们学了文字表达式表达磷在空气中燃烧生成五氧化二磷,我们同样可写出硫燃烧的文字表达式。
[板书]反应物是硫、氧气,生成的是二氧化硫,文字表达式:
硫+氧气点燃二氧化硫,左边是反应物,右边是生成物,中间用箭头连接,并注意条件是点燃。
[板书]为什么木条、硫分别在空气里和氧气里燃烧的现象不同?
它说明了什么?
(提示:
可从氧气含量去分析)
[板书]物质在空气中燃烧,实际上是物质与空气中氧气反应,由于空气中氧气含量较少,所以在空气中燃烧不如在氧气中剧烈。
1.它说明了氧气含量越高,燃烧越剧烈。
2.也说明了氮气不支持燃烧。
刚刚我们做了硫在空气和氧气中的实验,接下来我们来看一个视频,有关铝箔加热后在空气和氧气中燃烧的实验现象。
观看铝箔加热后在空气和氧气中燃烧的视频
看了视频,我们知道铝箔能不能在空气中燃烧?
铝箔在氧气中燃烧的实验现象又是什么呢?
[板书]铝加热后在空气中、氧气中现象
[板书]实验具体内容及步骤
铝燃烧生成的物质叫氧化铝(化学式为Al2O3)
[板书]铝在空气中不能燃烧,在氧气中剧烈燃烧,发出耀眼白光,放出大量的热,反应生成一种固体物质。
一起说说反应前、后物质及反应的文字表达式?
为什么要放一些细沙呢?
肯定并总结:
为了防止燃烧过程中溅落下来的溶渣把集气瓶炸裂。
为什么硫燃烧不需要铺细沙呢?
通过带火星木条、硫、铝在氧气中反应,我们可总结出氧气有哪些性质呢?
总结并写板书
[板书]氧气是一种化学性质较活泼的气体,它可支持燃烧,氧气含量越高,燃烧越剧烈。
请同学们说说你所知道的氧气支持燃烧的例子。
过渡:
氧气的性质决定用途,用途体现氧气的性质,再次播放有关氧气用途的影片
这里面的氧气用途有两种:
供呼吸及支持燃烧,那哪些是利用了它的支持燃烧的性质呢?
学生被激起探究欲望。
学生认真观看实验,并初步掌握实验的步骤
学生积极描述看到的实验现象
学生在老师的提示下,一起叙述反应物、生成物及硫燃烧反应的文字表达式。
认真思考,可能的回答:
空气中氧气含量低,氧气支持物质燃烧,氮气不支持燃烧
观看视频
不能
思考并回忆刚刚所看视频,积极描述看到的实验现像
然后一起回答,教师打出电子板书]反应前物质:
铝、氧气反应后的物质:
氧化铝,文字表达式:
铝+氧气点燃二氧化铝
思考,各抒己见。
回答:
生成的二氧化硫是气体
学生间相互讨论,并得出可能的结果。
讨论并积极发言。
讨论,回答:
航天航空、气焊、气割等。
通过实例让学生初步掌握观察实验的程序,并掌握实验探究的方法步骤。
通过观看视频,思考问题让学生从感性认识上升到理性思考,培养学生对实验的观察和描述做到系统、全面和深入。
让学生慢慢的学会归纳总结
5、提出化学反应的概念
1.提出化学反应的概念
2.总结规律得出化合反应的概念
我们刚刚学习了氧气的化学性质,还做了氧气与硫、铝箔的燃烧实验,那同学们能说说硫和铝箔在反应前后有什么变化,它们的燃烧和水变成了水蒸气有什么区别?
总结:
硫、铝的变化都生成了新物质,而水蒸发只是状态发生变化。
那么我们把生成新物质的变化叫化学变化。
没有新物质生成的变化叫物理变化。
[板书]二、化学反应
1、化学变化:
都生成了新物质的变化就叫做化学变化,也叫化学反应。
它的基本特征是生成新物质。
2、2、物理变化:
没有生成新物质的变化就叫做物理变化
根据化学变化概念,大家能举出生活中你身边所发生的化学变化吗?
比一比,看谁举得多?
化学变化的基本特征是生成新物质,它不仅有大小、状态上的变化而且常表现有一些现象,像颜色变化、生成气体、发光放热等。
是不是有现象就一定是化学变化呢?
你能举例说明吗?
小结:
现象只能帮助我们判断有无化学变化,有现象不一定就是化学变化,象灯泡发光放热,氧气变液氧、无色变淡蓝色,但他们都是物理变化。
讲解:
物理变化只是大小、形状、状态发生变化,例如:
粉笔变粉笔灰、水蒸发等。
化学变化与物理变化的本质区别是什么呢?
物理变化与化学变化的判断应根据是否有新物质生成,现象不能作为判断的依据。
[板书]3.化学性质:
需要通过化学变化而表现出来的性质。
我们今天学习的几个化学反应,通过其文字表达式,能发现它们有什么规律吗?
[板书]4.化合反应:
由两种或两种以上的物质反应,只生成一种物质的化学反应叫做化合反应。
作业:
......
讨论并回答:
硫、铝在氧气中燃烧前后物质发生了变发。
讨论并踊跃回答:
燃放鞭炮、钢铁生锈、木炭燃烧等。
通过思考得出区别:
有无新物质生成
通过思考观察得出:
它们都是由两种物质反应,只生成了一种物质
通过对实验信息的收集及分析得出化学反应这个概念,培养学生收集、分析加工信息的能力;
通过举例使学生把知识与生活联系起来,并激发学生学习兴趣。
学会观察,找规律,归纳总结
板书设计
课题2氧气
一、氧气的性质
1.氧气的物理性质(通常状况下)
颜色状态气味密度熔点沸点溶水性(是否易溶于水)
无色气体无味1.429g/L-218℃-183℃不易溶于水
>空气1.293g/L
2.氧气的化学性质
氧气化学性质比较活泼,能支持燃烧,氧气含量越高,燃烧越剧烈
二、化学变化
1.生成新物质的变化就叫做化学变化,也叫做化学反应。
其基本特征是生成新物质,它常表现为颜色改变、生成沉淀、产生气体及发光、放热等能量变化。
2.物理变化:
没有生成新物质的变化就叫做物理变化。
3.化学性质:
物质在化学反应中表现出来的性质叫化学性质。
4.化合反应:
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 氧气 教学 设计 流程图 知识 讲解
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《雷雨》中的蘩漪人物形象分析 1.docx
《雷雨》中的蘩漪人物形象分析 1.docx
