 完整word高考化学工艺流程图题型分类docxWord格式文档下载.docx
完整word高考化学工艺流程图题型分类docxWord格式文档下载.docx
- 文档编号:13755097
- 上传时间:2022-10-13
- 格式:DOCX
- 页数:35
- 大小:41.44KB
完整word高考化学工艺流程图题型分类docxWord格式文档下载.docx
《完整word高考化学工艺流程图题型分类docxWord格式文档下载.docx》由会员分享,可在线阅读,更多相关《完整word高考化学工艺流程图题型分类docxWord格式文档下载.docx(35页珍藏版)》请在冰豆网上搜索。
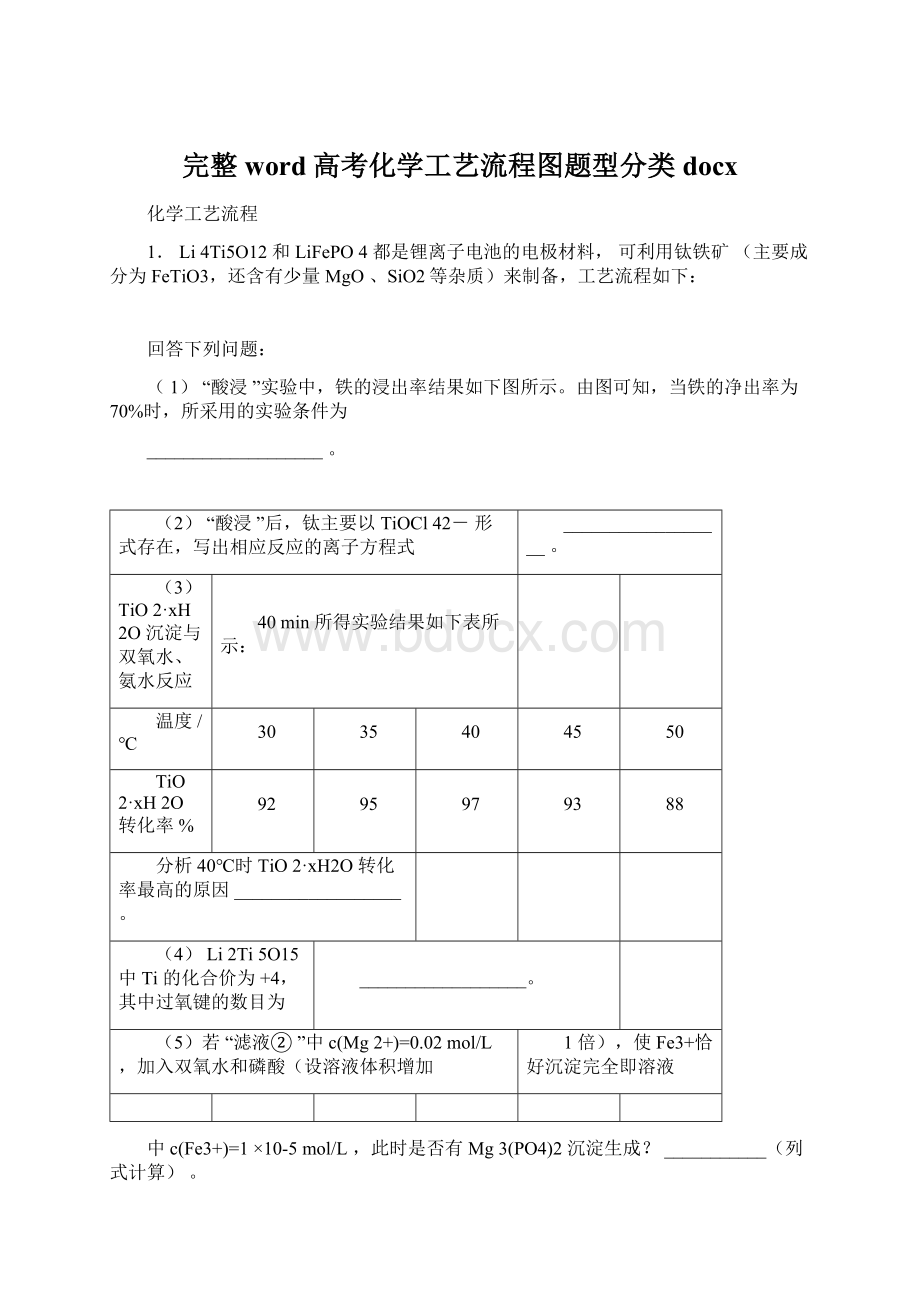
93
88
分析40℃时TiO2·
xH2O转化率最高的原因__________________。
(4)Li2Ti5O15中Ti的化合价为+4,其中过氧键的数目为
__________________。
(5)若“滤液②”中c(Mg2+)=0.02mol/L,加入双氧水和磷酸(设溶液体积增加
1倍),使Fe3+恰好沉淀完全即溶液
中c(Fe3+)=1×
10-5mol/L,此时是否有Mg3(PO4)2沉淀生成?
___________(列式计算)。
FePO4、Mg3(PO4)2的Ksp分别为1.3×
10-22、1.0×
10-24。
(6)写出“高温煅烧②”中由FePO4制备LiFePO4的化学方程式
。
【答案】
(1)100℃、2h,90℃,5h
(2)FeTiO3+4H++4Cl-=Fe2++TiOCl4
2-+2H2O
(3)低于40℃,TiO2·
xH2O转化反应速率随温度升高而增加;
超过
40℃,双氧水分解与氨气逸出导致TiO2·
xH2O
转化反应速率下降
(4)4
(5)Fe3+恰好沉淀完全时,c(PO43-)=1.310
1.010
22
5mol·
L-1=1.3×
10-17mol·
L-1,c3(Mg2+)×
c2(PO43-)=
(0.01)3×
(1.3×
10-17)2=1.7×
10-40<Ksp[Mg3(PO4)2],因此不会生成Mg3(PO4)2沉淀。
高温
(6)2FePO4+Li2CO3+H2C2O42LiFePO4+H2O↑+3CO2↑
2.水泥是重要的建筑材料。
水泥熟料的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。
实
验室测定水泥样品中钙含量的过程如图所示:
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸。
加入硝酸的目的是__________,
还可使用___________代替硝酸。
(2)沉淀A的主要成分是_________,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为
____________________________________。
(3)加氨水过程中加热的目的是___________。
沉淀B的主要成分为_____________、____________(填化学式)。
(4)草酸钙沉淀经稀H2SO4处理后,用KMnO4标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反
应为:
MnO
+
2
4
2+
-1的KMnO
O。
实验中称取0.400g水泥样品,滴定时消耗了
0.0500molL·
4+H+HCO→Mn
+CO+H
溶液36.00mL,则该水泥样品中钙的质量分数为
______________。
(1)将样品中可能存在的
Fe2+氧化为Fe3+;
双氧水(H2O2)
(2)SiO2
(或H2SiO3);
SiO2+4HF
SiF4↑+2HO
(3)防止胶体生成,易沉淀分离;
Fe(OH)3、
(OH)3
(4)45.0%
3.重铬酸钾是一种重要的化工原料,一般由铬铁矿制备,铬铁矿的主要成分为FeO·
Cr2O3,还含有硅、铝等杂质。
制备流程如图所示:
(1)步骤①的主要反应为:
232
3
+NaNO
+NaNO
FeO·
CrO+Na
CO
NaCrO
+FeO+CO
上述反应配平后FeO·
Cr2O3与NaNO3
的系数比为__________。
该步骤不能使用陶瓷容器,原因是
________________。
(2)滤渣1中含量最多的金属元素是____________,滤渣2的主要成分是____________及含硅杂质。
(3)步骤④调滤液2的pH使之变____________________(填“大”或“小”),原因是_________(用离子方程式表示)。
(4)有关物质的溶解度如图所示。
向
“滤液3”中加入适量KCl,蒸发浓缩,冷却结晶,过滤得到
K2Cr2O7固体。
冷却到___________________(填标号)得到的K2Cr2O7固体产品最多。
a.80℃
b.60℃
c.40℃
d.10℃
步骤⑤的反应类型是
(5)某工厂用
m1kg
铬铁矿粉(含
Cr2O340%)制备
K2Cr2O7,最终得到产品
m2kg,产率为
_____________。
(1)2:
7
陶瓷在高温下会与
Na2CO3反应
(2)铁Al(OH)3
(3)小
增大溶液中
H
+,促进平衡2CrO
42-
+2H
272-
O正向移动
CrO
+H
(4)d
复分解反应
(5)
190m2
100%
147m1
4.高锰酸钾(KMnO)是一种常用氧化剂,主要用于化工、防腐及制药工业等。
以软锰矿(主要成分为
)为
原料生产高锰酸钾的工艺路线如下:
(1)原料软锰矿与氢氧化钾按
1∶1的比例在“烘炒锅”中混配,混配前应将软锰矿粉碎,其作用
是
(2)“平炉”中发生的化学方程式为
(3)“平炉”中需要加压,其目的是
(4)将K2MnO4转化为KMnO4的生产有两种工艺。
①
CO2歧化法”是传统工艺,即在
KMnO
溶液中通入CO
气体,使体系呈中性或弱酸性,
K
发生歧化反
“
应,反应中生成K2MnO4、MnO2
和
(写化学式)。
②
“电解法”为现代工艺,即电解
K2MnO4
水溶液,电解槽中阳极发生的电极反应为
,
阴极逸出的气体是
③“电解法”和“CO
歧化法”中,K2MnO4的理论利用率之比为
(5)高锰酸钾纯度的测定:
称取
1.0800g样品,溶解后定容于
100mL容量瓶中,摇匀。
取浓度为
-1
平均消耗的体积为
0.2000molL·
的H2C2O4标准溶液20.00mL,加入稀硫酸酸化,用KMnO4溶液平行滴定三次,
24.48mL,该样品的纯度为
(列出计算式即可,已知
2MnO
4-
224
+10CO
+5HCO+6H=2Mn
↑+8HO)。
(1)增大反应物接触面积,加快反应速率,提高原料利用率;
(2)2MnO2+4KOH+O2
2K2MnO4+2H2O;
(3)提高氧气的压强,加快反应速率,增加软锰矿转化率;
(4)①KHCO3;
②MnO42--e-=MnO4-;
H2;
③3:
2;
20.0010-30.20002
100
158
5
24.48
100%。
1.0800
5.过氧化钙微溶于水,溶于酸,可作分析试剂、医用防腐剂、消毒剂。
以下是一种制备过氧化钙的实验方法。
(一)碳酸钙的制备
(1)步骤①加入氨水的目的是_______。
小火煮沸的作用是使沉淀颗粒长大,有利于____。
(2)右图是某学生的过滤操作示意图,其操作不规范的是______(填标号)。
a.漏斗末端颈尖未紧靠烧杯壁b.玻璃棒用作引流c.将滤纸湿润,使其紧贴漏斗壁d.滤纸边缘高出漏斗e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(二)过氧化钙的制备
(3)步骤②的具体操作为逐滴加入稀盐酸,至溶液中尚存有少量固体,此时溶液呈____性(填“酸”、“碱”或“中”)。
将溶液煮沸,趁热过滤。
将溶液煮沸的作用是___________。
(4)步骤③中反应的化学方程式为
________,该反应需要在冰浴下进行,原因是
_________。
(5)将过滤得到的白色结晶依次使用蒸馏水、乙醇洗涤,使用乙醇洗涤的目的是
_______。
(6)制备过氧化钙的另一种方法是:
将石灰石煅烧后,直接加入双氧水反应,过滤后可得到过氧化钙产品。
该工艺方法的优点是______,产品的缺点是_______。
(1)调节溶液pH使Fe(OH)3沉淀;
过滤分离;
(2)ade;
(3)酸;
除去溶液中溶解的CO2;
(4)CaCl2+2NH3·
H2
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 完整 word 高考 化学 工艺 流程图 题型 分类 docx
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 转基因粮食的危害资料摘编Word下载.docx
转基因粮食的危害资料摘编Word下载.docx
