 卓顶精文最新初中化学重要考点汇编化学用语docWord文档格式.docx
卓顶精文最新初中化学重要考点汇编化学用语docWord文档格式.docx
- 文档编号:13728219
- 上传时间:2022-10-13
- 格式:DOCX
- 页数:38
- 大小:347.32KB
卓顶精文最新初中化学重要考点汇编化学用语docWord文档格式.docx
《卓顶精文最新初中化学重要考点汇编化学用语docWord文档格式.docx》由会员分享,可在线阅读,更多相关《卓顶精文最新初中化学重要考点汇编化学用语docWord文档格式.docx(38页珍藏版)》请在冰豆网上搜索。
Mn
Ba
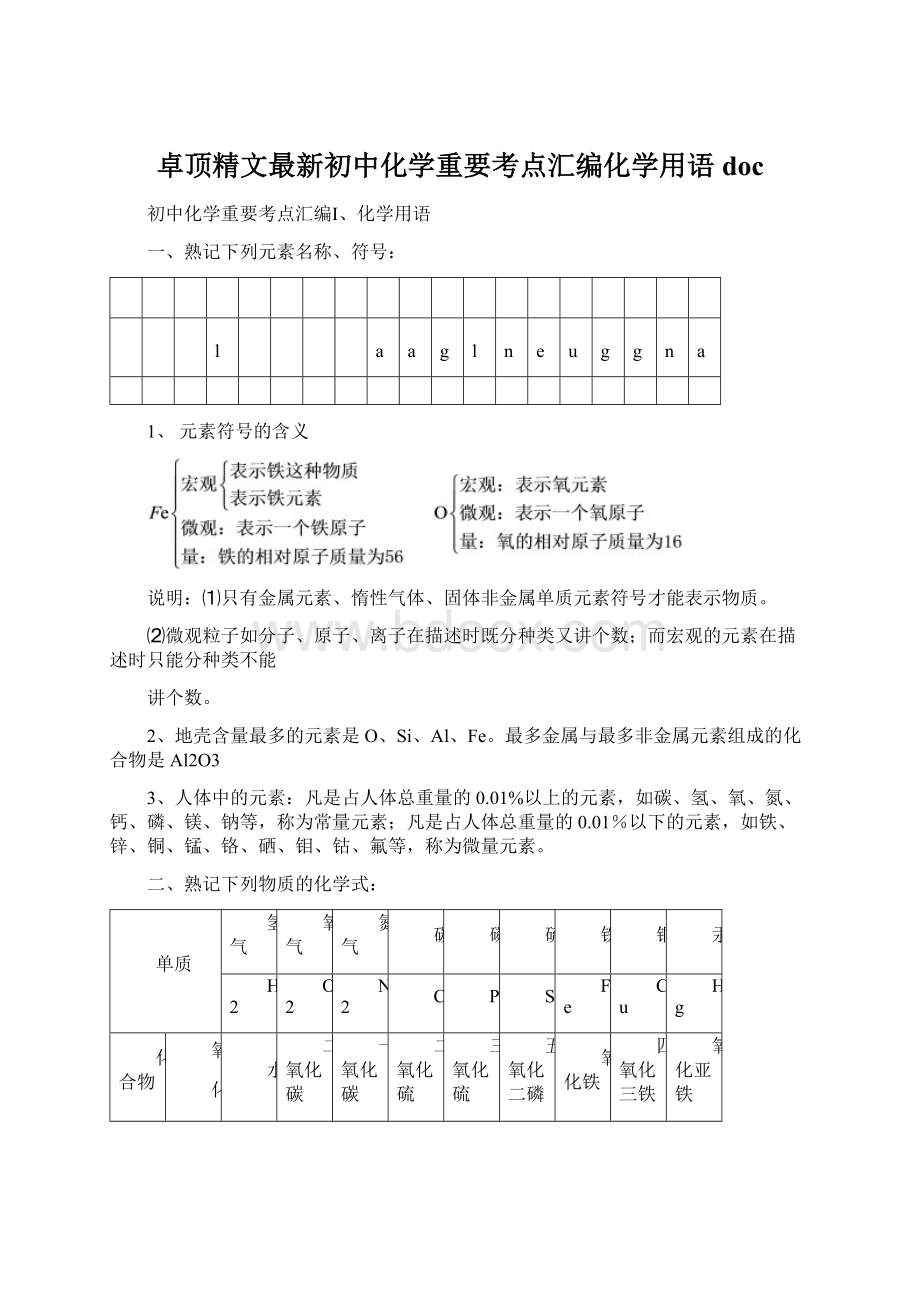
1、元素符号的含义
说明:
⑴只有金属元素、惰性气体、固体非金属单质元素符号才能表示物质。
⑵微观粒子如分子、原子、离子在描述时既分种类又讲个数;
而宏观的元素在描述时只能分种类不能
讲个数。
2、地壳含量最多的元素是O、Si、Al、Fe。
最多金属与最多非金属元素组成的化合物是Al2O3
3、人体中的元素:
凡是占人体总重量的0.01%以上的元素,如碳、氢、氧、氮、钙、磷、镁、钠等,称为常量元素;
凡是占人体总重量的0.01%以下的元素,如铁、锌、铜、锰、铬、硒、钼、钴、氟等,称为微量元素。
二、熟记下列物质的化学式:
单质
氢气
氧气
氮气
H2
O2
N2
化合物
化
物
水
二氧化碳
一氧化碳
二氧化硫
三氧化硫
五氧化二磷
氧化铁
四氧化三铁
氧化亚铁
H2O
CO2
CO
SO2
SO3
P2O5
Fe2O3
Fe3O4
FeO
氧化镁
氧化铜
氧化锌
二氧化锰
氧化钠
氧化钙
MgO
CuO
ZnO
MnO2
Na2O
CaO
酸
盐酸
硫酸
硝酸
磷酸
碳酸
亚硫酸
HCl
H2SO4
HNO3
H3PO4
H2CO3
H2SO3
碱
氢氧化钠
氢氧化钾
氢氧化钙
氢氧化钡
氢氧化铜
氢氧化铁
氢氧化镁
氢氧化亚铁
氢氧化铝
NaOH
KOH
Ca(OH)2
Ba(OH)2
Cu(OH)2
Fe(OH)3
Mg(OH)2
Fe(OH)2
Al(OH)3
盐
氯化钠
碳酸钠
氯化锌
氯化钙
氯化钾
硫酸钠
硫酸铜
氯化银
氯化铁
NaCl
Na2CO3
ZnCl2
CaCl2
KCl
Na2SO4
CuSO4
AgCl
FeCl3
氯化亚铁
氯化铝
硫酸亚铁
硫酸铁
硫酸锌
碳酸钙
氯化钡
硫酸钡
氯酸钾
FeCl2
AlCl3
FeSO4
Fe2(SO4)3
ZnSO4
CaCO3
BaCl2
BaSO4
KClO3
高锰酸钾
锰酸钾
硝酸铜
硝酸汞
氯化铵
硝酸铵
硫酸铵
碳酸氢铵
碳酸氢钠
KMnO4
K2MnO4
Cu(NO3)2
Hg(NO3)2
NH4Cl
NH4NO3
(NH4)2SO4
NH4HCO3
NaHCO3
有机物
甲烷
乙醇
葡萄糖
CH4
C2H5OH
C6H12O6
1、化学式的含义:
2、化学符号的含义:
数字位置
含义
举例
元素符号前
表示原子个数
2H表示2个氢原子
化学式前
表示分子的个数
2CO表示2个一氧化碳分子
离子符号前
表示离子的个数
2Na+表示2个钠离子
元素符号左上方
表示原子的质量
2H表示这种氢原子的质量数是2
元素符号正上方
表示元素(或原子团)化合价的数目
表示硫酸锌元素为+2价,硫酸根为-2价。
元素符号右上角
表示离子所带正(或负)电荷数
Mg2+表示镁离子或1个镁离子。
数字“2”表示1个镁离子带2个单位的正电荷
元素符号右下角
表示构成1个分子的原子个数或化合物中离子个数
H2表示氢气或1个氢气分子等。
数字“2”表示构成1个氢分子的氢原子个数(或1个氢分子是由2个氢原子构成)
原子结构示意图
表示某电子层上的电子数
2、化学式书写:
按照金左氧右、正前负后顺序书写,然后把元素的化合价交叉写在元素的右下角,再进行约分。
3、常见物质的俗名、学名、化学式
俗名
水银
干冰
煤气
沼气天然气
生石灰
熟石灰消石灰石灰浆石灰水
石灰石大理石
学名
化学式
食盐
酒精
铁锈赤铁矿
小苏打
纯碱、苏打
烧碱、苛性钠
三氧化二铁
氢氯酸
草木灰
碳酸钾
K2CO3
三、熟记下列元素在化合物中的化合价:
Fe(FeO)
Fe(Fe2O3)
+1
+2
+3
-2
-1
NH4
OH
NO3
ClO3
CO3
SO4
PO4
HCO3
MnO4(KMnO4)
-3
1、在计算物质化合价时,按照化合物中各元素化合价的代数和为零这一原则进行。
四、化学方程式
遵循原则
以客观事实为依据遵守质量守恒定律
书写
a、配平b、条件c、箭号
含义:
2H2+O2
2H2O
宏观
表明反应物、生成物、反应条件氢气和氧气在点燃的条件下生成水
微观
表示反应物和生成物之间分子每2个氢分子与1个氧分子化合生成2个水分子
量
各物质间质量比每4份质量的氢气与32份质量的氧气完全化合生成36份质量的水
提供的信息
①哪些物质参加反应(反应物);
②通过什么条件反应:
③反应生成了哪些物质(生成物);
④参加反应的各粒子的相对数量;
⑤反应前后质量守恒
五、元素周期表的规律:
①同一周期中的元素电子层数相同,从左至右核电荷数、质子数、核外电子数依次递增。
②同一族中的元素核外电子数相同、元素的化学性质相似,从上至下核电荷数、质子数、电子层数依次递增。
③非金属元素位于元素周期表的右上角,惰性气体位于元素周期表的最后一列。
六、原子结构知识中的八种决定关系
决定关系
原因
质子数决定原子核所带的电荷数(核电荷数)
原子中质子数=核电荷数
质子数决定元素的种类
不同元素原子中质子数不同
质子数、中子数决定原子的相对原子质量
原子中质子数+中子数=原子的相对原子质量
电子能量高低决定电子运动区域距离原子核的远近
离核越近的电子能量越低,越远的能量越高
原子最外层的电子数决定元素的类别
原子最外层的电子数<4为金属,>或=4为非金属,=8(第一层为最外层时=2)为稀有气体元素。
原子最外层的电子数决定元素的化学性质
原子最外层的电子数<4为失电子,>或=4为得电子,=8(第一层为最外层时=2)为稳定
原子最外层的电子数决定元素的化合价
原子失电子后元素显正价,得电子后元素显负价,化合价数值=得失电子数
原子最外层的电子数决定离子所带的电荷数
原子失电子后为阳离子,得电子后为阴离子,电荷数=得失电子数
六、常见化学用语区别
1、“溶化”与“熔化”:
“溶化”是指固体在液体中溶解。
如蔗糖在水中溶化了,碘在酒精中溶化了。
“熔化”是指固体加热到一定程度变成了液态。
如铁加热到1535℃时熔化成铁水,硫加热到112.8℃时即变成液态硫。
2.“蒸发”与“蒸馏”:
“蒸发”是在加热条件下溶液里溶剂气化的过程。
它能使溶液浓缩或溶质以晶体析出。
蒸发一般在蒸发皿中进行。
如氯化钠溶液经蒸发后可得NaCl晶体。
“蒸馏”是利用液体混合物各组分的沸点不同,使液体气化而进行的分离操作,它是分离或提纯液态混合物的常用方法。
蒸馏一般在蒸馏烧瓶中进行。
如蒸馏水就是用蒸馏方法制取的。
3.“通入”与“插入”:
“通入”一般指某气体通过导管进入某种溶液里。
例如把CO2气体通入到石灰水中。
“插入”一般指某种玻璃仪器放进另一种仪器中或某液体内。
如把玻璃管插入橡皮塞中,又如在制CO2实验中,为了防止气体从长颈漏斗逸出,需将漏斗下端插入液面以下。
4.“鉴别”与“鉴定”:
“鉴别”是根据物质的特征将几种物质区分、辨别出来。
如鉴别NaCl和Na2SO4溶液,可用滴入BaCl2溶液的方法,产生白色沉淀的原溶液为Na2SO4溶液,无变化的原溶液为NaCl溶液。
“鉴定”是要确定某物质的组成或是否存在。
例如,鉴定某白色晶体是否NH4Cl,就需证明该白色晶体中既含有NH4+,又含有Cl-。
5、点燃与燃烧:
点燃是条件,燃烧是现象
6、“烟”和“雾”:
“烟”一般指固体小颗粒,“雾”一般指液体小液滴。
7、“炭”和“碳”:
“碳”描述的是元素,“炭”描述的是具体的物质。
8、“吸水性”“吸附性”和“脱水性”:
“吸水性”“吸附性”指物质的物理性质,前者所吸的对象特指水,后者所吸的对象比较广泛。
“脱水性”指物质的化学性质。
9、“逸”和“溢”:
前者描述的对象是气体,后者描述的对象是液体。
Ⅱ、重要的物质
1、物质的分类:
1概念
定义
微观结构图
备注
混合物
由不同分子构成的物质
混合物和纯净物的主要区别在于物质是否是同一分子构成。
纯净物
由一种分子构成的物质
由同种元素组成的纯净物
由一种元素组成的物质不一定是单质,也可能是混合物,但一定不可能是化合物
由不同种元素组成的纯净物
由不同种元素组成的物质不一定是化合物,但化合物一定是由不同种元素组成的。
氧化物
由两种元素组成的,其中一
种是氧元素的化合物
氧化物一定是含氧化合物,但含氧化合物不一定是氧化物。
⑵物质分类易错点总结
水银不是银
水银Hg银Ag
铅芯不是铅
铅芯是石墨,铅Pt
干冰不是冰
干冰是固态二氧化碳,冰是固态水
纯碱不是碱
纯碱虽然显碱性,但是盐
冰水混合物不是混合物
冰水混合物是水的不同状态,是同种分子构成,属于纯净物
2、化学肥料:
种类
氮肥
磷肥
钾肥
对植物生长的作用
氮是构成植物体内蛋白质、核酸、叶绿素的主要成分。
氮肥能促使茎、叶茂盛,叶色浓绿,产量高、品质好
磷能促使作物根系发达,增强抗寒抗旱能力,早熟,穗粒增多,籽粒饱满
钾能促使作物茎杆粗壮,增强抗病、抗倒伏、抗旱、抗寒能力,促进糖和淀粉的生成
常用化肥
碳铵NH4HCO3,尿素CO(NH2)2,硫铵(NH4)2SO4,硝铵NH4NO3,氨水NH3·
磷矿粉〔磷酸钙Ca3(PO4)2〕
氯化钾KCl,硫酸钾K2SO4,草木灰(含K2CO3)
另外在有些化肥中同时含有两种或两种以上的营养元素,如磷酸二氢铵NH4H2PO4、硝酸钾(KNO3)等。
这样的化肥叫复合肥料。
这类肥料的特点是能同时均匀地供给作物几种养分,充分发挥营养元素间的相互作用,有效成分高。
3、人体所需的营养素
营养素
功能作用
来源
蛋白质
促进生长发育和新陈代谢
动物蛋白--肉
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 卓顶精文 最新 初中化学 重要 考点 汇编 化学 用语 doc
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 (完整word版)信息论与编码期末考试题----学生复习用.doc
(完整word版)信息论与编码期末考试题----学生复习用.doc
 (完整版)固定资产盘点表.xls
(完整版)固定资产盘点表.xls
 标本采集要求及注意事项.ppt
标本采集要求及注意事项.ppt
