 新高考化学试题解析分项17物质结构与性质选修Word文档格式.docx
新高考化学试题解析分项17物质结构与性质选修Word文档格式.docx
- 文档编号:13222296
- 上传时间:2022-10-08
- 格式:DOCX
- 页数:72
- 大小:3.02MB
新高考化学试题解析分项17物质结构与性质选修Word文档格式.docx
《新高考化学试题解析分项17物质结构与性质选修Word文档格式.docx》由会员分享,可在线阅读,更多相关《新高考化学试题解析分项17物质结构与性质选修Word文档格式.docx(72页珍藏版)》请在冰豆网上搜索。
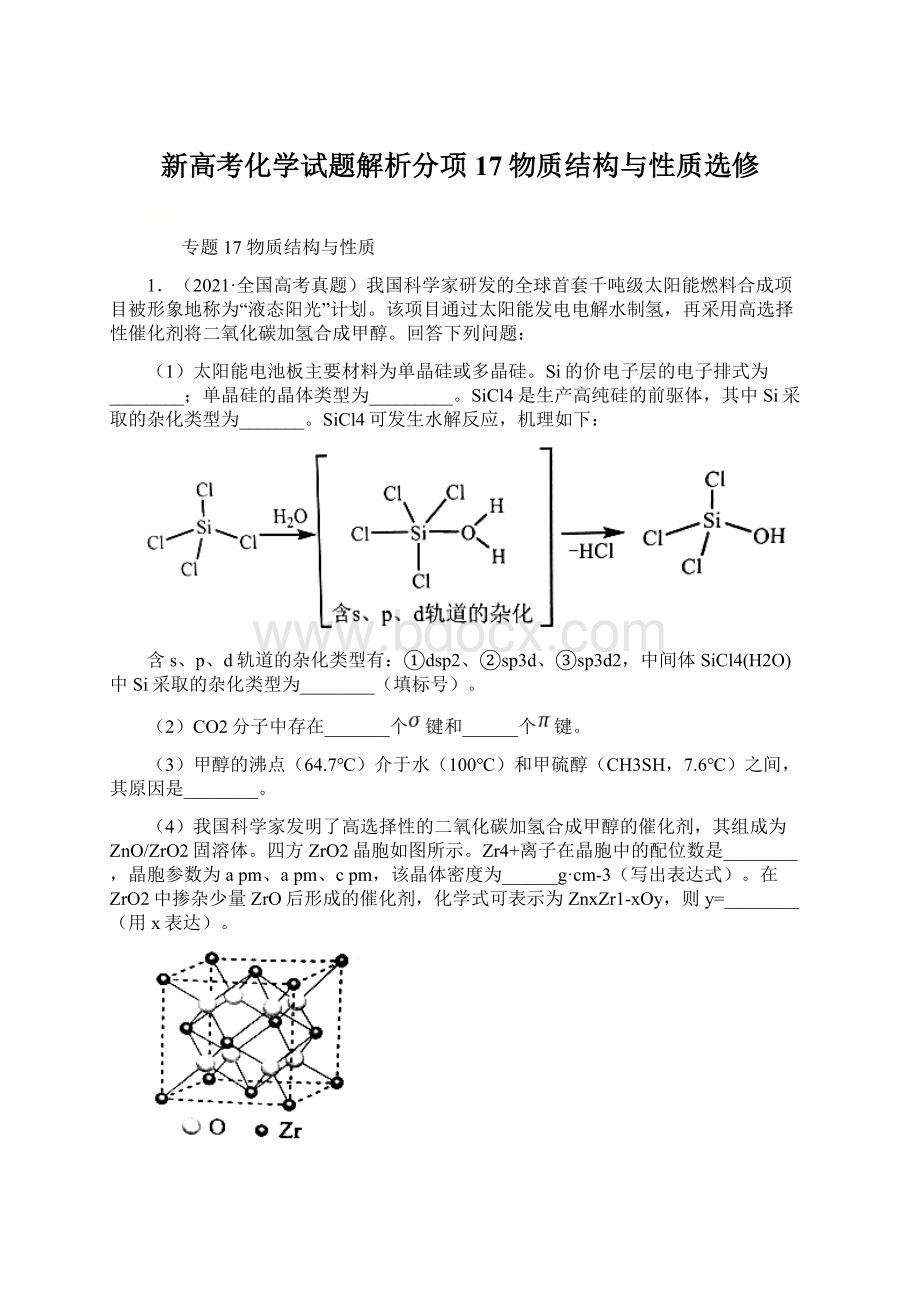
四方ZrO2晶胞如图所示。
Zr4+离子在晶胞中的配位数是________,晶胞参数为apm、apm、cpm,该晶体密度为______g·
cm-3(写出表达式)。
在ZrO2中掺杂少量ZrO后形成的催化剂,化学式可表示为ZnxZr1-xOy,则y=________(用x表达)。
【答案】3s23p2原子晶体(共价晶体)sp3②22甲硫醇不能形成分子间氢键,而水和甲醇均能,且水比甲醇的氢键多82-x
【解析】
(1)基态Si原子的核外电子排布式为1s22s22p63s23p2,因此Si的价电子层的电子排式为3s23p2;
晶体硅中Si原子与Si原子之间通过共价键相互结合,整块晶体是一个三维的共价键网状结构,因此晶体硅为原子晶体;
SiCl4中Si原子价层电子对数为4+=4,因此Si原子采取sp3杂化;
由图可知,SiCl4(H2O)中Si原子的δ键数为5,说明Si原子的杂化轨道数为5,由此可知Si原子的杂化类型为sp3d,故答案为:
3s23p2;
原子晶体(共价晶体);
sp3;
②;
(2)CO2的结构式为O=C=O,1个双键中含有1个δ键和1个π键,因此1个CO2分子中含有2个δ键和2个π键,故答案为:
2;
(3)甲醇分子之间和水分子之间都存在氢键,因此沸点高于不含分子间氢键的甲硫醇,甲醇分子之间氢键的总强度低于水分子之间氢键的总强度,因此甲醇的沸点介于水和甲硫醇之间,故答案为:
甲硫醇不能形成分子间氢键,而水和甲醇均能,且水比甲醇的氢键多;
(4)以晶胞中右侧面心的Zr4+为例,同一晶胞中与Zr4+连接最近且等距的O2-数为4,同理可知右侧晶胞中有4个O2-与Zr4+相连,因此Zr4+离子在晶胞中的配位数是4+4=8;
1个晶胞中含有4个ZrO2微粒,1个晶胞的质量m=,1个晶胞的体积为(a×
10-10cm)×
(a×
(c×
10-10cm)=a2c×
10-30cm3,因此该晶体密度===g·
cm-3;
在ZrO2中掺杂少量ZrO后形成的催化剂,化学式可表示为ZnxZr1-xOy,其中Zn元素为+2价,Zr为+4价,O元素为-2价,根据化合物化合价为0可知2x+4×
(1-x)=2y,解得y=2-x,故答案为:
;
2-x。
2.(2021·
吉林长春市·
长春外国语学校高二月考)过渡金属元素铬是不锈钢的重要成分,在工农业生产和国防建设中有着广泛应用。
(1)对于基态Cr原子,下列叙述正确的是_______(填标号)。
A.轨道处于半充满时体系总能量低,核外电子排布应为
B.4s电子能量较高,总是在比3s电子离核更远的地方运动
C.电负性比钾高,原子对键合电子的吸引力比钾大
(2)三价铬离子能形成多种配位化合物。
中提供电子对形成配位键的原子是_______,中心离子的配位数为_______。
(3)中配体分子、以及分子的空间结构和相应的键角如图所示。
中P的杂化类型是_______。
的沸点比的_______,原因是_______,的键角小于的,分析原因_______。
(4)在金属材料中添加颗粒,可以增强材料的耐腐蚀性、硬度和机械性能。
具有体心四方结构,如图所示,处于顶角位置的是_______原子。
设Cr和Al原子半径分别为和,则金属原子空间占有率为_______%(列出计算表达式)。
【答案】AC6高存在分子间氢键含有一对孤对电子,而含有两对孤对电子,中的孤对电子对成键电子对的排斥作用较大Al
(1)A.基态原子满足能量最低原理,Cr有24个核外电子,轨道处于半充满时体系总能量低,核外电子排布应为,A正确;
B.Cr核外电子排布为,由于能级交错,3d轨道能量高于4s轨道的能量,即3d电子能量较高,B错误;
C.电负性为原子对键合电子的吸引力,同周期除零族原子序数越大电负性越强,钾与铬位于同周期,铬原子序数大于钾,故铬电负性比钾高,原子对键合电子的吸引力比钾大,C正确;
故答案为:
AC;
(2)中三价铬离子提供空轨道,提供孤对电子与三价铬离子形成配位键,中心离子的配位数为三种原子的个数和即3+2+1=6,故答案为:
6;
(3)的价层电子对为3+1=4,故中P的杂化类型是;
N原子电负性较强,分子之间存在分子间氢键,因此的沸点比的高;
的键角小于的,原因是:
含有一对孤对电子,而含有两对孤对电子,中的孤对电子对成键电子对的排斥作用较大,故答案为:
高;
存在分子间氢键;
含有一对孤对电子,而含有两对孤对电子,中的孤对电子对成键电子对的排斥作用较大;
(4)已知具有体心四方结构,如图所示,黑球个数为,白球个数为,结合化学式可知,白球为Cr,黑球为Al,即处于顶角位置的是Al原子。
设Cr和Al原子半径分别为和,则金属原子的体积为,故金属原子空间占有率=%,故答案为:
Al;
。
3.(2021·
广东高考真题)很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。
例如,解毒剂化合物I可与氧化汞生成化合物Ⅱ。
(1)基态硫原子价电子排布式为__________。
(2)H2S、CH4、H2O的沸点由高到低顺序为__________。
(3)汞的原子序数为80,位于元素周期表第______周期第ⅡB族。
(4)化合物Ⅲ也是一种汞解毒剂。
化合物Ⅳ是一种强酸。
下列说法正确的有________。
A.在I中S原子采取sp3杂化
B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C-C-C键角是180°
D.在Ⅲ中存在离子键与共价键
E.在Ⅳ中硫氧键的键能均相等
(5)汞解毒剂的水溶性好,有利于体内重金属元素汞的解毒。
化合物I与化合物Ⅲ相比,水溶性较好的是________。
(6)理论计算预测,由汞(Hg)、锗(Ge)、锑(Sb)形成的一种新物质X为潜在的拓扑绝缘体材料。
X的晶体可视为Ge晶体(晶胞如图9a所示)中部分Ge原子被Hg和Sb取代后形成。
①图9b为Ge晶胞中部分Ge原子被Hg和Sb取代后形成的一种单元结构,它不是晶胞单元,理由是__________________。
②图9c为X的晶胞,X的晶体中与Hg距离最近的Sb的数目为_________;
该晶胞中粒子个数比Hg:
Ge:
Sb=_________。
③设X的最简式的式量为Mr,则X晶体的密度为________g/cm3(列出算式)。
【答案】3s23p4H2O>
H2S>
CH4六AD化合物III由图9c可知,图9b中Sb、Hg原子取代位置除图9b外还有其它形式41:
1:
2
(1)基态硫原子核外电子排布式为1s22s22p63s23p4,因此基态硫原子价电子排布式为3s23p4,故答案为:
3s23p4。
(2)H2S、CH4、H2O均为分子晶体,H2O分子间存在氢键,沸点较高,H2S、CH4的分子间范德华力随相对分子质量增大而增加,因此沸点由高到低顺序为:
H2O>
CH4,故答案为:
CH4。
(3)第六周期0族元素的原子序数为86,因此第80号元素Hg位于第六周期第ⅡB族,故答案为:
六。
(4)A.中S原子的价层电子对数=2+=4,因此S原子采取sp3杂化,故A正确;
B.中含有的元素为H、C、O、S、Hg,同周期元素从左至右元素的电负性逐渐增大,同主族元素从上至下元素的电负性逐渐减小,因此5种元素中电负性最大的为O元素,故B错误;
C.中C原子成键均为单键,因此C原子采取sp3杂化,所以C-C-C键角接近109º
28’,故C错误;
D.中存在C-H、C-C、C-S、S=O、S-O、S-H共价键和与Na+之间的离子键,故D正确;
E.中硫氧键分为硫氧单键和硫氧双键,共价键种类不同,因此二者的键能不同,故E错误;
综上所述,说法正确的是AD项,故答案为AD。
(5)中羟基能与水分子之间形成分子间氢键,为易溶于水的钠盐,溶于水后电离出的中O原子均能与水分子之间形成氢键,相同物质的量两种物质溶于水后,形成的氢键更多,因此化合物III更易溶于水,故答案为:
化合物III。
(6)①对比图9b和图9c可得X晶体的晶胞中上下两个单元内的原子位置不完全相同,不符合晶胞晶胞是晶体的最小重复单位要求,故答案为:
由图9c可知,图9b中Sb、Hg原子取代位置除图9b外还有其它形式。
②以晶胞上方立方体中右侧面心中Hg原子为例,同一晶胞中与Hg距离最近的Sb的数目为2,右侧晶胞中有2个Sb原子与Hg原子距离最近,因此X的晶体中与Hg距离最近的Sb的数目为4;
该晶胞中Sb原子均位于晶胞内,因此1个晶胞中含有Sb原子数为8,Ge原子位于晶胞顶点、面心、体心,因此1个晶胞中含有Ge原子数为1+8×
+4×
=4,Hg原子位于棱边、面心,因此1个晶胞中含有Hg原子数为6×
=4,则该晶胞中粒子个数比Hg:
Sb=4:
4:
8=1:
2,故答案为:
4;
2。
③1个晶胞的质量m=,1个晶胞的体积V=(x×
10-7cm)2×
(y×
10-7cm)=x2y×
10-21cm3,则X晶体的密度为==g/cm3,故答案为:
4.(2021·
河北高考真题)KH2PO4晶体具有优异的非线性光学性能。
我国科学工作者制备的超大KH2PO4晶体已应用于大功率固体激光器,填补了国家战略空白。
(1)在KH2PO4的四种组成元素各自所能形成的简单离子中,核外电子排布相同的是__(填离子符号)。
(2)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+表示,与之相反的用-表示,称为电子的自旋磁量子数.对于基态的磷原子,其价电子自旋磁量子数的代数和为___。
(3)已知有关氨、磷的单键和三键的键能(kJ•mol-1)如表:
N—N
N≡N
P—P
P≡P
193
946
197
489
从能量角度看,氮以N2、而白磷以P4(结构式可表示为)形式存在的原因是___。
(4)已知KH2PO4是次磷酸的正盐,H3PO2的结构式为___,其中P采取___杂化方式。
(5)与PO电子总数相同的等电子体的分子式为__。
(6)磷酸通过分子间脱水缩合形成多磷酸,如:
如果有n个磷酸分子间脱水形成环状的多磷酸,则相应的酸根可写为___。
(7)分别用○、●表示H2PO和K+,KH2PO4晶体的四方晶胞如图(a)所示,图(b)、图(c)分别显示的是H2PO、K+在晶胞xz面、yz面上的位置:
①若晶胞底边的边长均为apm、高为cpm,阿伏加德罗常数的值为NA,晶体的密度__g•cm-3(写出表达式)。
②晶胞在x轴方向的投影图为__(填标号)。
【答案】和或在原子数目相同的条件下,N2比N4具有更低的能量,而P4比P2具有更低的能量,能量越低越稳定sp3SiF4、SO2F2
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 新高 化学试题 解析 17 物质 结构 性质 选修
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 国企会计岗位笔试试题及答案解析(分享).docx
国企会计岗位笔试试题及答案解析(分享).docx
 行政事业单位内部审计流程图(按照新内部审计准则).xls
行政事业单位内部审计流程图(按照新内部审计准则).xls
