 GMP检查评定的项目和内容_精品文档Word文档下载推荐.doc
GMP检查评定的项目和内容_精品文档Word文档下载推荐.doc
- 文档编号:13202530
- 上传时间:2022-10-08
- 格式:DOC
- 页数:18
- 大小:157KB
GMP检查评定的项目和内容_精品文档Word文档下载推荐.doc
《GMP检查评定的项目和内容_精品文档Word文档下载推荐.doc》由会员分享,可在线阅读,更多相关《GMP检查评定的项目和内容_精品文档Word文档下载推荐.doc(18页珍藏版)》请在冰豆网上搜索。
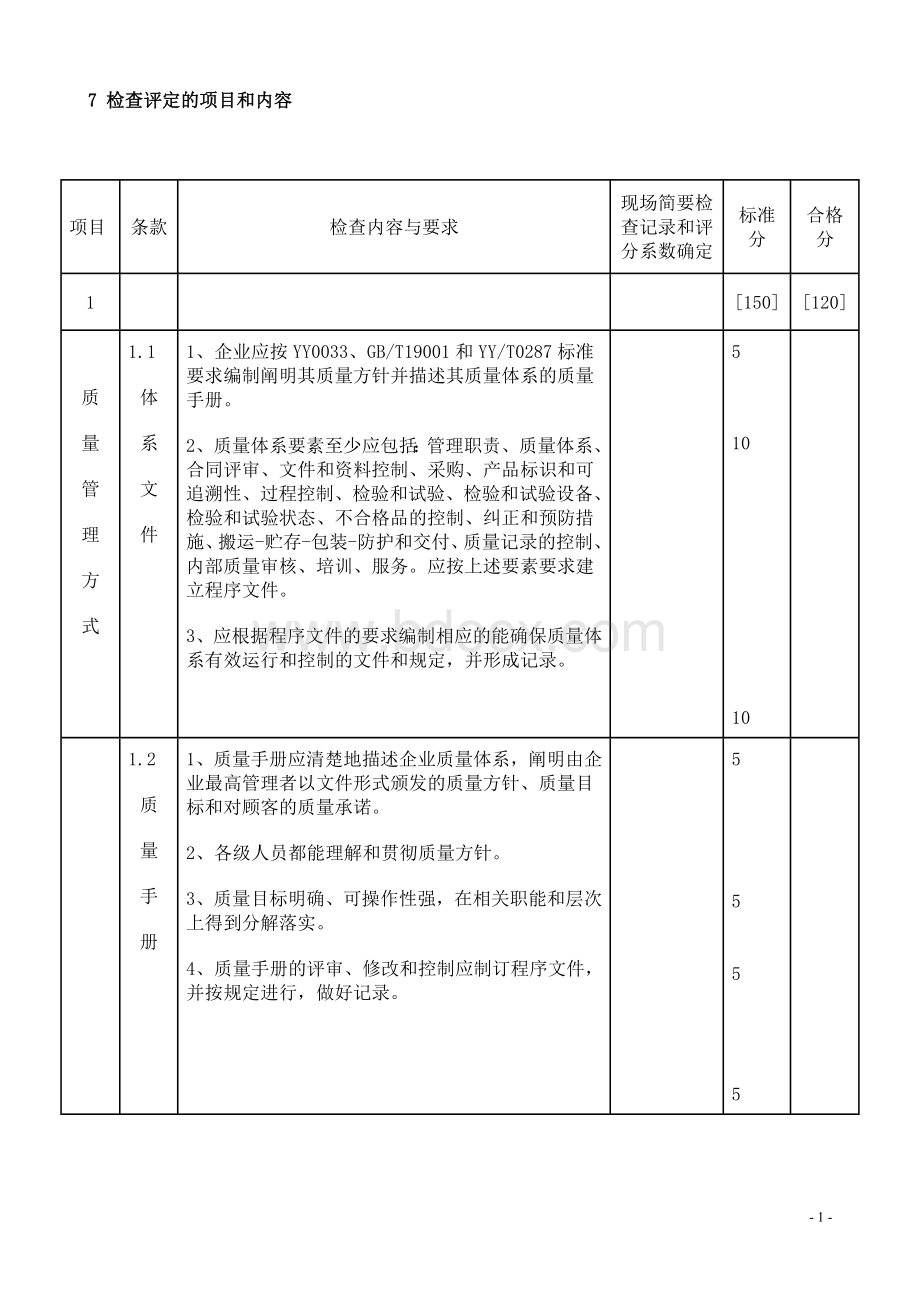
文
件
1、企业应按YY0033、GB/T19001和YY/T0287标准要求编制阐明其质量方针并描述其质量体系的质量手册。
2、质量体系要素至少应包括:
管理职责、质量体系、合同评审、文件和资料控制、采购、产品标识和可追溯性、过程控制、检验和试验、检验和试验设备、检验和试验状态、不合格品的控制、纠正和预防措施、搬运-贮存-包装-防护和交付、质量记录的控制、内部质量审核、培训、服务。
应按上述要素要求建立程序文件。
3、应根据程序文件的要求编制相应的能确保质量体系有效运行和控制的文件和规定,并形成记录。
5
10
1.2
手
册
1、质量手册应清楚地描述企业质量体系,阐明由企业最高管理者以文件形式颁发的质量方针、质量目标和对顾客的质量承诺。
2、各级人员都能理解和贯彻质量方针。
3、质量目标明确、可操作性强,在相关职能和层次上得到分解落实。
4、质量手册的评审、修改和控制应制订程序文件,并按规定进行,做好记录。
1.3
的
控
制
1、按文件资料控制程序文件,对与质量有关的所有文件和资料(包括质量体系文件、产品质量文件、有关的外部文件和资料等)进行控制。
2、文件应按规定进行批准、发布、更改、废止和保存。
3、按规定受控的文件应有受控状态标识。
4、发布、使用的文件为批准的有效版本,已作废的文件除留档外,不得在工作现场出现。
5、文件的更改应及时、准确,并应由该文件的原审批部门进行审批。
6、应制定质量记录的管理规定(规定至少应包含记录分类、汇总、保管、保存期限等内容)。
1.4
组
织
机
构
1、企业最高管理者应在厂级管理层中指定一名成员为管理者代表,并书面明确其职责和权限。
2、对从事与质量有关的管理、执行和验证工作的部门和人员,应有书面文件规定其职责,包括:
企业领导层人员职责与权限;
各职能部门职责与权限;
检验、验证人员职责与权限;
各岗位操作人员的职责与权限;
组织机构图。
1.5
人
员
和
培
训
企业应配备与所生产产品相适应的各类人员,并按程序文件进行培训。
1、企业最高管理者应熟悉国家有关医疗器械法律、法规,熟悉产品生产技术,对产品质量负全部责任。
2、从事生产、技术和质量管理的部门负责人应具有大专(或相当于大专以上学历,并熟悉本部门业务,有生产、技术和质量管理的实践经验。
生产管理部门与质量管理部门负责人不得互相兼任。
3、检验人员须有高中以上学历,实验室检验人员并需经省级以上药品监督管理部门认可的专业机构进行专业技术培训合格。
4、参与企业质量体系内部审核的人员均应有医疗器械内审员证书,内审员不少于2人。
5、关键生产岗位操作人员应经专业技术培训合格方能上岗。
6、有员工名册、按人员培训的程序文件制定的人员培训计划和人员受培训的档案记录。
记录项
1.6
评
审
内
部
核
1、管理评审的程序文件。
2、企业最高管理者,应按管理评审程序规定对质量体系进行评审,确保持续的适应性和有效性。
3、对管理评审过程中发现的问题应及时采取有效措施,有计划地加以解决。
4、应有内部质量体系审核的程序文件,由有资格的内审员有计划、系统地进行内部质量体系审核。
5、审过程中发现的问题有关部门负责人应及时采取纠正措施,并在跟踪审核活动中应予验证。
6、管理评审、内审记录(报告等)应予以保存。
2
[145]
[116]
生
产
环
境
、
设
施
布
局
2.1
厂
址
区
1、厂区位置应远离空气和水污染区;
洁净厂房与市政交通干道之间的距离不小于50米。
2、厂区内应整洁,无积水、杂草、露天垃圾、蚊蝇孳生地,垃圾及废弃物料有指定的集中堆放地点,并有防扩散措施。
3、厂区内应尽量减少露土面积;
路面平整不易起尘。
4、厂生产区与生活区分开。
2.2
房
1、企业应提供洁净区内生产工艺流程图和空气调节、配电照明等平/立面图;
新建、改建、扩建的洁净区厂房应提供有资质的设计单位设计的图纸。
2、应采用中央空调、集中送风的空气调节净化系统,有管理文件和保养维护记录。
3、进入洁净区的管道、送、回风口布局合理,水、电、气输送线路与墙体接口处应可靠密封,照明灯具不得悬吊。
4、洁净车间安全门向安全疏散方向开启,平时密封良好,紧急情况发生时应能保证畅通。
5、洁净车间门口应有有效防止异物进入的措施,有玻璃窗的应双层密闭,进入清洁区前的门厅宽敞、明亮、整洁。
6、有足够的人员清洁空间,洗衣间的洁净度级别不低于三十万级,应有足够的洗衣、干燥空间并配置消毒设施。
7、不同洁净度要求的区间出入口处,有易于观察的压差表,洁净区各车间应有温、湿度计,压差表、温、湿度计有校验记录,自然照度差和有夜班的应有应急照明设施。
8、洁净区应按本《细则》相应附件的规定进行监测,监测项目要有记录并达到要求。
审查员查阅半年的监测记录,并现场抽查、验证、记录。
9、洁净区内墙、顶棚和地面应平整、光滑、无裂缝、无颗粒物脱落、无油(水)渍,能耐受清洗和消毒,水池、地漏不得对无菌医疗器具产生污染。
10、生产区按工艺流程合理布局,人流、物流应分开,洁净区的门应密封良好,并向洁净度高的方位开启。
11、操作台(板)应光滑、平整、无缝隙、不脱落异物,便于清洗、消毒,不可用木质或油漆台面。
12、洁净区内应配置空气消毒装置,有平面布置图、编号和使用记录。
13、每个洁净间(区)工作人员人均面积≥4m2。
14、注、挤塑间送、回风合理,回风不得再循环使用。
2.3
人员净化
1、应建立、执行人员进出洁净区的清洁程序和管理制度,人员清洁程序合理。
2、洗手装置(按最大班人数计算)每10人设一个,龙头关闭不能用手,如有卫生间、洁具间、职工休息室不能对洁净区产生不良影响。
3、进入洁净区工作的人员应穿不易脱落纤维的防静电工作服(应能阻留人体脱落物)并戴口罩,非一次性使用口罩、工作鞋要规定清洗办法和频次。
5
2.4
物料
净化
1、应建立、执行物料进出洁净区的清洁程序,有脱外包装室、净化室和双层传递窗(或气闸室)。
2、精洗、烘干工序应在10万级洁净室(区)内独立的工作间进行。
2.5
用水、用
气
1、具有制备达到纯化水要求的设备(需清洗与药、血液直接接触部件的应制备注射用水),水的输送管道和贮罐应是不锈钢或其他无毒材料并定期消毒,制水能力能满足生产需要。
2、冷却用水应达到国家饮用水标准,洁净区工位器具应用纯化水清洗,清洗与药(血)液直接接触部件应用注射用水。
3、应按控制工艺用水的管理文件和相关标准检测并记录:
用去离子法制得的纯化水:
电阻率>0.5兆欧·
厘米(或电导率≤2μs/cm)1次/班。
用蒸馏法制得的纯化水和注射用水:
PH、氯化物、铵盐1次/班检测。
全性能检测1次/周。
4、洁净室(区)内使用的压缩气体应经过净化处理,与产品使用表面相接触的气体应进行验证和常规控制。
3
[70]
[56]
备
工
装、
位
器
具
3.1设备、工装、工位器具技术要求
1、洁净区内选用的设备与工装应具有防尘、防污染措施,设备、工装与管道表面应光洁、平整、不得有颗粒物质脱落,易于清洗和消毒。
2、与物料或产品直接接触的设备、工装及管道表面应清洁卫生、无毒、耐腐蚀、无死角,并易于清洗和消毒。
3、设备所用的润滑剂、冷却剂、清洗剂及在洁净区内通过模具成型后不清洗的零配件所用的脱模剂,都不得对产品造成污染。
4、置独立的模具间(或区域),用于模具的维护和存放。
5、工位器具应易于清洗和消毒,应定期使用纯化水在洁净区内清洗,在洁净区内用于储存的工位器具应无孔带盖且有明显标识。
洁净区与一般生产区使用的工位器具要严格分开、不得交叉使用。
3.2
设备、工装、工位器具配置
1、企业应配置与生产规模相适应的工位器具。
2、企业应配置与生产规模相适应的生产设备和工艺装备。
其中包括:
全部注、挤、吹塑件的加工设备,注射针、静脉输液针生产企业还应具有与生产工艺相适应的针管加工设备。
3.3
设备、工装、工位器具管理
1.生产设备、工艺装备实行统一购置、统一安装验收、统一管理、建立台帐。
对主要设备和工艺装备并应建立档案。
2.建立生产设备、工艺装备的检查、维修、保养制度和工位器具管理制度。
对生产设备的完好状态应有明显标识。
3.应编制主要设备的操作规程,明确规定设备的使用方法、维护保养方法和频次。
4.主要设备和工艺装备的操作人员、维修人员应经培训合格后上岗。
特殊环境下工作的灭菌设备操作人员、维修人员应持证上岗。
5.应做好主要设备和工艺装备的检查、维修、保养、验证,并做好记录。
6.生产设备、工艺装备和工位器具的技术指标应符合洁净环境控制和工艺文件的要求。
4
[60]
[48]
采
购
与
库
4.1
采购文件
应制订原料、外协件和外购件采购程序文件和管理文件,以确保所采购的产品符合规定要求。
1、应编制采购文件,至少包括采购计划、采购清单、采购合同/技术协议书、分承包方名录。
注:
采购清单中若有必须持有医疗器械产品注册证、生产企业许可证企业的产品(主要零组件、粒料),应符合本《细则》规定。
2、采购合同/技术协议书应明确规定采购物料的质量要求,至少包括以下内容:
产品名称、型号规格、执行标准或技术条件、检验规程、接收方式及有关技术资料的名称或其他明确标识的适用版本。
3、对没有国家标准和行业标准的原材(辅)料,企业应制定符合产品要求的技术标准,直接采用分供方企业标准的,应满足产品标准要求;
4、应保存有关采购文件,以满足可追溯性要求。
4.2
分承包方评价
应制定分承包方评价的程序文件。
1、应根据采购文件的要求,评价和选定分承包方,建立并保存合格的分承包方的质量记录。
2、分承包方评价的内容至少应包括:
a.关键外购、外协件的分承包方是否具有符合国家法律、法规、规章及本《细则》规定要求的证照;
b.分承包方的生产条件是否具备本《细则》规定要求的设备条件和环境条件;
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- GMP 检查 评定 项目 内容 精品 文档
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 12处方点评管理规范实施细则_精品文档.doc
12处方点评管理规范实施细则_精品文档.doc
 17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
 新人教版《雪地里的小画家》ppt课件.ppt
新人教版《雪地里的小画家》ppt课件.ppt
