 物理化学---知识点总结文档格式.doc
物理化学---知识点总结文档格式.doc
- 文档编号:13067023
- 上传时间:2022-10-04
- 格式:DOC
- 页数:34
- 大小:500.50KB
物理化学---知识点总结文档格式.doc
《物理化学---知识点总结文档格式.doc》由会员分享,可在线阅读,更多相关《物理化学---知识点总结文档格式.doc(34页珍藏版)》请在冰豆网上搜索。
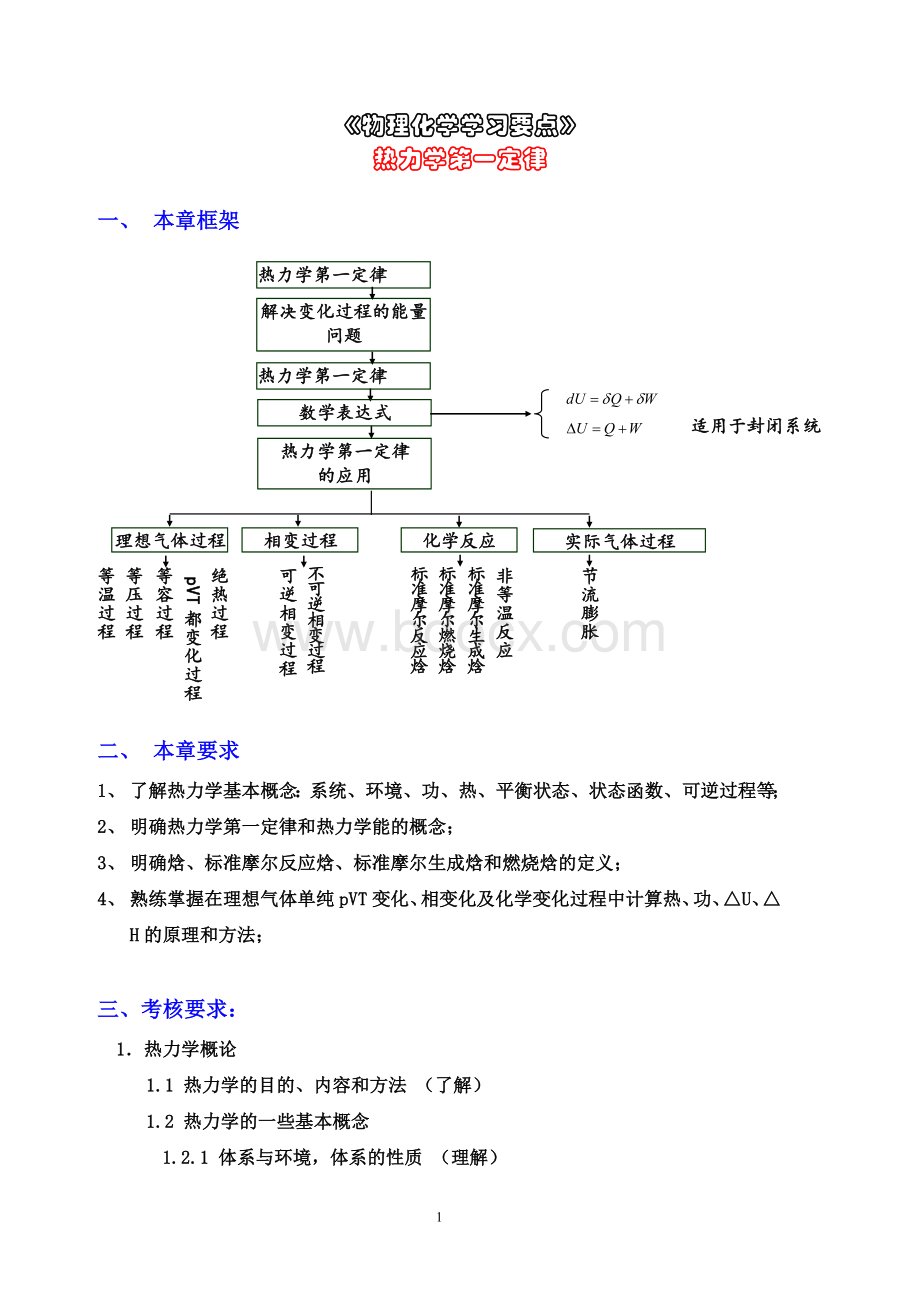
2、明确热力学第一定律和热力学能的概念;
3、明确焓、标准摩尔反应焓、标准摩尔生成焓和燃烧焓的定义;
4、熟练掌握在理想气体单纯pVT变化、相变化及化学变化过程中计算热、功、△U、△H的原理和方法;
三、考核要求:
1.热力学概论
1.1热力学的目的、内容和方法(了解)
1.2热力学的一些基本概念
1.2.1体系与环境,体系的性质(理解)
1.2.2
热力学平衡态和状态函数(理解)
2.热力学第一定律
2.1热和功(掌握)
2.2热力学能(掌握)
2.3热力学第一定律的表述与数学表达式(应用)
3.体积功与可逆过程
3.1等温过程的体积功(应用)
3.2可逆过程与最大功(理解)
4.焓与热容
4.1焓的定义(了解)
4.2焓变与等压热的关系(应用)
4.3等压热容和等容热容(理解)
5.热力学第一定律对理想气体的应用
5.1理想气体的热力学能和焓(掌握)
5.2理想气体的Cp与Cv之差(理解)
5.3理想气体的绝热过程
(掌握)
6.热力学第一定律对实际气体的应用
6.1节流膨胀与焦耳-汤姆逊效应(了解)
7.热力学第一定律对相变过程的应用(掌握)
8.化学热力学
8.1化学反应热效应
8.1.1等压热效应与等容热效应(掌握)
8.1.2反应进度(了解)
8.2赫斯定律与常温下反应热效应的计算
8.2.1赫斯定律(应用)
8.2.2标准摩尔生成焓与标准摩尔燃烧焓
(掌握)
8.3标准反应焓变与温度的关系—基尔霍夫定律(应用)
四、重要概念
1、系统与环境;
2、隔离系统、封闭系统、敞开系统;
注意:
隔离系统Q=0,W=0
3、广度性质(加和性:
V,U,H,S,A,G)
强度性质(物质的量,T,p);
4、功W和热Q;
注意W与Q的符号;
W与Q均为途径函数(非状态函数)
5、热力学能;
6、焓;
7、热容;
8、状态与状态函数;
9、平衡态;
10、
可逆过程;
11、节流过程;
12、真空膨胀过程;
13、标准态;
14、标准摩尔反应焓,标准摩尔生成焓,标准摩尔燃烧焓
五、重要公式与适用条件
1.体积功:
W=-p外dV(封闭系统,计算体积功)
2.热力学第一定律:
DU=Q+W,dU=Q+W(封闭系统)
3.焓的定义:
H=U+pV
4.热容:
定容摩尔热容CV,m=QV/dT=(¶
Um/¶
T)V
定压摩尔热容Cp,m=Qp/dT=(¶
Hm/¶
T)P
理想气体:
Cp,m-CV,m=R;
凝聚态:
Cp,m-CV,m≈0
理想单原子气体CV,m=3R/2,Cp,m=CV,m+R=5R/2
5.标准摩尔反应焓:
由标准摩尔生成焓DfHBy(T)或标准摩尔燃烧焓DcHBy(T)计算
DrHmy=SvBDfHBy(T)=-SvBDcHBy(T)
6.基希霍夫公式(适用于相变和化学反应过程)
DrHmy(T2)=DrHmy(T1)+
7.等压摩尔反应热与等容摩尔反应热的关系式
Qp-QV=DrHm(T)-DrUm(T)=SvB(g)RT
8.理想气体的可逆绝热过程方程:
六、各种过程Q、W、DU、DH的计算
1、理想气体:
等温过程dT=0,DU=DH=0,Q=W;
非等温过程,DU=nCV,mDT,DH=nCp,mDT,
单原子气体CV,m=3R/2,Cp,m=CV,m+R=5R/2
2、对于凝聚相,状态函数通常近似认为与温度有关,而与压力或体积无关,即
DU≈DH=nCp,mDT
3.等压过程:
p外=p=常数,非体积功为零W'
=0
(1)W=-p外(V2-V1),DH=Qp=,DU=DH-D(pV),Q=DU-W
(2)真空膨胀过程p外=0,W=0,Q=DU
理想气体结果:
dT=0,W=0,Q=DU=0,DH=0
(3)等外压过程:
W=-p外(V2-V1)
4.等容过程:
dV=0
W=0,QV=DU=,DH=DU+VDp
5.绝热过程:
Q=0
(1)绝热可逆过程W==DU=,DH=DU+DpV
理想气体:
(2)绝热一般过程:
由方程W=DU=建立方程求解。
6.节流过程(等焓过程):
DH=0,Q=0
焦耳-汤姆逊系数μJ-T=(¶
T/¶
p)H,理想气体μJ-T=0,实际气体μJ-T≠0
7.相变过程:
(1)可逆相变(正常相变或平衡相变):
在温度T对应的饱和蒸气压下的相变,如水在常压下的0℃结冰或冰溶解
(2)不可逆相变
热力学第二定律
一、本章框架
二、本章要求
1.了解自发过程的共同特征;
2.理解第二、第三定律的表述;
3.了解卡诺循环的意义;
4.理解克劳修斯不等式;
5.掌握熵增原理和平衡判据的一般准则;
6.明确熵、赫姆霍兹函数、吉布斯函数、标准摩尔熵及标准摩尔生成吉布斯自由能的定义并会应用;
7.熟练掌握在理想气体单纯pVT变化、相变及化学变化过程中计算△S、△A、△G的原理和方法;
8.理解热力学基本方程;
9.掌握推导热力学公式的演绎方法;
10.了解麦克斯韦关系式的推导及应用;
三、重要概念
1.卡诺循环
2.热机效率
3.熵
4.亥姆霍兹函数
5.吉布斯函数
四、主要公式与定义式
1.热机效率:
η=-W/Q1=(Q1+Q2)/Q1=1-T2/T1
2.卡诺定理:
任何循环的热温熵小于或等于0
不可逆
可逆
Q1/T1+Q2/T2≤0
3.熵的定义式:
dS=Qr/T
4.亥姆霍兹(Helmholtz)函数的定义式:
A=U-TS
5.吉布斯(Gibbs)函数的定义式:
G=H-TS,G=A+pV
6.热力学第三定律:
S*(0K,完美晶体)=0
7.过程方向的判据:
(1)等温等压不做非体积功过程(最常用):
dG<
0,自发(不可逆);
dG=0,平衡(可逆)。
(2)一般过程用熵判据:
DS(隔离系统)>
DS(隔离系统)=0,平衡(可逆)。
DS(绝热系统)>
DS(绝热系统)=0,平衡(可逆)。
(3)等温等容不做非体积功过程:
dA<
dA=0,平衡(可逆)。
8.热力学基本方程与麦克斯韦关系式
基本式:
dU=TdS-pdV
其他式:
dH=d(U+pV)=TdS+Vdp
dA=d(U-TS)=-SdT–pdV
dG=d(H-TS)=-SdT+Vdp
以上系列式,应重点掌握dG=-SdT+Vdp
在恒压下的关系式dG=-SdT和恒温时的关系式dG=-Vdp。
麦克斯韦关系式(了解):
若dF=Mdx+Ndy,则(¶
M/¶
y)x=(¶
N/¶
x)y
即:
利用dU=TdS-pdV关系有:
-(¶
T/¶
V)S=(¶
p/¶
S)V
dH=TdS+Vdp关系有:
(¶
p)S=(¶
V/¶
S)p
dA=-SdT-pdV关系有:
(¶
S/¶
V)T=(¶
T)V
dG=-SdT+Vdp关系有:
p)T=(¶
T)p
五、DS、DA、DG的计算
1.DS的计算
(1)理想气体pVT过程的计算
dS=Qr/T=(dU-Wr)/T=(nCV,mdT-pdV)/T
(状态函数与路径无关,理想气体:
p=nRT/V)
积分结果:
DS=nCV,mln(T2/T1)+nRln(V2/V1)(代入:
V=nRT/p)
=nCp,mln(T2/T1)+nRln(p1/p2)(Cp,m=CV,m+R)
特例:
等温过程:
DS=nRln(V2/V1)
等容过程:
DS=nCV,mln(T2/T1)
等压过程:
DS=nCp,mln(T2/T1)
(2)等容过程:
DS=(nCV,m/T)dT
(3)等压过程:
DS=
(4)相变过程:
可逆相变DS=DH/T
(5)环境过程:
认为是恒温的大热源,过程为可逆
DS=Qr(环)/T(环)=-Q(系)/T(环)
(6)绝对熵的计算:
利用热力学第三定律计算的熵为绝对熵,过程通常涉及多个相变过程,是一个综合计算过程。
(7)标准摩尔反应熵的计算
DrSmy=SvBSmy(B,T)
2.DG的计算
(1)平衡相变过程:
DG=0
(2)等温过程:
DG=DH-TDS
(3)非等温过程:
DG=DH-DTS=DH-(T2S2-T1S1)=DH-(T2DS-S1DT)
诀窍:
题目若要计算DG,一般是恒温过程;
若不是恒温,题目必然会给出绝对熵S的值。
3.DA的计算
(1)恒温恒容不做非体积功可逆过程:
DA=0
(2)恒温:
DA=DU-TDS=DG-D(pV)
(3)非恒温过程:
DG=DU-DTS=DU-(T2S2-T1S1)=DU-(T2DS-S1DT)
诀窍:
题目若要计算DA,一般是恒温过程;
若不是恒温,题目必然会给出绝对熵。
1.
了解自发过程的共同特征;
2.
理解第二、第三定律的表述;
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 物理化学 知识点 总结
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 第二章-传统相机的性能与种类.ppt
第二章-传统相机的性能与种类.ppt
 三级健康管理师题库(附答案).docx
三级健康管理师题库(附答案).docx
 专业分包合同风险控制要点一览表 - 副本.rtf
专业分包合同风险控制要点一览表 - 副本.rtf
