 医疗器械临床试验基本文件目录(2016版)Word格式.doc
医疗器械临床试验基本文件目录(2016版)Word格式.doc
- 文档编号:13037563
- 上传时间:2022-10-03
- 格式:DOC
- 页数:3
- 大小:93KB
医疗器械临床试验基本文件目录(2016版)Word格式.doc
《医疗器械临床试验基本文件目录(2016版)Word格式.doc》由会员分享,可在线阅读,更多相关《医疗器械临床试验基本文件目录(2016版)Word格式.doc(3页珍藏版)》请在冰豆网上搜索。
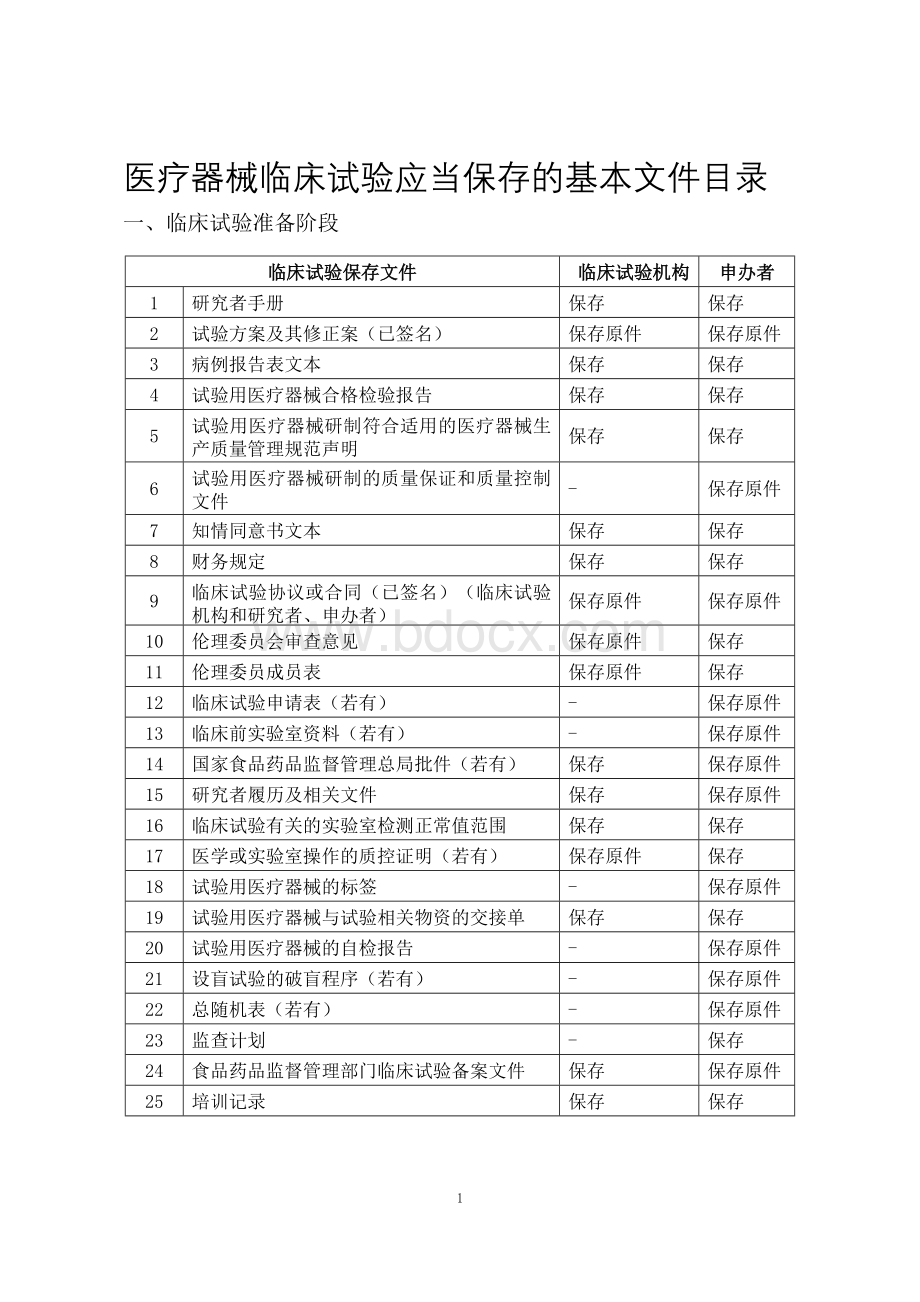
保存原件
3
病例报告表文本
4
试验用医疗器械合格检验报告
5
试验用医疗器械研制符合适用的医疗器械生产质量管理规范声明
6
试验用医疗器械研制的质量保证和质量控制文件
-
7
知情同意书文本
8
财务规定
9
临床试验协议或合同(已签名)(临床试验机构和研究者、申办者)
10
伦理委员会审查意见
11
伦理委员成员表
12
临床试验申请表(若有)
13
临床前实验室资料(若有)
14
国家食品药品监督管理总局批件(若有)
15
研究者履历及相关文件
16
临床试验有关的实验室检测正常值范围
17
医学或实验室操作的质控证明(若有)
18
试验用医疗器械的标签
?
19
试验用医疗器械与试验相关物资的交接单
20
试验用医疗器械的自检报告
21
设盲试验的破盲程序(若有)
22
总随机表(若有)
23
监查计划
24
食品药品监督管理部门临床试验备案文件
25
培训记录
二、临床试验进行阶段
26
研究者手册更新件(若有)
27
其他文件(方案、病例报告表、知情同意书、书面情况通知)的更新(若有)
28
医学、实验室检查,操作的正常值范围更新(若有)
29
30
监查员访视报告
31
已签名的知情同意书
32
原始医疗文件
33
病例报告表(已填写,签名,注明日期)
34
研究者对严重不良事件的报告(若有)
35
申办者对严重不良事件和可能导致严重不良事件的器械缺陷的报告(若有)
36
受试者鉴认代码表
37
受试者筛选表与入选表
38
研究者签名样张及研究者授权表
三、临床试验终止或者完成后
39
试验用医疗器械处理记录
40
完成试验受试者代码目录
41
监查、核查、检查记录
42
最终监查报告
43
治疗分配记录
44
破盲证明(若有)
45
临床试验小结或临床试验报告
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 医疗器械 临床试验 基本 文件 目录 2016
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 第二章-传统相机的性能与种类.ppt
第二章-传统相机的性能与种类.ppt
 三级健康管理师题库(附答案).docx
三级健康管理师题库(附答案).docx
 专业分包合同风险控制要点一览表 - 副本.rtf
专业分包合同风险控制要点一览表 - 副本.rtf
