 届高中化学专题04化学反应速率难点大串讲学案新人教版选修4.docx
届高中化学专题04化学反应速率难点大串讲学案新人教版选修4.docx
- 文档编号:12680698
- 上传时间:2023-04-21
- 格式:DOCX
- 页数:30
- 大小:2.10MB
届高中化学专题04化学反应速率难点大串讲学案新人教版选修4.docx
《届高中化学专题04化学反应速率难点大串讲学案新人教版选修4.docx》由会员分享,可在线阅读,更多相关《届高中化学专题04化学反应速率难点大串讲学案新人教版选修4.docx(30页珍藏版)》请在冰豆网上搜索。
届高中化学专题04化学反应速率难点大串讲学案新人教版选修4
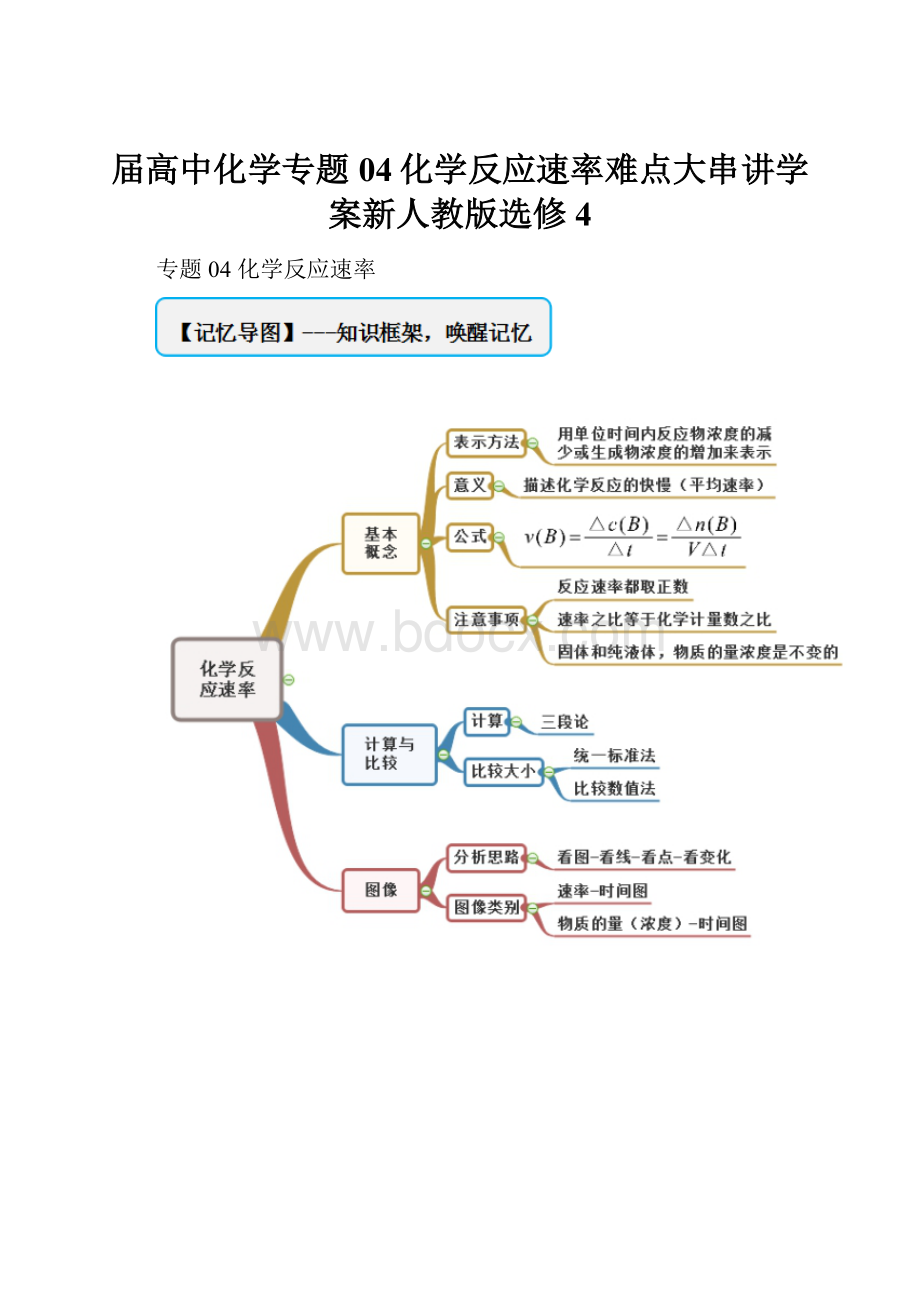
专题04化学反应速率
知识一化学反应速率理解
【例1】.下列对“化学反应速率”的理解正确的是()
A.化学反应速率表示的是化学反应进行的程度
B.化学反应速率可以用单位时间内反应物浓度的变化来表示
C.化学反应速率可以用任何一种反应物或生成物的浓度变化来表示
D.化学反应速率可以是正值,也可以是负值
【答案】B
【变式】1.下列关于化学反应速率的说法正确的是()
A.化学反应速率是指单位时间内任何一种反应物物质的量浓度的减少或任何一种生成物物质的量浓度的增加
B.化学反应速率为0.1mol·L-1·s-1是指1秒钟时某物质的浓度为0.1mol·L-1
C.根据化学反应速率的大小可以知道化学反应进行的快慢
D.对于任何化学反应来说,反应速率越快,反应现象就越明显
【答案】C
知识二化学反应速率的测定
【例2】某化学兴趣小组设计实验探究反应速率的测定和比较。
[实验目的]测定锌和稀硫酸反应的速率。
[实验用品]锥形瓶、双孔塞、分液漏斗、直角导管、50mL注射器、铁架台、秒表、锌粒、1mol·L-1硫酸、4mol·L-1硫酸。
[实验步骤]
(1)取一套装置(装置如图所示),加入40mL1mol·L-1的硫酸,测量收集10mLH2所需的时间。
(2)取另一套装置,加入40mL4mol·L-1的硫酸,测量收集10mLH2所需的时间。
[实验现象]锌跟硫酸反应________,收集10mL气体,
(2)所用时间比
(1)所用时间________。
[实验结果]
加入试剂
反应时间
反应速率
40mL1mol·L-1硫酸
40mL4mol·L-1硫酸
[实验结论]4mol·L-1硫酸与锌反应比1mol·L-1硫酸与锌反应速率________。
[注意事项]
(1)锌粒的颗粒(即表面积)大小________;
(2)40mL的硫酸要迅速加入;
(3)装置________,且计时要迅速准确;
(4)气体收集可以用排水量气装置(如图)代替。
[实验讨论]除本实验测定反应速率的方法外,可行的方案还有(至少填两条):
①________________________________________________________________________,
②________________________________________________________________________,
③________________________________________________________________________,
④________________________________________________________________________。
【答案】
[实验现象]产生气泡短
[实验结果]长小短大
[实验结论]大
[注意事项]
(1)基本相同(3)气密性良好
[实验讨论]①测定单位时间内产生H2的体积;②测定一段时间内H+的浓度变化
③测定一段时间内Zn粒质量变化(答两条即可)
①测定单位时间内产生H2的体积
②测一段时间内H+的浓度变化
③测一段时间内Zn粒质量的变化
【变式】1.化学反应速率是通过实验测定的,测量下列化学反应的速率时,测量依据不合理的是()
选项
化学反应
测量依据(单位时间内)
A
CO(g)+H2O(g)===CO2(g)+H2(g)
压强变化
B
Zn+H2SO4===ZnSO4+H2↑
H2体积
C
2NO2(g)
N2O4(g)
颜色深浅
D
Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
沉淀质量
【答案】A
2.下列都是测定气体产物(一定时间内)反应速率的装置图,不能达到目的的是()
【答案】AD
【解析】A装置不能用长颈漏斗,D装置产生的CO2能被Na2CO3溶液吸收。
知识三化学反应速率的计算和比较
【例3-1】.在2L密闭容器内,某气体反应物在2s内由8mol变为7.2mol,则用该气体表示该反应的平均反应速率为()
A.0.4mol·L-1·s-1B.0.3mol·L-1·s-1
C.0.2mol·L-1·s-1D.0.1mol·L-1·s-1
【答案】C
【解析】用该气体表示反应的平均反应速率为v=
=
=0.2mol·L-1·s-1,C正确。
【变式】1.在2L的密闭容器中,发生反应3A(g)+B(g)2C(g),若最初加入的A和B都是4mol,测得10s内A的平均速率v(A)=0.12mol·L-1·s-1,则反应进行到10s时容器中B的物质的量是()
A.1.6molB.2.8mol
C.3.2molD.3.6mol
【答案】C
2.在可逆反应2A(g)+3B(g)
xC(g)+D(g)中,已知:
反应开始加入的物质只有A、B,起始浓度A为5mol·L-1,B为3mol·L-1,前2minC的平均反应速率为0.5mol·L-1·min-1,2min后,测得D的浓度为0.5mol·L-1,则关于此反应的下列说法中正确的是()
A.2min末时A和B的浓度之比为5∶3
B.x=1
C.2min末时B的浓度为1.5mol·L-1
D.2min末时A消耗的浓度为0.5mol·L-1
【答案】C
【解析】依题意2min末c(C)=0.5mol·L-1·min-1×2min=1mol·L-1,而c(D)=0.5mol·L-1,所以x=2。
2A(g)+3B(g)2C(g)+D(g)
c(起始)/mol·L-15300
c(变化)/mol·L-111.510.5
c(2min末)/mol·L-141.510.5
可知C正确。
3.在一定温度下,向一个2L的真空密闭容器中(预先装入催化剂)通入1molN2和3molH2,经过一段时间后,测得容器内压强是起始时的0.9倍。
在此时间段内H2的平均反应速率为0.1mol·L-1·min-1,则经过时间为()
A.2minB.3minC.4minD.5min
【答案】B
【例3-2】
(1)可逆反应2A+3B
2C+D相同条件下的反应速率,反应速率最快的是()
A.v(A)=0.5mol/(L·min)B.v(B)=0.01mol/(L·s)
C.v(C)=0.35mol/(L·min)D.v(D)=0.4mol/(L·min)
【答案】D
【解析】如果都用物质B表示反应速率,根据反应速率之比是化学计量数之比可知选项A~D分别是[mol/(L·min)]0.75、0.6、0.525、1.2,因此反应速率最快的是选项D,答案选D。
(2)已知4NH3+5O2⇌4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,正确的关系是()
A.4vNH3)=5vO2)B.6vO2)=5vH2O)
C.4vNH3)=6vH2O)D.5vO2)=4v(NO)
【答案】B
答案选B。
【变式】1.反应A(g)+3B(g)
2C(g)+2D(g)在四种情况下的反应速率分别为①ν(A)=0.25mol/(L·s)②ν(B)=27mol/(L·min)③ν(C)=0.4mol/(L·s)④ν(D)=36mol/(L·min)。
下列选项正确的是
A.④>①>③>②B.③<②<④<①
C.①>②>③>④D.④>②>③>①
【答案】A
2.在不同条件下分别测得反应2SO2(g)+O2(g)
2SO3(g)的化学反应速率,其中表示该反应进行的最快的是()
A.v(SO2)=4mol·L-1·min-1B.v(O2)=3mol·L-1·min-1
C.v(SO2)=0.1mol·L-1·s-1D.v(O2)=0.1mol·L-1·s-1
【答案】D
【解析】比较:
必须统一标准。
换算成同一物质进行比较是关键,本题首先需要统一单位。
【例3-3】已知:
反应aA(g)+bB(g)
cC(g),某温度下,在2L的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
(1)从反应开始到12s时,用A表示的反应速率为________________。
(2)经测定前4s内v(C)=0.05mol·L-1·s-1,则该反应的化学方程式为___________________。
(3)请在图中将生成物C的物质的量浓度随时间的变化曲线绘制出来。
(4)若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为甲:
v(A)=0.3mol·L-1·s-1;乙:
v(B)=0.12mol·L-1·s-1;丙:
v(C)=9.6mol·L-1·min-1;
则甲、乙、丙三个容器中反应速率由快到慢的顺序为________________________。
【答案】
(1)0.05mol·L-1·s-1
(2)3A(g)+B(g)
2C(g)(3)
(4)乙>甲>丙
(3)生成物C的浓度从0开始增加,到12s时达到最大,Δc(A)∶Δc(C)=a∶c=3∶2,所以Δc(C)=2×
=0.4mol·L-1。
(4)丙容器中v(C)=9.6mol·L-1·min-1=0.16mol·L-1·s-1,则甲容器中
=
=0.1mol·L-1·s-1,乙容器中
=
=0.12mol·L-1·s-1,丙容器中
=
=0.08mol·L-1·s-1,故甲、乙、丙三个容器中反应速率由快到慢的顺序为乙>甲>丙。
【变式】1.一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是()
A.该反应的化学方程式为3B+4D
6A+2C
B.反应进行到1s时,v(A)=v(D)
C.反应进行到6s时,B的平均反应速率为0.05mol·L-1·s-1
D.反应进行到6s时,各物质的反应速率相等
【答案】C
2.一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示。
下列叙述正确的是()
A.反应开始到10s末时,用Z表示的反应速率为0.158mol·L-1·s-1
B.反应开始到10s末时,X的物质的量浓度减少了0.79mol·L-1
C.反应开始到10s时,Y的转化率为79.0%
D.反应的化学方程式为X(g)+Y(g)
Z(g)
【答案】C
【解析】分析图象,关键是看变化量和走势,从走势分析X、Y是反应物,Z是生成物,初步分析它们的变化量分别为Δn(X)=1.20mol-0.41mol=0.79mol,Δn(Y)=1.0mol-0.21mol=0.79mol,Δn(Z)=1.58mol,首先确定该反应的化学方程式为X(g)+Y(g)===2Z(g)。
据选项要求分别计算出v(Z)=
=0.079mol·L-1·s-1;Δc(X)=
=0.395mol·L-1;α(Y)=
×100%=79%,只有C选项正确。
3.在373K时,把0.5molN2O4通入体积为5L的恒容真空密闭容器中,立即出现红棕色气体。
反应进行到2s时,NO2的浓度为0.02mol·L-1。
在60s时,体系达到平衡状态,此时容器内的压强为开始时的1.6倍。
下列说法错误的是()
A.前2s以N2O4的浓度变化表示的平均反应速率为0.005mol·L-1·s-1
B.在2s时体系内的压强为开始时的1.1倍
C.平衡时体系内含N2O40.2mol
D.平衡时,N2O4的转化率为40%
【答案】D
60s时达到平衡,此时容器内的压强为开始时的1.6倍,由上述分析可得平衡时总物质的量n=0.8mol,设容器内n(N2O4)=xmol,则生成n(NO2)=2(0.5-x)mol,即xmol+2(0.5-x)mol=0.8mol,x=0.2mol,所以C正确;D、平衡时,N2O4的转化率=
×100%=60%,所以D错误。
本题正确答案为D。
1.对于反应:
CaCO3+2HCl===CaCl2+H2O+CO2↑,下列说法正确的是()
A.用HCl和CaCl2表示的反应速率数值不同,但所表示的意义相同
B.不能用CaCO3的浓度变化来表示反应速率,但可用水来表示
C.用H2O和CO2表示的化学反应速率相同
D.用CaCl2浓度的减小表示其反应速率
【答案】A
【解析】因为CaCO3是固体,H2O为纯液体,不能用其浓度的变化来表示化学反应速率;D中CaCl2为生成物,故应用其浓度的增加来表示反应速率,故B、C、D项错误;在同一反应中,选用不同的物质表示反应速率,反应速率数值之比等于化学方程式中化学计量数之比,数值可能相同,也可能不同,但意义相同,故A项正确。
2.在四个不同的容器中,在不同的条件下进行合成氨反应:
N2+3H2
2NH3。
根据在相同时间内测定的结果判断,生成氨的速率最快的是
A.v(H2)=0.1mol·L−1·min−1B.v(N2)=0.2mol·L−1·min−1
C.v(NH3)=0.15mol·L−1·min−1D.v(H2)=0.3mol·L−1·min−1
【答案】B
3.反应4A(s)+3B(g)===2C(g)+D(g),经2min,B的浓度减少0.6mol·L-1。
对此反应速率的表示正确的是()
A.用A表示的反应速率是0.4mol·L-1·min-1
B.分别用B、C、D表示的反应速率之比是3∶2∶1
C.在2min末的反应速率,用B表示是0.3mol·L-1·min-1
D.在2min内的反应速率,用C表示是0.3mol·L-1·min-1
【答案】B
【解析】固体A不具有浓度概念,该物质的反应不能用mol·L-1·min-1的单位来表示。
4.2molA与2molB混合于2L的密闭容器中,发生如下反应:
2A(g)+3B(g)
2C(g)+zD(g)
若2s后,A的转化率为50%,测得v(D)=0.25mol·L-1·s-1,下列推断正确的是()
A.v(C)=v(D)=0.2mol·L-1·s-1B.z=3
C.B的转化率为75%D.反应前与2s后容器的压强比为4∶3
【答案】C
【解析】A的起始量为2mol,转化50%即转化1mol,根据反应关系知B转化1.5mol,C生成1mol,又因为v(D)=0.25mol·L-1·s-1,可计算出2s时D的生成量为0.25mol·L-1·s-
1×2L×2s=1mol,故知z=2,B错;v(C)=v(D)=v(A)=0.25mol·L-1·s-1,故A错;B的转化率为
×100%=75%,C正确;反应达2s时,容器内总物质的量为nA+nB+nC+nD=1mol+0.5mol+1mol+1mol=3.5mol。
故反应前后的容器中气体总物质的量之比为4∶3.5,压强比为4∶3.5,D错。
5.在四种不同条件下测得反应2SO2+O2
2SO3的反应速率如下表所示:
编号
(1)
(2)
(3)
(4)
反应速率
[mol/(L·min)]
v(SO2)
v(O2)
v(SO3)
v(O2)
0.4
0.25
0.5
0.3
其中反应速率最快的是()
A.
(1)B.
(2)
C.(3)D.(4)
【答案】D
6.将4molA气体和2molB气体置于2L密闭容器中,混合后发生如下反应:
2A(g)+B(g)⇌2C(g)+D(s),若经2s后测得C的浓度为0.6mol•L-1,下列说法正确的是()
A.用物质A表示的反应速率为0.6mol(L•s)-1B.2s时物质B的含量为23.3%
C.2s时物质A的转化率为30%D.2s时物质B的浓度为0.3mol•L-1
【答案】C
【解析】起始A的浓度为
=2mol/L,B的浓度为
=1mol/L,经2s后侧得C的浓度为0.6mol•L-1,
2A(g)+B(g)
2C(g),
起始(mol/L)210
变化(mol/L)0.60.30.6
2s时(mol/L)1.40.70.6
A、2s内,用物质A表示的反应的平均速率为v(A)=
=0.3mol•L-1•s-1,故A错误;B、2s时物质B的含量未注明是物质的量含量还是质量含量,无法计算,故B错误;C、2s时物质A的转化率为α=
×100%=30%,故C正确;D、2s时物质B的浓度为1mol/L-0.3mol/L=0.7mol•L-1,故D错误;故选C。
7.将N2和H2的混合气体分别充入甲、乙、丙三个容器中进行合成氨反应,经过一段时间后反应速率为:
v甲(H2)=3mol·L-1·min-1,v乙(N2)=2mol·L-1·min-1,v丙(NH3)=1mol·L-1·min-1。
这段时间内三个容器中合成氨的反应速率的大小关系为()
A.v甲>v乙>v丙B.v乙>v甲>v丙
C.v甲>v丙>v乙D.v甲=v乙=v丙
【答案】B
【解析】根据反应N2+3H22NH3,
v甲(H2)=1mol·L-1·min-1;v乙(N2)=2mol·
L-1·min-1;
v丙(NH3)=0.5mol·L-1·min-1,数值大者速率大,即v乙>v甲>v丙。
8.一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是()
A.该反应的化学方程式为3B+4D
6A+2C
B.反应进行到1s时,v(A)=v(D)
C.反应进行到6s时,B的平均反应速率为0.05mol·L-1·s-1
D.反应进行到6s时,各物质的反应速率相等
【答案】C
9.向某密闭容器中加入0.3molA、0.1molC和一定量的B三种气体,一定条件下发生如下反应:
3A(g)
B(g)+2C(g),各物质的浓度随时间变化如图所示[t0~t1阶段的c(B)变化未画出]。
下列说法中正确的是()
A.若t1=15s,则用A的浓度变化表示t0~t1阶段的平均反应速率为0.004mol·L-1·s-1
B.t1时该反应达到平衡,A的转化率为60%
C.该容器的容积为2L,B的起始的物质的量为0.02mol
D.t0~t1阶段,此过程中容器与外界的热交换总量为akJ,该反应的热化学方程式为3A(g)
B(g)+2C(g)ΔH=-50akJ·mol-1
【答案】B
50a/3kJ,即3A(g)
B(g)+2C(g)ΔH=-50a/3kJ·mol-1,D错误;正确选项B。
10.一定温度下,A、B、C三个容器中均进行同一个反应:
N2(g)+3H2(g)
2NH3(g)ΔH=-QkJ·mol-1,在相同的时间段内,测得如下数据:
容器
A
B
C
反应速率/mol·L-1·min-1
v(H2)=3
v(N2)=3
v(NH3)=4
则三个容器放出的热量Q的大小关系为()
A.B>C>AB.A>B>CC.C>A>BD.B>A>C
【答案】A
【解析】合成氨是放热反应,即Q>O,化学反应速率的定义单位时间内反应物浓度的减少或生成物浓度的增加量,因为是相同的时间段,假设时间为1min,容器体积为1L,以N2为基准,A容器,N2浓度变化为3/3mol·L-1=1mol·L-1,放出的热量为QkJ,B容器,N2浓度变化为3mol·L-1,放出的能量为3QkJ,C容器,N2浓度变化为4/2mol·L-1=2mol·L-1,放出的热量为2QkJ,因此放出热量的顺序是B>C>A,故A正确。
11.化学实验是进行化学研究的有效方法,请回答下列实验中的有关问题。
I.用如图所示的装置测定中和热。
实验药品:
100mL0.50mol‧L-1盐酸、100mL0.55mol‧L-1NaOH溶液。
实验步骤:
略。
回答下列问题:
(1)从实验装置上看,还缺少环形玻璃搅拌棒,该装置的作用是____________;有同学提议可以用铜质搅拌棒替代,你是否赞同(说明理由)________________。
(2)你认为该实验成功的关键是______________________________。
II.影响化学反应速率的因素很多,某校课外兴趣小组用实验的方法进行探究。
甲、乙两个兴趣小组利用Mg、Fe、Cu和不同浓度的硫酸(0.5mol‧L-1、2mol‧L-1、18.4mol‧L-1),设计实验方案来研究影响反应速率的因素。
(1)请帮助甲小组完成研究的实验报告:
实验步骤
现象
结论
①分别取等体积0.5mol‧L-1硫酸于试管中
②分别投入大小、形状相同的Mg、Fe、Cu
③观察金属表面产生气体的快慢
①产生气体的速率Mg>Fe
②Cu上无气体产生
_________
根据控制变量法,要得出正确的实验结论,在实验过程中需要保持温度和压强相同。
(2)乙小组为了更精确地研究浓度对反应速率的影响,利用右图装置进行定量实验。
该小组选用的实验药品是:
Fe、2mol‧L-1硫酸和______mol‧L-1硫酸。
【答案】搅拌(将溶液混合均匀)不赞同,铜质搅拌棒易散热,使实验误差增大减少中和热的损失金属性越强的金属单质与稀硫酸反应的速率越快(合理答案可给分)0.5
(2)该实验成功的关键是:
减少热量的损失。
II.
(1)结论:
金属性越强的金属单质与稀硫酸反应的速率越快(合理答案可给分)。
(2)该小组选用的实验药品是:
Fe、2mol‧L-1硫酸和0.5mol‧L-1硫酸。
铁在浓硫酸中被钝化,所以不可选用浓硫酸。
12.在容积为2L的密闭容器中进行如下反应:
A(g)+2B(g)
3C(g)+nD(g)。
开始时A为4mol,B为6mol;5min末时C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol/(L·min)。
计算:
(1)5min末A的物质的量浓度为_________。
(2)前5min内化学反应速率v(B)为_________。
(3)化学方程式中n值为_________。
(4)此反应在四种不同情况下的反应速率分别为:
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高中化学 专题 04 化学反应 速率 难点 串讲 新人 选修
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《阿凡达》观后感.docx
《阿凡达》观后感.docx
