 中考一模化学试题含答案.docx
中考一模化学试题含答案.docx
- 文档编号:1233034
- 上传时间:2022-10-19
- 格式:DOCX
- 页数:34
- 大小:464.78KB
中考一模化学试题含答案.docx
《中考一模化学试题含答案.docx》由会员分享,可在线阅读,更多相关《中考一模化学试题含答案.docx(34页珍藏版)》请在冰豆网上搜索。
中考一模化学试题含答案
2020-2021年中考一模化学试题(含答案)
一、选择题(培优题较难)
1.在托盘天平(灵敏度极高)两边各放一只等质量的烧杯,在两只烧杯里各加入足量、等质量、等质量分数的稀盐酸,调节天平至平衡,然后向左端烧杯加入5.6克铁,要使天平再次平衡,应向右边烧杯加入
A.5.4克氧化钙B.5.6克铜C.6克镁D.10克碳酸钙
【答案】A
【解析】天平的两边增加的量相同时天平才能仍然平衡。
5.6克铁和足量的盐酸反应生成0.2g氢气,氧化钙和盐酸反应生成盐和水,没有气体逸出,增加的量为5.4g,天平平衡;5.6g铜和酸不反应,增加的量为5.6g;6g镁和酸反应生成气体0.5g;增加5.5g;10g碳酸钙和足量的酸反应生成二氧化碳4.4g,增加5.6g;选A
点睛:
天平的平衡问题的关键是余下的物质一样多,天平平衡。
2.有一包固体粉末,可能含碳、铝、铜、氧化铝、氧化铜中的一种或几种。
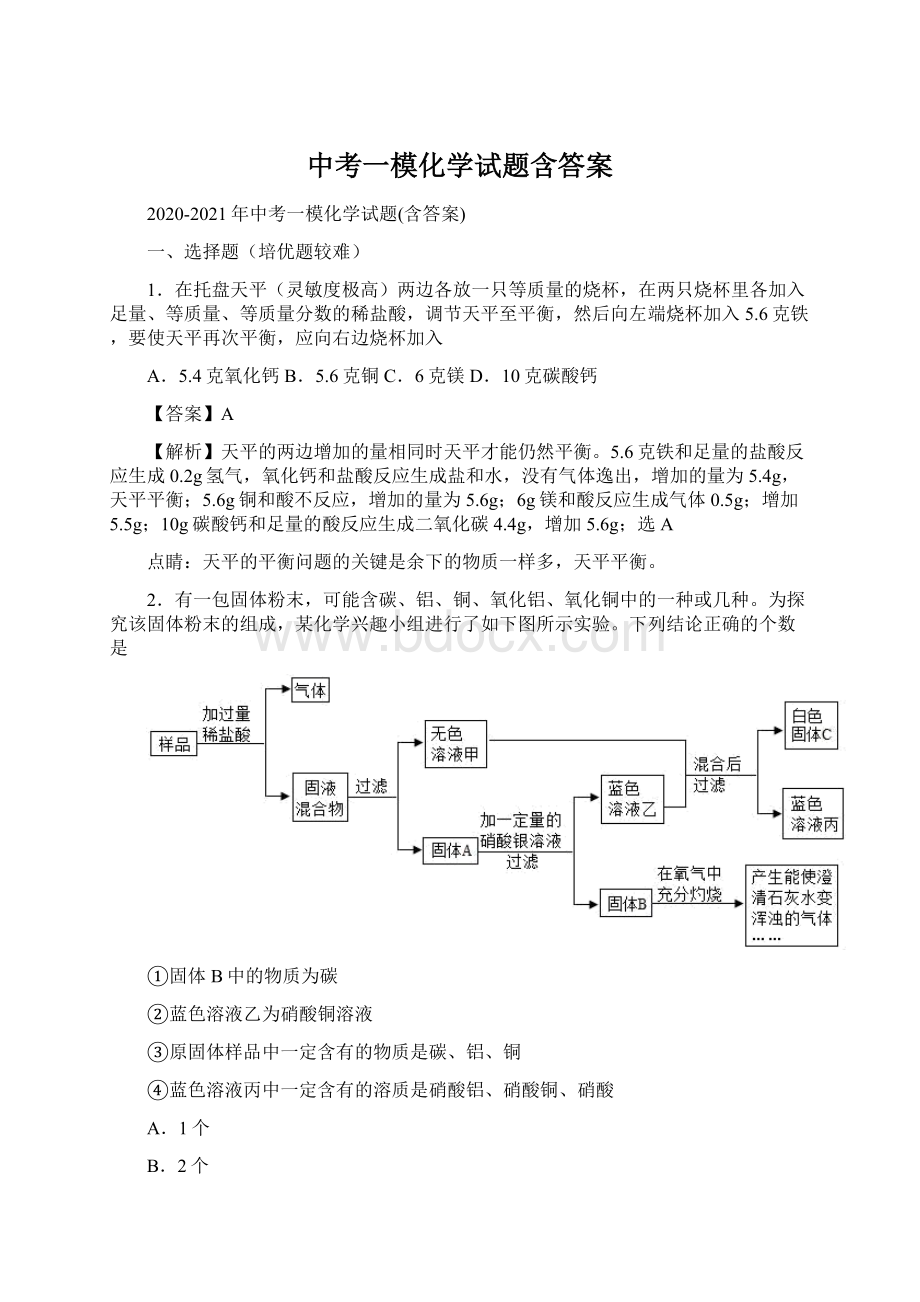
为探究该固体粉末的组成,某化学兴趣小组进行了如下图所示实验。
下列结论正确的个数是
①固体B中的物质为碳
②蓝色溶液乙为硝酸铜溶液
③原固体样品中一定含有的物质是碳、铝、铜
④蓝色溶液丙中一定含有的溶质是硝酸铝、硝酸铜、硝酸
A.1个
B.2个
C.3个
D.4个
【答案】B
【解析】
【详解】
①固体B在氧气中充分灼烧,生成能使澄清石灰水变浑浊的二氧化碳气体(说明原固体有碳),可能还含有铜,故该说法不正确;
②无色溶液甲与蓝色溶液乙反应生成白色固体,说明蓝色溶液乙中含有硝酸银,故该说法不正确;
③向样品中加入过量稀盐酸有气体生成,根据金属活动性顺序可知,是铝与盐酸反应,生成的气体是氢气;固体A与硝酸银反应有蓝色溶液生成,说明固体A中含有铜,铜与硝酸银反应生成银和硝酸铜,反应的化学方程式为;铜与硝酸银反应生成银;固体B在氧气中充分灼烧,生成能使澄清石灰水变浑浊的气体,该气体是二氧化碳。
灼烧能生成二氧化碳气体的物质是碳,故固体B中含有的物质是碳、银(或C、Ag);样品中加过量稀盐酸有气体产生,说明原固体中有铝;将反应后的固液混合物过滤,得到无色溶液甲(说明原固体中没有氧化铜)和固体A,固体A加一定量的硝酸银溶液并过滤,得到蓝色溶液乙(说明原固体中有铜)和固体B;固体B在氧气中充分灼烧,生成能使澄清石灰水变浑浊的二氧化碳气体(说明原固体有碳)。
故原固体样品中一定含有的物质是碳、铝、铜(或C、A1、Cu),故该说法正确;
④无色溶液甲与蓝色溶液乙反应生成白色固体,说明蓝色溶液乙中含有硝酸银,无色溶液甲中溶质是盐酸及盐酸与铝反应生成的氯化铝。
盐酸与硝酸银反应生成氯化银和硝酸,氯化铝与硝酸银反应生成氯化银和硝酸铝,蓝色溶液乙中的溶质硝酸铜不参与反应。
故蓝色溶液丙中一定含有的溶质是硝酸铝、硝酸铜和硝酸(或Al(NO3)3、Cu(NO3)2、HNO3),故该说法正确;
正确的说法有:
③④;故选:
B。
3.下列各组物质在溶液中能大量共存,且溶液呈无色的是()
A.Na2CO3、NH4NO3、Ca(OH)2
B.Fe2(SO4)3、Na2SO4、Mg(NO3)2
C.AlCl3、Ba(NO3)2、CaCl2
D.Na2CO3、AgNO3、BaCl2
【答案】C
【解析】
A、Ca(OH)2和Na2CO3能生成白色沉淀碳酸钙,不能大量共存;NH4NO3、Ca(OH)2会生成氨气和水,不能大量共存,B、三者之间不反应,能大量共存,但Fe2(SO4)3溶于水呈黄色;C、三者之间不反应,能大量共存,且符合无色透明的要求;D、AgNO3、BaCl2反应生成氯化银白色沉淀,不能大量共存;Na2CO3、BaCl2能生成碳酸钡白色沉淀,不共存。
故选C.
点睛:
熟记常见沉淀:
碳酸钙、碳酸钡、氯化银、硫酸钡、氢氧化镁,氢氧化铜,氢氧化铁等;常见溶液的颜色:
含亚铁离子时溶液为浅绿色;含铁离子时溶液为黄色;含铜离子时溶液为蓝色。
4.某同学将mgMg、A1、Zn、Fe的混合物放入足量的稀盐酸中,充分反应后,将所得溶液小心蒸干,得到(m+7.1)g不含结晶水的固体,则m的取值范围是
A.2.4≤m≤6.5
B.2.4 C.1.8≤m≤6.5 D.1.8 【答案】D 【解析】 【分析】 【详解】 将mgMg、A1、Zn、Fe的混合物放入足量的稀盐酸中,充分反应后,将所得溶液小心蒸干,得到(m+7.1)g不含结晶水的固体,该不含结晶水的固体是由金属离子(Mg2+、A13+、Zn2+、Fe2+)和Cl-组成的。 根据质量守恒定律可知: 不含结晶水的固体中含有Cl-的质量为(m+7.1)g-mg=7.1g。 则该反应消耗稀盐酸的质量为: 7.1g÷=7.3g。 假设分别为四种金属单质与等量的稀盐酸反应,则 由计算可知,若为四种金属单质与等量的稀盐酸反应时,m最大值为6.5g,最小值为1.8g,而该物质为混合物,故m的最大值应小于6.5g,最小值应大于1.8g,故选D。 5.为了除去粗盐中的Ca2+、Mg2+、SO42﹣及泥砂,可将粗盐溶于水,然后进行下列五项操作①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液.下列操作顺序中最合适的是() A.②④⑤①③B.⑤④②③①C.⑤②④③①D.②⑤④①③ 【答案】D 【解析】 试题分析: 镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可以将镁离子沉淀,硫酸根离子用钡离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀,至于先除镁离子,还是先除硫酸根离子都行,钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,离子都沉淀了,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,所以正确的顺序为: ⑤加过量的BaCl2溶液,④加过量的Na2CO3溶液,②加过量的NaOH溶液,①过滤,③加适量的盐酸;或者,②加过量的NaOH溶液,⑤加过量的BaCl2溶液,④加过量的Na2CO3溶液,①过滤,③加适量的盐酸.所以正确的顺序是⑤④②①③或②⑤④①③ 故选D. 考点: 氯化钠与粗盐提纯;物质除杂或净化的探究;实验步骤的探究. 点评: 在解此类题时,注意除杂的最后不能再有其他杂质,过滤要放在所有沉淀步骤的最后. 6.童童同学将一定量的氧化铜粉末加入到100g溶质的质量分数为14%的稀硫酸中,充分反应后固体全部消失,为了避免该废液排放造成污染,他又向废液中加入20g铁粉,充分反应后过滤,滤渣的质量为20g,加稀硫酸时所消耗的氧化铜质量是() A.8gB.10gC.12gD.14g 【答案】B 【解析】 【分析】 要使加入的铁粉和得到的固体质量相等必须使硫酸消耗多余的Fe: 从CuSO4+Fe=FeSO4+Cu,可以看出铁转化出铜,这是一个使固体质量增加的过程,而题目明确的说明过滤后的固体质量与投入的铁粉质量相同,这只能说明氧化铜被溶解后,硫酸仍然有剩余,剩余的硫酸继续消耗铁粉,且消耗铁粉的质量与前一步固体增加的质量相等;利用这一等量关系,计算所加入氧化铜的质量; 【详解】 设原先氧化铜的质量为,则与氧化铜反应的硫酸的质量,生成硫酸铜的质量, = =2 设加入铁粉与硫酸铜溶液充分反应固体增加的质量为,生成硫酸亚铁的质量为;与剩余稀硫酸反应的铁的质量为,生成硫酸亚铁的质量为, =0.1 =8-0.7 反应前后固体质量不变,即与硫酸反应消耗铁的质量等于与硫酸铜反应固体增加的质量,即: = 0.1=8-0.7解得=10g, 答: 原先氧化铜的质量为10g。 故选B。 【点睛】 在金属活动性顺序里,位于氢前面的金属能置换出盐酸、稀硫酸中的氢;位于前面的金属能把位于后面的金属置换出来。 7.推理是化学学习中常用的思维方法,下列推理正确的是 A.铁能将铜从硫酸铜溶液中置换出来,因此银也能将铜从硫酸铜溶液中置换出来 B.物质燃烧需要同时满足三个条件,因此灭火也需要同时破坏这三个条件 C.碱溶液的pH>7,因此测得某溶液的pH=12,该溶液一定是碱溶液 D.NaOH溶液中OH﹣能与酸反应,因此KOH溶液中的OH﹣也能与酸反应 【答案】D 【解析】A.金属活动顺序表: KCaNaMgAlZnFeSnPbHCuHgAgPtAu,金属的位置越靠前,金属的活动性越强。 位置靠前的金属能将位于其后的金属从它的盐溶液中置换出来。 铁在铜前,所以铁能将铜从硫酸铜溶液中置换出来,银在铜后,因此银不能将铜从硫酸铜溶液中置换出来;B.物质燃烧需要同时满足三个条件,因此灭火时只需要破坏一个条件就能到达灭火的目的;C.碱溶液的pH>7,如测得某溶液的pH=12,该溶液一定是碱性溶液,但不一定是碱的溶液;D.溶液的化学性质是由溶质溶于水产生的离子决定的,同样的微粒决定同样的性质。 NaOH溶液中OH﹣能与酸反应,因此KOH溶液中的OH﹣也能与酸反应,选D 点睛: 1、溶液的性质决定于溶液中的溶质产生的微粒。 2、熟记金属活动顺序表及其三个意义 8.某同学进行了煅烧石灰石的实验,过程如下(假设杂质不发生变化,酒精喷灯中的燃料是酒精C2H5OH)。 相关说法正确的是 A.步骤Ⅰ可证明煅烧石灰石的产物中有二氧化碳 B.步骤Ⅱ、Ⅲ可证明煅烧石灰石的产物中有氧化钙 C.白色固体M是氢氧化钙和碳酸钙的混合物 D.白色固体M中钙元素的质量等于煅烧前石灰石中钙元素的质量 【答案】B 【解析】 A、由于酒精燃烧生成了二氧化碳,该实验澄清的石灰水变浑浊不能证明煅烧石灰石的产物中有二氧化碳;B、由于氧化钙能与水化合生成了氢氧化钙,氢氧化钙溶液显碱性,能使酚酞试液变红色;C、由于石灰石中含有杂质,白色固体M中含有氢氧化钙和杂质,可能含有碳酸钙;D、由于氧化钙能与水化合生成了氢氧化钙,氢氧化钙微溶于水,白色固体M中钙元素的质量小于煅烧前石灰石中钙元素的质量.故选B. 点睛: 分析反应后的成分是,除考虑生成物外,还要考虑反应物是否有剩余。 反应前后元素的种类质量不变。 9.有一镁的合金2.4g,在合金中加入100g一定溶质质量分数的稀盐酸后,金属与稀盐酸恰好完全反应,产生氢气的质量为m,下列说法错误的是() A.若是镁铝合金,则m>0.2g B.若是镁铁合金,m=0.16g,则合金中铁的质量分数是50% C.若是镁铜合金,则稀盐酸溶质的质量分数小于7.3% D.若是镁锌合金,则m<0.2g 【答案】B 【解析】 镁、铝、锌、铁和稀盐酸反应的化学方程式及其反应物、生成物之间的质量关系为: Mg+2HCl═MgCl2+H2↑,2Al+6HCl═2AlCl3+3H2↑,Zn+2HCl═ZnCl2+H2↑, 24 73 2 54 219 6 65 73 2 Fe+2HCl═FeCl2+H2↑, 56 73 2 A、2.4g镁和稀盐酸完全反应生成0.2g氢气,2.4g铝和稀盐酸完全反应生成的氢气质量大于0.2g,因此若是镁铝合金,则m>0.2g,正确; B、如果合金中铁的质量分数是50%,则铁和镁的质量都是1.2g,1.2g镁和稀盐酸反应生成氢气质量是0.1g,1.2g铁和稀盐酸反应生成氢气质量为: 1.2g×2÷56=0.04g,合金中铁的质量分数是50%时,反应生成氢气质量为: 0.1g+0.04g=0.14g,错误;C、铜不能和稀盐酸反应,2.4g镁和稀盐酸完全反应需要氯化氢质量是7.3g,而混合物中的镁质量小于2.4g,因此消耗氯化氢的质量小于7.3g,即若是镁铜合金,则稀盐酸溶质的质量分数小于7.3%,正确;D、2.4g镁和稀盐酸完全反应生成0.2g氢气,2.4g锌和稀盐酸完全反
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 中考 化学试题 答案
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 转基因粮食的危害资料摘编Word下载.docx
转基因粮食的危害资料摘编Word下载.docx
