 课堂版高中毕业会考化学实验考查.docx
课堂版高中毕业会考化学实验考查.docx
- 文档编号:12320127
- 上传时间:2023-04-18
- 格式:DOCX
- 页数:9
- 大小:18.77KB
课堂版高中毕业会考化学实验考查.docx
《课堂版高中毕业会考化学实验考查.docx》由会员分享,可在线阅读,更多相关《课堂版高中毕业会考化学实验考查.docx(9页珍藏版)》请在冰豆网上搜索。
课堂版高中毕业会考化学实验考查
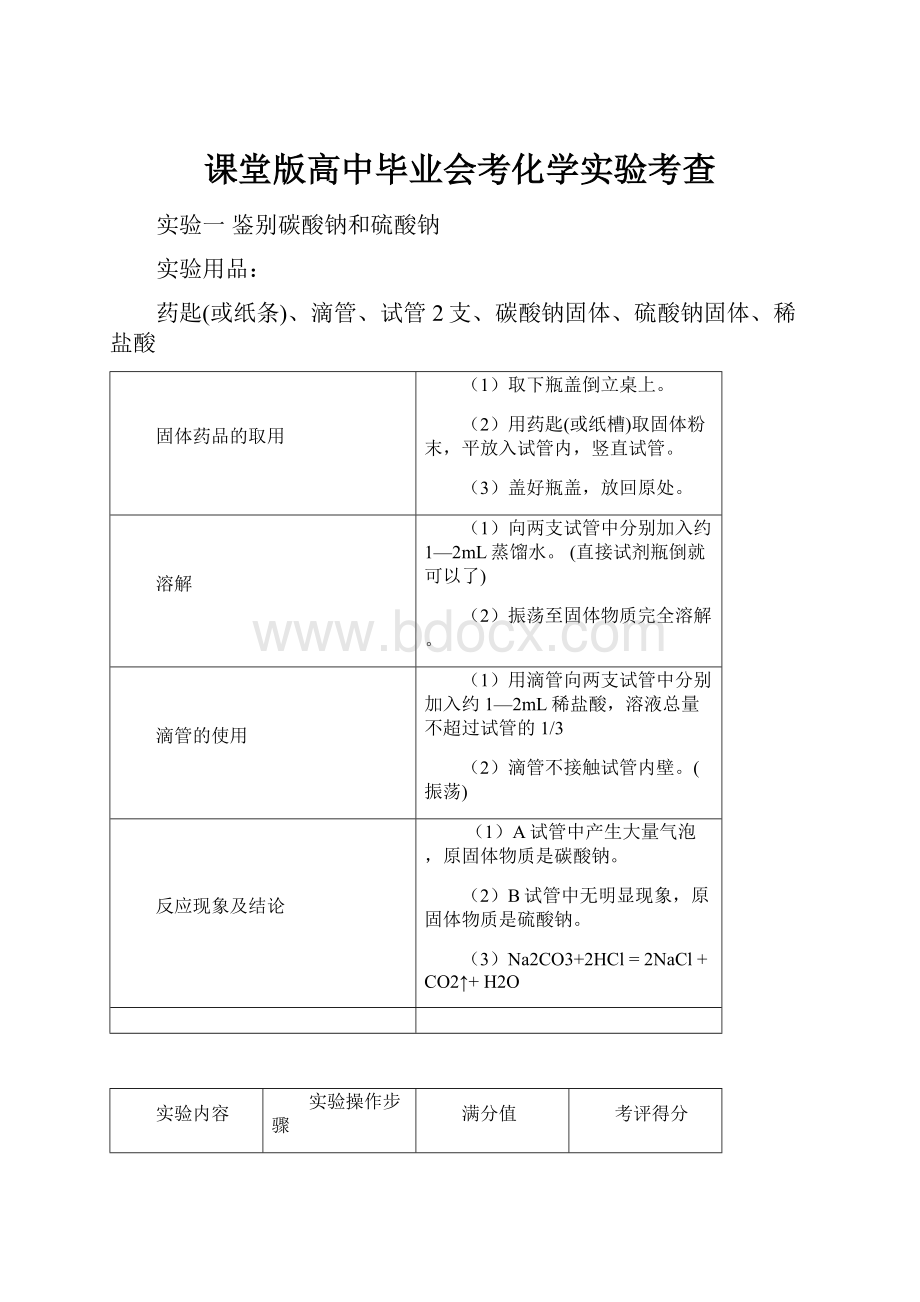
实验一鉴别碳酸钠和硫酸钠
实验用品:
药匙(或纸条)、滴管、试管2支、碳酸钠固体、硫酸钠固体、稀盐酸
固体药品的取用
(1)取下瓶盖倒立桌上。
(2)用药匙(或纸槽)取固体粉末,平放入试管内,竖直试管。
(3)盖好瓶盖,放回原处。
溶解
(1)向两支试管中分别加入约1—2mL蒸馏水。
(直接试剂瓶倒就可以了)
(2)振荡至固体物质完全溶解。
滴管的使用
(1)用滴管向两支试管中分别加入约1—2mL稀盐酸,溶液总量不超过试管的1/3
(2)滴管不接触试管内壁。
(振荡)
反应现象及结论
(1)A试管中产生大量气泡,原固体物质是碳酸钠。
(2)B试管中无明显现象,原固体物质是硫酸钠。
(3)Na2CO3+2HCl=2NaCl+CO2↑+H2O
实验内容
实验操作步骤
满分值
考评得分
固体药品的取用
用药匙分别取少量碳酸钠和硫酸钠固体于两支试管中,试管编号为A、B
2
溶解
向两支试管中分别加入少量蒸馏水,振荡
2
滴管的使用
在上述澄清溶液中分别滴加稀盐酸,振荡
2
反应现象及结论
(1)A试管中反应的现象是
,原固体物质是。
(2)B试管中反应的现象是
,原固体物质是。
反应的化学方程式是
。
2
实验习惯
遵守规则、洗涤干净、整理物品、清理卫生
2
实验二配制100mL1mol·L—1盐酸
实验用品:
100mL容量瓶、烧杯、10mL量筒、玻璃棒、胶头滴管、蒸馏水、浓盐酸(密度1.19g·cm—3,质量分数37.5%)、
计算浓盐酸的用量
1.19g·cm—3
V
37.5%
=1mol·L—1
0.1L
36.5g·mol—1
V=8.2mL
量筒的使用
用量筒量取所需的浓盐酸,量筒读数正确
溶液的稀释
用玻璃棒引流盐酸于加水的烧杯中并搅拌
移液
用玻璃棒引流已稀释的盐酸移入容量瓶中,不流出瓶外
洗涤
(1)用水洗涤烧杯与玻璃棒2—3次
(2)洗涤液用玻璃棒引流注入容量瓶,不流出瓶外
定容
(1)用玻璃棒引流继续加水,溶液离刻度2—3cm时,改用胶头滴管加水至100mL。
(2)凹液面最低处与刻度相平。
混匀
倒转与摇动方法正确
实验内容
实验操作步骤
满分值
考评得分
计算
计算浓盐酸的用量
1
量筒的使用
用量筒量取所需的浓盐酸
1
溶液的稀释
将浓盐酸加入盛有水(约20mL)的烧杯中稀释并冷却。
1
移液
将已稀释的盐酸移入容量瓶中
1
洗涤
用约15mL的水洗涤烧杯,并将洗涤液注入容量瓶
2
定容
继续加水至100mL
2
混匀
将溶液摇匀
1
实验习惯
遵守规则、洗涤干净、整理物品、清理卫生
1
实验三证明某白色晶体是硫酸铵
实验用品:
试管、试管夹、酒精灯、玻璃棒、药匙、胶头滴管、硫酸铵(白色晶体)、水、NaOH溶液(3mol/L或10%)、BaCl2溶液、稀盐酸、红色石蕊试纸
药品的取用
(1)用药匙小端或纸槽盛药品,送入试管底部。
(2)瓶盖倒立在桌面,标签向手心,瓶口紧挨试管口。
(3)胶头滴管下端不伸入试管口、不接触试管。
加热
(1)酒精灯用火柴点燃,用毕用灯帽盖灭。
(2)试管夹从试管底部向上套入,并夹住试管中上部,拇指不能按在短柄上。
(3)试管与桌面成45℃角,试管口不准对着人,灯芯不可接触试管。
试纸使用
(1)把红色石蕊试纸润湿,粘在玻璃棒一端。
(2)将试纸放在试管口附近,不接触试管口。
实验现象结论
(1)白色沉淀;SO42-;Ba2++SO42-==BaSO4↓
(2)由红变蓝;NH3;
(3)(NH4)2SO4
实验内容
实验操作步骤
满分值
考评得分
药品的取用;硫酸根离子的检验
(1)取少量白色晶体于试管中,
(2)向试管中加入少量稀盐酸振荡,再加入氯化钡溶液振荡
2
酒精灯使用;试管夹使用;加热试管里的液体
(1)另取少量白色晶体于另一支试管中,向试管中加入少量氢氧化钠溶液振荡
(2)加热
2
试纸的使用
用红色石蕊试纸检验所生成的气体
2
实验现象结论
(1)加入稀盐酸无现象,白色晶体溶解,继续加入氯化钡溶液后观察到有证明溶液中含有含离子;反应的离子方程式为。
(2)石蕊试纸颜色变化情况是,证明产生的气体是。
(3)白色固体是。
3
实验习惯
遵守规则、洗涤干净、
整理物品、清理卫生
1
实验四氢氧化铝的制取及性质
实验用品:
试管、胶头滴管、Al2(SO4)3溶液、NaOH溶液、氨水、盐酸溶液
液体药品取用
(1)取下瓶盖倒立在桌面,标签向手心,瓶口紧挨试管口,倒完及时塞好,放回原处。
(2)溶液约取3mL。
氢氧化铝制取
(1)滴管下端不接触试管。
(2)氨水应逐滴加入,并不断振荡,至沉淀不再生成为止。
现象及化学方程式
(1)白色胶状沉淀生成
(2)Al2(SO4)3+6NH3.H2O=
2Al(OH)3↓+3(NH4)2SO4
氢氧化铝与盐酸反应
(1)白色沉淀消失
(2)Al(OH)3+3HCl=AlCl3+3H2O
氢氧化铝与氢氧化钠反应
(1)白色沉淀消失
(2)Al(OH)3+NaOH=NaAlO2+2H2O
实验内容
实验操作步骤
满分值
考评得分
液体药品的取用
取一试管倒入3mLAl2(SO4)3溶液
1
氢氧化铝制取
向试管里滴加氨水制取氢氧化铝,并将其一半分装于另一试管中
2
现象与化学方程式
加氨水时观察到的现象,
反应的化学方程式。
2
氢氧化铝与盐酸反应
向其中一支试管中加入盐酸,观察到现象
,反应的化学方程式为。
2
氢氧化铝与氢氧化钠反应
向另一支试管中加入NaOH溶液,观察到现象是,反应的化学方程式为。
2
实验习惯
遵守规则、洗涤干净、
整理物品、清理卫生
1
实验五证明金属镁比铝活泼
实验用品:
试管、镊子、砂纸、镁条、铝片、1mol·L-1盐酸。
镊子、砂纸的使用
1.镊子使用正确。
2.用砂纸将镁条、铝片上的氧化膜除去。
固体药品取用
1.瓶盖倒放桌上。
2.用镊子将打磨过的一小段镁条和一小片铝片分别送入两支试管底部。
液体药品取用
1.瓶盖倒放桌上。
2.标签向手心。
3.沿试管壁分别加入2mL
1mol·L-1盐酸。
现象与反应的方程式
两支试管壁都有气泡生成且伴有热量产生,但镁与盐酸反应更剧烈,速度比铝快。
Mg+2HCl==MgCl2+H2↑
2Al+6HCl==2AlCl3+3H2↑
实验内容
实验操作步骤
满分值
考试得分
除去固体表面的氧化膜
取一小段镁条和一小片铝片,用砂纸分别将其表面的氧化膜除去。
2
固体药品
取用
取两支试管,用镊子将打磨过的一小段镁条和一小片铝片分别送入试管中。
2
液体药品
取用
在上述两支试管中分别加入2mL1mol·L-1盐酸
2
结论现象与反应的方程式
请你描述观察到的现象__________,
反应方程式_______________________;
。
实验结论:
________________________。
3
实验习惯
遵守纪律,洗涤干净,
整理物品,清理卫生
1
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 课堂 高中 毕业 会考 化学 实验 考查
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《雷雨》中的蘩漪人物形象分析 1.docx
《雷雨》中的蘩漪人物形象分析 1.docx
