 初始审查送审材料清单模板.docx
初始审查送审材料清单模板.docx
- 文档编号:12214705
- 上传时间:2023-04-17
- 格式:DOCX
- 页数:12
- 大小:18.71KB
初始审查送审材料清单模板.docx
《初始审查送审材料清单模板.docx》由会员分享,可在线阅读,更多相关《初始审查送审材料清单模板.docx(12页珍藏版)》请在冰豆网上搜索。
初始审查送审材料清单模板
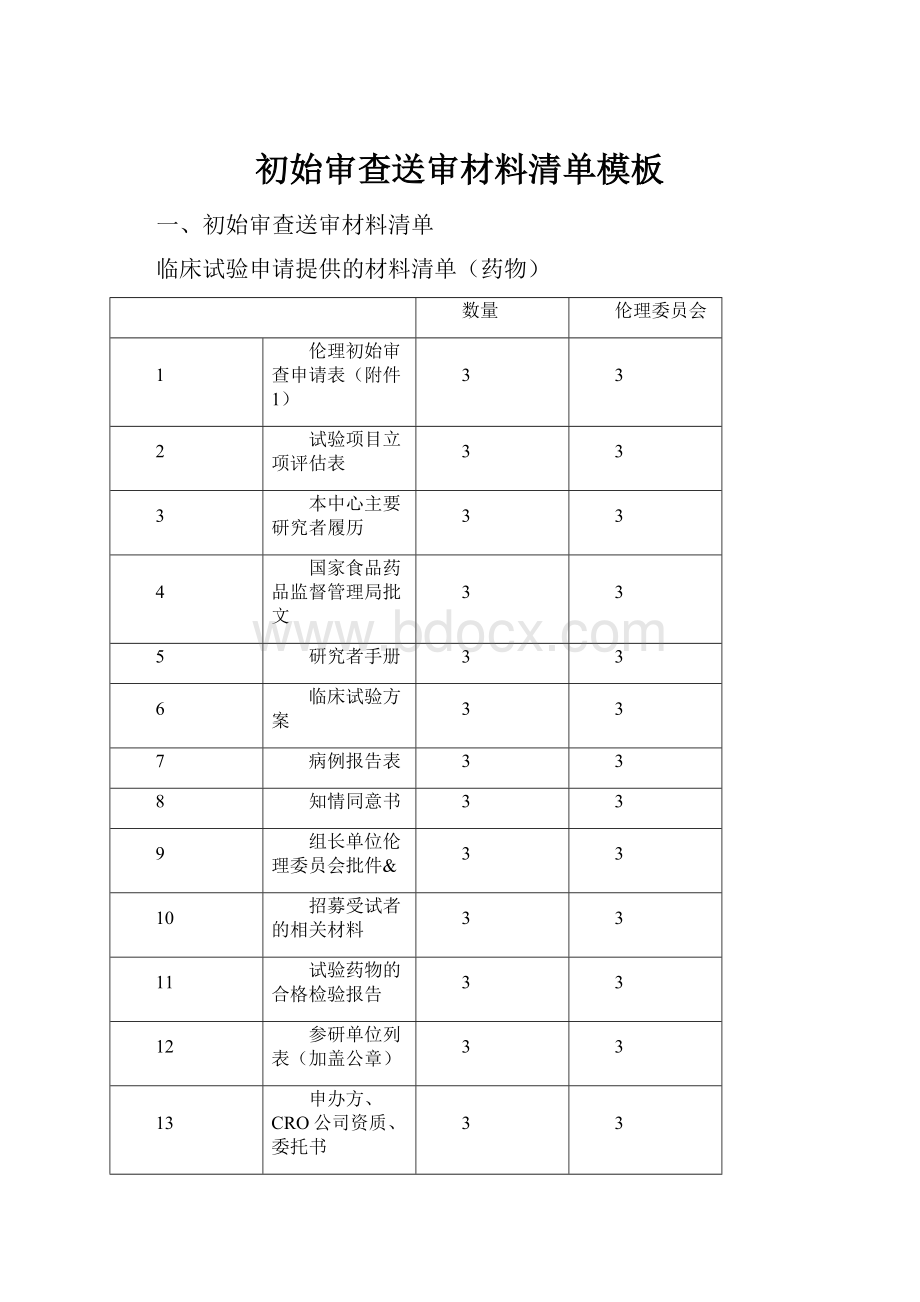
一、初始审查送审材料清单
临床试验申请提供的材料清单(药物)
数量
伦理委员会
1
伦理初始审查申请表(附件1)
3
3
2
试验项目立项评估表
3
3
3
本中心主要研究者履历
3
3
4
国家食品药品监督管理局批文
3
3
5
研究者手册
3
3
6
临床试验方案
3
3
7
病例报告表
3
3
8
知情同意书
3
3
9
组长单位伦理委员会批件&
3
3
10
招募受试者的相关材料
3
3
11
试验药物的合格检验报告
3
3
12
参研单位列表(加盖公章)
3
3
13
申办方、CRO公司资质、委托书
3
3
14
其他(研究病历、日志卡等)
3
3
临床试验申请提供的材料清单(器械)
数量
伦理委员会
1
伦理初始审查申请表(附件1)
3
3
2
试验项目立项评估表
3
3
3
本中心主要研究者履历
3
3
4
国家食品药品监督管理局批文(如适用)
3
3
5
研究者手册
3
3
6
临床试验方案
3
3
7
病例报告表
3
3
8
知情同意书
3
3
9
其它伦理委员会对申请研究项目的重要决定(如适用)
3
3
10
招募受试者的相关材料(如适用)
3
3
11
产品说明书/产品行业标准
3
3
12
产品质量检测报告/自测报告
12
参研单位列表(加盖公章)
3
3
13
申办方、CRO公司资质、委托书
3
3
14
其他(研究病历、日志卡等)
3
3
临床试验申请提供的材料清单(体外诊断试剂)
数量
伦理委员会
1
伦理初始审查申请表(附件1)
3
3
2
试验项目立项评估表
3
3
3
本中心主要研究者履历
3
3
4
国家食品药品监督管理局批文(如适用)
3
3
5
研究者手册
3
3
6
临床试验方案
3
3
7
试验数据记录表
3
3
8
产品质量检测报告/自测报告
3
3
9
产品说明书
3
3
10
产品行业标准
3
3
11
知情同意书(或免除知情的申请书)
3
3
12
参研单位列表(加盖公章)
3
3
13
申办方、CRO公司资质、委托书
3
3
注意事项:
1、&其它伦理委员会对申请研究项目的重要决定的说明,应提供以前否定结论的理由。
2、附件1伦理审查申请表需由PI签字,递交电子版材料时附上PI签字的扫描件。
3、申办方应将伦理费汇款凭证发到伦理办公室黄老师的邮箱:
********@。
4、装订要求:
每项资料间请用彩色纸质分类索引卡(如图1)进行分隔,用50mm长尾夹固定资料后装入档案盒(如图2,药物/器械临床试验请用55mm规格,体外诊断试剂请用35mm规格)中进行邮寄。
图1图2
5、伦理初审材料3份递交到伦理委员会办公室,其中1份原件,2份复印件。
6、申办方在递交伦理初审材料至伦理委员会办公室之前,请先确认伦理递交信及伦理初审申请PI的签字是否完成,由伦理委员会审查电子版资料并确认无误后再递交纸质版资料。
7、关于伦理审查材料的递交,本中心SAE报告、方案违背报告、研究进展报告需先经过机构办公室再交到伦理委员会;其它类型审查或备案资料请您直接与伦理委员会联系,递交伦理资料时,请您将交到伦理委员会资料的最终版及递交回执交到机构办备案(包括电子版和纸质版原件)。
联系地址:
机构办公室:
办公楼3楼药物临床试验机构办公室,电话:
********
伦理秘书联系方式:
实训楼3楼科教信息部,吴科长,电话:
********
伦理委员会办公室联系方式:
实训楼3楼伦理委员会办公室,电话:
********
附件1
初始审查申请
项目
项目来源
项目批件号
方案版本号
方案版本日期
知情同意书版本号
知情同意书版本日期
组长单位
组长单位主要研究者
参加单位
柳州市人民医院
本院承担科室
本院主要研究者
一、研究信息
●方案设计类型
✧□实验性研究
✧□观察性研究:
□回顾性分析,□前瞻性研究
●研究信息
✧资金来源:
□企业,□政府,□学术团体,□本单位,□自筹
✧数据与安全监察委员会:
□有,□无
✧其它伦理委员会对该项目的否定性或提前中止的决定:
□无,□有→请提交相关文件
✧研究需要使用人体生物标本:
□否,□是→填写下列选项
©采集生物标本:
□是,□否
©利用以往保存的生物标本:
□是,□否
✧研究干预超出产品说明书范围,没有获得行政监管部门的批准:
□是,□否
(选择“是”,填写下列选项)
©研究结果是否用于注册或修改说明书:
□是,□否
©研究是否用于产品的广告:
□是,□否
©超出说明书使用该产品,是否显著增加了风险:
□是,□否
✧医疗器械的类别:
□I类,□Ⅱ类,□Ⅲ类,□体外诊断试剂
●招募受试者
✧谁负责招募:
□医生,□研究者,□研究助理,□研究护士,□其它:
✧招募方式:
□广告,□个人联系,□数据库,□中介,□其它:
✧招募人群特征:
□健康者,□患者,□弱势群体,□孕妇
©弱势群体的特征(选择弱势群体,填写选项):
□儿童/未成年人,□认知障碍或健康状况而没有能力做出知情同意的成人,
□申办者/研究者的雇员或学生,□教育/经济地位低下的人员,
□疾病终末期患者,□囚犯或劳教人员,□其它:
©知情同意能力的评估方式(选择弱势群体,填写该选项):
□临床判断,□量表,□仪器
©涉及孕妇研究的信息(选择孕妇,填写该选项):
□没有通过经济利益引诱其中止妊娠,□研究人员不参与中止妊娠的决策,
□研究人员不参与新生儿生存能力的判断
✧受试者报酬:
□有,□无
©报酬金额:
元
©报酬支付方式:
□按随访观察时点,分次支付,
□按完成的随访观察工作量,一次性支付,
□完成全部随访观察后支付
●知情同意的过程
✧谁获取知情同意:
□医生/研究者,□医生,□研究者,□研究护士,□研究助理
✧获取知情同意地点:
□私密房间/受试者接待室,□诊室,□病房
✧知情同意签字:
□受试者签字,□法定代理人签字
©知情同意的例外:
□否,□是→填写下列选项
±□申请开展在紧急情况下无法获得知情同意的研究:
°研究人群处于危及生命的紧急状况,需要在发病后很快进行干预。
°在该紧急情况下,大部分病人无法给予知情同意,且没有时间找到法定代理人。
°缺乏已被证实有效的治疗方法,而试验药物或干预有望挽救生命,恢复健康,或减轻病痛。
±□申请免除知情同意・利用以往临床诊疗中获得的病历/生物标本的研究。
±□申请免除知情同意・研究病历/生物标本的二次利用。
±□申请免除知情同意签字・签了字的知情同意书会对受试者的隐私构成不正当的威胁,联系受试者真实身份和研究的唯一记录是知情同意文件,并且主要风险就来自于受试者身份或个人隐私的泄露。
±□申请免除知情同意签字・研究对受试者的风险不大于最小风险,并且如果脱离“研究”背景,相同情况下的行为或程序不要求签署书面知情同意。
如访谈研究,邮件/电话调查。
二、主要研究者信息
●主要研究者声明:
✧□本人与该研究项目不存在利益冲突□本人与该研究项目存在利益冲突
●主要研究者负责的在研项目数:
项
●主要研究者负责的在研项目中,与本项目的目标疾病相同的项目数:
项
申请人责任声明
我将遵循GCP、方案以及伦理委员会的要求,开展本项临床研究
申请人签字
日期
二、跟踪审查送审材料清单
1.修正案审查申请
●修正案审查申请(附件2)
●伦理递交信
●临床研究方案修正说明页
●修正的临床方案
●修正的知情同意书
●知情同意书修正说明页
●修正的招募材料
●临床试验方案修正对照表
2.研究进展报告
●研究进展报告
●其它
3.严重不良事件报告
●严重不良事件报告
4.违背方案报告
●违背方案报告
5.暂停/终止研究报告
●暂停/终止研究报告
●其它
6.研究完成报告
●研究完成报告
●分中心小结
三、复审送审材料清单
复审申请
●复审申请(附件3)
●修正的临床研究方案(注明版本号/版本日期)
●修正的知情同意书(注明版本号/版本日期)
●修正的招募材料(注明版本号/版本日期)
●其它
附件2
修正案审查申请
项目
项目来源
方案版本号
方案版本日期
知情同意书版本号
知情同意书版本日期
伦理审查批件号
主要研究者
一、一般信息
●提出修正者:
□项目资助方,□研究中心,□主要研究者
●修正类别:
□研究设计,□研究步骤,□受试者例数,□纳入排除标准,□干预措施,
□知情同意书,□招募材料,□其它:
●为了避免对受试者造成紧急伤害,在提交伦理委员会审查批准前对方案进行了修改并实施:
□不适用,□是
二、修正的具体内容与原因
三、修正案对研究的影响
●修正案是否增加研究的预期风险:
□是,□否
●修正案是否降低受试者预期受益:
□是,□否
●修正案是否涉及弱势群体:
□是,□否
●修正案是否增加受试者参加研究的持续时间或花费:
□是,□否
●如果研究已经开始,修正案是否对已经纳人的受试者造成影响:
□不适用,□是,□否
●在研受试者是否需要重新获取知情同意:
□是,□否
申请人签名
日期
附件3
复审申请
项目
项目来源
方案版本号
方案版本日期
知情同意书版本号
知情同意书版本日期
伦理审查批件号
主要研究者
修正情况
●完全按伦理审查意见修改的部分
●参考伦理审查意见修改的部分
●没有修改,对伦理审查意见的说明
申请人签名
日期
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 初始 审查 送审 材料 清单 模板
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
