 整理精品药品不良反应病例报告调查表_精品文档.doc
整理精品药品不良反应病例报告调查表_精品文档.doc
- 文档编号:1201248
- 上传时间:2022-10-18
- 格式:DOC
- 页数:3
- 大小:47KB
整理精品药品不良反应病例报告调查表_精品文档.doc
《整理精品药品不良反应病例报告调查表_精品文档.doc》由会员分享,可在线阅读,更多相关《整理精品药品不良反应病例报告调查表_精品文档.doc(3页珍藏版)》请在冰豆网上搜索。
。
。
。
。
。
。
。
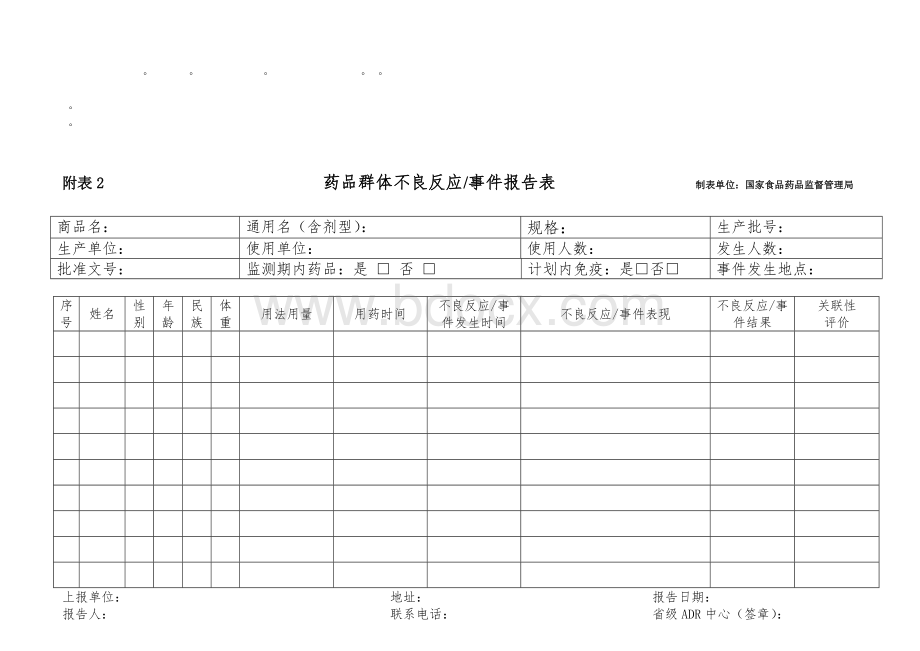
附表2药品群体不良反应/事件报告表制表单位:
国家食品药品监督管理局
商品名:
通用名(含剂型):
规格:
生产批号:
生产单位:
使用单位:
使用人数:
发生人数:
批准文号:
监测期内药品:
是□否□
计划内免疫:
是□否□
事件发生地点:
序号
姓名
性别
年龄
民族
体重
用法用量
用药时间
不良反应/事件发生时间
不良反应/事件表现
不良反应/事件结果
关联性
评价
上报单位:
地址:
报告日期:
报告人:
联系电话:
省级ADR中心(签章):
附:
1)其它相关资料请按附录C要求另附页报告;
2)典型病例请填写《药品不良反应/事件报告表》;
3)不良反应/事件结果指治愈、好转、有后遗症或死亡。
药品群体不良反应/事件报告要求
一、医疗卫生机构报告要求:
1.事件描述
①发生时间
②地点
③涉及药品名称
④药品不良反应/事件主要表现
⑤诊治过程
⑥转归情况
⑦在该地区是否为计划内免疫药品
2.典型病例详细填写《药品不良反应/事件报告表》
3.报告人及联系电话
二、药品生产企业报告要求:
1.事件发生、发展、处理等相关情况
2.药品说明书(进口药品须提供国外说明书)
3.质量检验报告
4.是否在监测期内(进口药是否为首次获准进口五年内)
5.注册、再注册时间
6.药品生产批件
7.执行标准
8.国内外药品安全性研究情况、国内外药品不良反应发生情况包括文献报道
9.典型病例详细填写《药品不良反应/事件报告表》
10.报告人及联系电话
三、省、自治区、直辖市药品不良反应监测中心报告要求
1.组织填写《药品群体不良反应/事件报告表》
2.整理、分析收到材料
3.提出关联性评价意见
4.密切关注事件后续发展
5.事件过程详细调查报告(事件发生、发展、处理、结果等)
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 整理 精品 药品 不良反应 病例 报告 调查表 文档
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 12处方点评管理规范实施细则_精品文档.doc
12处方点评管理规范实施细则_精品文档.doc
 17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
