 p区元素二习题.docx
p区元素二习题.docx
- 文档编号:11607221
- 上传时间:2023-03-28
- 格式:DOCX
- 页数:27
- 大小:31.50KB
p区元素二习题.docx
《p区元素二习题.docx》由会员分享,可在线阅读,更多相关《p区元素二习题.docx(27页珍藏版)》请在冰豆网上搜索。
p区元素二习题
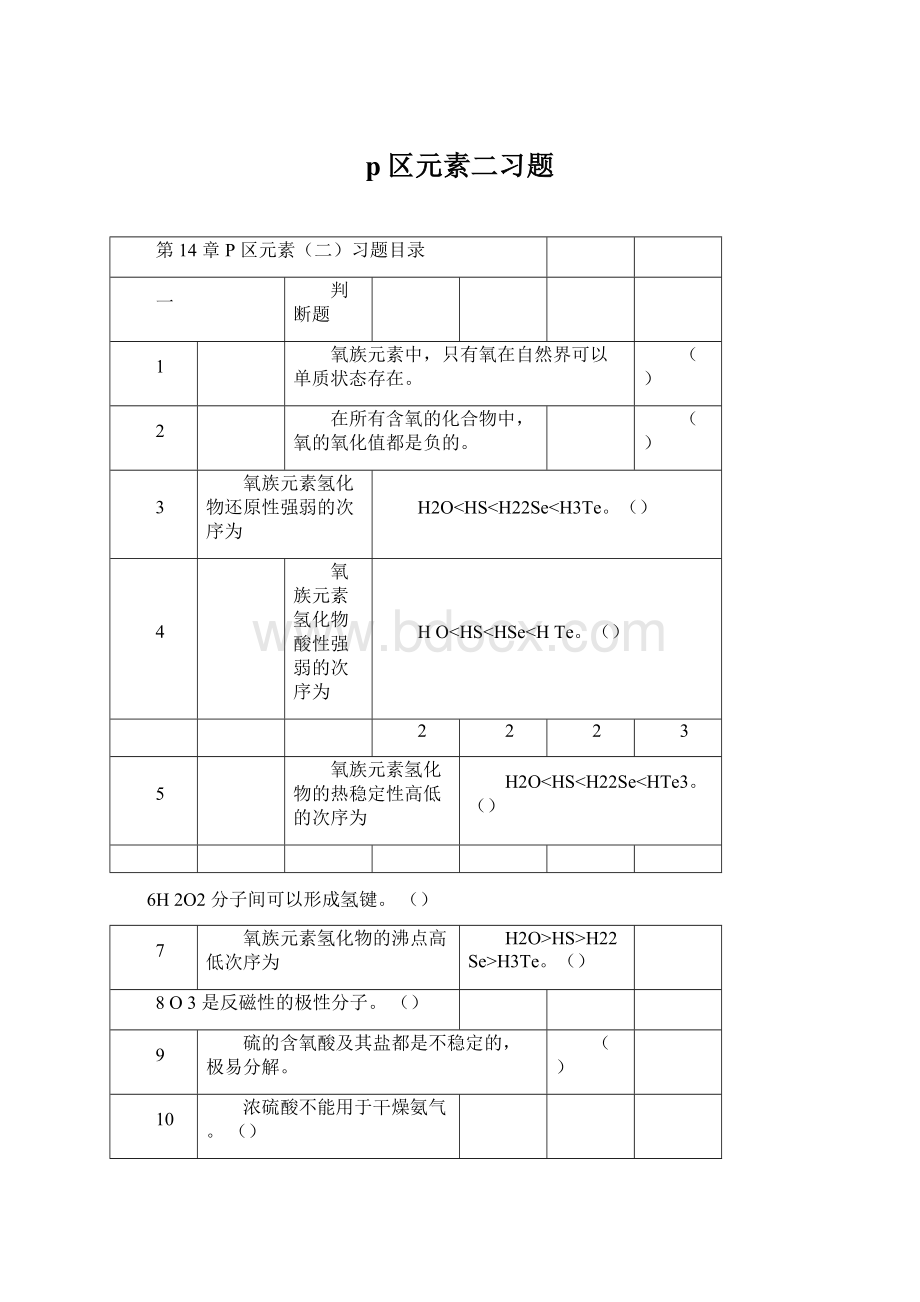
第14章P区元素
(二)习题目录
一
判断题
1
氧族元素中,只有氧在自然界可以单质状态存在。
()
2
在所有含氧的化合物中,氧的氧化值都是负的。
()
3
氧族元素氢化物还原性强弱的次序为
H2O () 4 氧族元素氢化物酸性强弱的次序为 HO () 2 2 2 3 5 氧族元素氢化物的热稳定性高低的次序为 H2O () 6H2O2分子间可以形成氢键。 () 7 氧族元素氢化物的沸点高低次序为 H2O>HS>H22Se>H3Te。 () 8O3是反磁性的极性分子。 () 9 硫的含氧酸及其盐都是不稳定的,极易分解。 () 10 浓硫酸不能用于干燥氨气。 () 11 可用浓硫酸干燥CO气体。 () 2 12 H2S在空气中燃烧的产物只能是 SO2和H2O。 () 13 可用FeS与HNO3反应制取H2S。 () 14 SO 2 是大气的主要污染源之一,酸雨主要是由 SO形成的。 () 2 15 浓硫酸虽有强氧化性,但仍可用铁罐运输。 () 16浓硫酸属于高沸点酸。 () 17将H2S通入MnSO4溶液中,可得到MnS沉淀。 () 18H2S溶液放置一段时间变混浊,是因为H2S被空气氧化生成S沉淀。 () 19 用Na2S溶液与含Cr3+的溶液反应,得不到 Cr2S3,若想制得Cr2S3必须采用干法。 106 用Na2S溶液与含Al3+的溶液反应,可得到Al2S3。 () 20 硫代硫酸钠的俗名是大苏打。 () 21 海波的化学式为Na2S2O3·5H2O。 () 22 在照像行业中Na2S2O3作为定影剂使用是基于它具有还原性。 () 23 在酸性溶液中,KMnO只能将HS氧化为单质硫。 () 4 2 24 氢氟酸能腐蚀玻璃,故需要用塑料瓶保存。 () 25 在氢卤酸中,由于氟的非金属性强,所以氢氟酸的酸性最强。 () 26 所有卤素元素都有正的氧化值。 () 27 在卤素与氧的化合物中,每种卤素都有多种正氧化值。 () 28 卤化氢沸点高低的次序为HF () 29 卤化氢热稳定性高低的次序为 HF>HCl>HBr.>HI。 () 30 卤化氢还原性强弱的次序为 HF () 31卤化氢酸性强弱的次序为HCl>HBr.>HI>HF。 () 32卤素单质在水中都可以发生歧化反应。 () 33卤素单质在酸性介质中更容易发生歧化反应。 () 34除HF外,可用卤化物与浓硫酸反应制取卤化氢。 () 35卤素单质水解反应进行的程度由Cl2到I2依次减弱。 () 36HClO4是最强的无机酸。 () 37氯的含氧酸酸性强弱次序为HClO () 38 氯的含氧酸盐热稳定性强弱次序为MClO () 39 氯的含氧酸氧化性强弱的次序为 HClO () 2 3 4 40 氯酸钾是强氧化剂,在氯酸钾的水溶液中加入 KI 即有I2生成。 () 41 将KClO3溶液与KI溶液混合,无明显现象发生,当加入稀 H2SO4后,就有I2生成。 () 42 在氯的含氧酸中,随着氯的氧化值增加,其氧化性越来越强。 () 43 可用溴化钠与浓磷酸反应制取溴化氢。 () 44 常温下BrO-在碱性溶液中不能存在。 () 45 卤酸的酸性强弱次序为: HClO>HBrO>HIO。 () 3 3 3 46 高溴酸的氧化性比高氯酸的弱。 () 47 次卤酸盐热稳定性高低的次序为 MClO>MBrO>MIO。 () 48 高卤酸氧化性强弱的次序为HClO4>HBrO4>H5IO6。 () 49 高卤酸酸性强弱的次序为 HClO>HBrO>HIO 。 () 4 4 5 6 50 卤酸酸性强弱的次序为HClO3>HBrO3>HIO3。 () 51 次卤酸酸性强弱的次序为 HClO>HBrO>HIO。 () 52HNO是一元酸,HCO是二元酸,HBO是三元酸,HPO是四元酸,HIO 是五元酸。 () 3 2 3 3 3 4 2 7 5 6 53 在含有Fe3+的溶液中加入 H2S,可生成 Fe2S3沉淀。 () 二选择题 1下列物质中沸点最高的是()。 (A)H2Se;(B)H2S;(C)H2Te;(D)H2O。 2下列叙述中错误的是()。 (A)自然界中只存在单质氧而没有单质硫; (B)氧既有正氧化值化合物,也有负氧化值的化合物; (C)由2H和O组成的水叫重水; (D)O2和O3是同素异形体。 3大气的臭氧层能保护人类的生态环境,其原因是()。 (A)能保温; (B)能消毒; (C)能防止地球表面水蒸气逸散; (D)能吸收紫外线。 4人们非常重视高层大气中的臭氧,因为它()。 (A)有消毒作用;(B)有温室效应; (C)有助于植物生长;(D)能吸收紫外线。 5有助于反应3O2→2O3(△rH>0)进行的条件是()。 (A)高温和低压;(B)高温和高压; (C)低温和低压;(D)低温和高压。 6O2和O3属于()。 (A)同位素;(B)类质同晶体; (C)同素异形体;(D)同分异构体。 7下列氢化物在水溶液中,酸性最强的是()。 (A)H2O;(B)H2S;(C)H2Se;(D)H2Te。 8下列对氧族元素性质的叙述中正确的()。 (A)氧族元素与其它元素化合时,均可呈现+2,+4,+6或-1,-2等氧化值; (B)氧族元素电负性从氧到钋依次增大; (C)氧族元素的电负性从氧到钋依次减小; (D)氧族元素都是非金属元素。 9H2O2在与用硫酸酸化的KI溶液反应时起的作用是()。 (A)还原剂;(B)氧化剂;(C)弱酸;(D)既是氧化剂又是还原剂。 10下列叙述中错误的是()。 (A)H2O2分子构型为直线形; (B)H2O2既有氧化性又有还原性; (C)H2O2是弱酸; (D)HO在酸性介质中能使KMnO溶液褪色。 224 11下列关于过氧化氢分子结构的描述中,正确的是()。 (A)分子在空间成平面形; (B)两个O-H键不在同一平面; (C)两个O-H键相互垂直; (D)H-O 键与 O-O键之间夹角成 90o。 12下列氧化物的水合物酸性最强的是()。 (A)Ge(OH);(B)HSeO;(C)HPO;(D)Ca(OH)。 424342 13下列试剂可用于定量测定碘的是() 。 (A)NaS;(B)NaSO;(C)NaSO;(D)NaSO。 223223228 13浓H2SO4与Zn反应的产物中不可能有的物质是()。 (A)SO2;(B)H2;(C)S;(D)H2S。 15Na2S2O3作照像定影剂时,它是一种()。 (A)氧化剂;(B)还原剂;(C)配位剂;(D)漂白剂。 16将稀盐酸与下列化合物混合,其中不产生气体的是()。 (A)BaS;(B)BaSO3;(C)BaSO4;(D)BaS2O3。 17欲干燥H2S气体,在下列干燥剂中应选用()。 (A)浓H2SO4;(B)KOH;(C)CaO;(D)P2O5。 18SO可以除去水中的氯气,其中SO的作用是()。 22 (A)氧化剂;(B)还原剂;(C)配位剂;(D)漂白剂。 19在下列各盐溶液中通入H2S(g)不生成硫化物沉淀的是()。 (A)Ag+;(B)Cd2+;(C)Pb2+;(D)Mn2+。 20下列各组硫的化合物中,均不具有还原性的是() (A)K2S2O7,Na2S2O3;(B)H2SO3,Na2S2O3; (C)KSO,NaSO;(D)NaSO,HSO。 22722822323 。 21下列离子在酸性溶液中能够稳定存在的是() 。 (A)SO42-;(B)S22-;(C)S2O32-;(D)S2O82-。 22SO、SO、HS三种硫的化合物中,能使溴水褪色的是()。 3 2 2 (A)SO 和SO;(B)SO 和HS; 3 2 3 2 (C)SO2 和H2S;(D)SO3、SO2和H2S。 23分别向下列各组离子的溶液中加酸,其溶液澄清,并产生臭蛋气味的一组离子是() 。 (A)S2-和SO2- ;(B)S2-和SO2-; 4 x 4 (C)SO2-和SO2-- ;(D)S x 2-和SO2-。 23 3 3 24 列反应中产物错误的是()。 (A)在CuSO4中通入H2S生成CuS; (B)Na2S与HCl(aq)作用生成H2S; (C)H2S与Cl2混合生成硫酸; (D)FeS与HNO3作用生成H2S。 25 下列物质中,既能和 HS溶液反应又能和酸化的 KMnO(aq) 2 4 (A)Fe(NO3)3(aq);(B)FeSO4(aq); (C)H2SO(aq)3 ;(D)CuSO4(aq)。 26下列叙述中错误的是()。 (A)SO2分子是非极性分子;(B)SO2可使品红褪色;(C)HSO是中强酸;(D)HSO既有氧化性又有还原性。 2323 27下列含氧酸盐溶于HAc的()。 (A)CaSiO3;(B)BaSO3;(C)BaSO4;(D)CaSO4。 28下列各组硫化物中,都难溶于 0.3mol·L-1HCl而能溶于浓 (A)Bi2S3和CdS;(B)ZnS和PbS; 反应的是()。 HCl的()。 (C)CuS和Sb2S3;(D)As2S3和HgS。 29下列各组离子的酸性溶液中,通入H2S都能生成沉淀的一组是()。 (A)Mn2+、Pb2+、Sb3+;(B)Mn2+、Fe2+、Sb3+; 2+2+3+2+2+2+ (C)Cu、Cd、Sb;(D)Fe、Cu、Mn。 30下列各组离子与Na2S溶液反应,都不生成黑色沉淀的一组是()。 (A)Fe2+、Bi3+;(B)Cd2+、Zn2+;(C)Mn2+、Pb2+;(D)Ag+、Al3+。 31焦硫酸的分子式为()。 (A)HSO;(B)HSO·xSO(x>1);(C)HSO;(D)HSO。 227243228224 32SnS不溶于新配制的(NH4)2S中,但可溶于放置一定时间的(NH4)2S溶液中,这是因为()。 (A)存放一定时间的(NH4)2S中,存在Sx2-,它具有氧化性; (B)存放一定时间的(NH4)2S中,存在Sx2-,它具有还原性; (C)存放一定时间的(NH4)2S中,存在Sx2-,它具有碱性; (D)存放一定时间的(NH4)2S中,存在Sx2-,它具有酸性。 33下列各组溶液中,各种离子能在溶液中大量共存的是()。 (A)SO 4 2-、SO2- 、Na+、H+;(B)Cu2+、NH+、Cl- 、NO- ; 2 3 4 3 (C)Fe 3+ - + - 3+ - + - 、Cl 、K 、NCS;(D)Cr 、Cl 、Na、OH。 34下列物质中酸性最强的是()。 (A)HS;(B)HSO;(C)HSO;(D)HSO。 2 2 3 2 4 2 2 7 320 用容量法定量测定碘,常使用的标准溶液() 。 (A)Na 2 S;(B)Na 2 SO;(C)NaSO;(D)NaSO。 3 2 4 2 2 3 35下列叙述中,错误的是()。 (A)Na2S2O3可作为还原剂,在反应中只能被氧化成 S4O62-; (B)在早期的防毒面具中,曾应用Na2S2O3作解毒剂; (C)照相术中,AgBr被Na2S2O3溶液溶解而生成配离子; (D)Na2S2O3可用于棉织物等漂白后脱氯。 36下列化合物中氧化能力最强的是()。 (A)NaSO;(B)NaSO;(C)NaSO;(D)NaSO。 22323246228 37某未知液中含有 (A)NaCl(aq);(B)Br KSO或KSO,要简便地鉴定它们,最好加入下列试剂中的() 2423 2(aq);(C)H2O2(aq);(D)KOH(aq)。 。 38将含某阴离子的溶液先用 HSO酸化后,再加入 24 KMnO。 在加 4 KMnO前后只观察到紫色褪 4 去,说明该溶液中可能存在的阴离子是() 。 (A)S2O32-;(B)SO32-;(C)NO3-;(D)PO43-。 39下列分子或离子中含有43键的是()。 (A)NO3-;(B)SO32-;(C)O3;(D)SO42-。 40下列分子或离子中含有43键的是()。 (A)SO2;(B)NO3-;(C)NO2;(D)NO2+。 41卤素单质X2在碱性介质中的歧化反应可表示为: ------ X2+2OH=X+XO+H2O,3X2+6OH=5X+XO+3H2O 不能发生任何歧化反应的卤素()。 (A)溴;(B)氯;(C)氟;(D)碘。 42X2在H2O中的歧化反应趋势较大的()。 (A)F2;(B)Cl2;(C)Br2;(D)I2。 43 卤素单质中,与水不发生水解反应的是() 。 (A)F2;(B)Cl2;(C)Br2;(D)I2。 44SiX4中,可以与HX发生加合反应的()。 (A)SiF4;(B)SiCl4;(C)SiBr4;(D)SiI 4。 45在常温下,易被空气氧化的氢卤酸是()。 (A)HF;(B)HCl;(C)HBr;(D)HI。 46 下列关于卤素单质性质的叙述中,正确的是() 。 (A)卤素单质在溶液中能氧化水中的氧 ; (B)卤素有较高的化学活泼性,在自然界中以化合态存在 ; (C)卤素单质加淀粉溶液呈蓝紫色; (D)卤素单质在碱性溶液中均能发生歧化反应。 47 下列叙述中正确的是()。 (A)卤素的最高氧化值均等于其族序数 ; (B)卤素的电子亲合能随着原子序数的增大而变小 ; (C)卤素的电负性随着原子序数的增大而变小 ; (D)卤素单质的氧化性以I2最弱,所以自然界中只能有单质碘。 48下列实验可以用来区别NaBr(aq)和NaI(aq)的是()。 (A)分别通入CO;(B)分别通入Cl; 22 (C)分别加入NaNO(aq);(D)分别加入K(s)。 3 49决定卤素单质熔点高低的主要因素是()。 (A)卤素单质分子的极性大小; (B)卤素单质的相对分子质量的大小; (C)卤素单质分子中的化学键的强弱; (D)卤素单质分子的氧化性强弱。 50氢卤酸中最强的酸是()。 (A)HF;(B)HCl;(C)HBr;(D)HI。 51下列酸中不属于弱酸的是()。 (A)HI;(B)HClO2;(C)HOCl;(D)HF。 52氯的含氧酸中,酸性最强的()。 (A)HClO;(B)HClO2;(C)HClO3;(D)HClO4。 53下列物质中,与Cl2作用生成漂白粉的是()。 (A)水合硫酸钙;(B)无水硫酸钙;(C)氢氧化钙;(D)氯化钙。 54HClO4的酸酐是()。 (A)ClO3;(B)ClO2;(C)Cl2O5;(D)Cl2O7。 55列氯化物中,能与水反应的是()。 (A)NaCl;(B)BaCl2;(C)PCl3;(D)CCl4。 56下列氢化物热稳定性顺序正确的()。 (A)HF>HI>HBr>HCl;(B)HF>HCl>HBr>HI; (C)HI>HBr>HCl>HF;(D)HI>HBr>HF>HCl。 57在下列各种酸中氧化性最强的是()。 (A)HClO3;(B)HClO;(C)HClO4;(D)HCl。 58在氢卤酸中,由HF到HI酸性逐渐增强,其主要原因是()。 (A)从HF到HI键能减弱;(B)从F到I原子的电负性减小; (C)从F到I的相对原子质量增大;(D)从F到I原子的电子亲合能减小。 59为制备卤化氢水溶液,下列方法中错误的是()。 (A)萤石与浓硫酸反应制备HF,再溶于水; (B)先电解食盐水制备Cl2和H2,再合成HCl溶于水; (C)溴化钠与浓硫酸反应制取HBr气体,再溶于水; (D)将溴逐滴加入在磷与水的混合物中制备HBr气体,再溶于水。 60下列关于氯的含氧酸及其钠盐性质变化规律的叙述中错误的是()。 (A)氯的含氧酸氧化能力比其相应钠盐的氧化能力弱; (B)随着氯的氧化值增大,含氧酸酸性增强,即HClO4是氯的含氧酸中酸性最强的; (C)氯的含氧酸的热稳定性比相应钠盐的热稳定性差; (D)在酸性介质中,氯的含氧酸根离子的氧化能力比在碱性介质中的氧化能力强。 61氯的含氧酸中,热稳定性最强的是()。 (A)HClO;(B)HClO2;(C)HClO3;(D)HClO4。 62氯的含氧酸盐中,热稳定性最强的()。 (A)KClO;(B)KClO2;(C)KClO3;(D)KClO4。 63下列能够相互作用产生Cl2的一组物质是()。 (A)HCl+I2;(B)HClO3+I2;(C)NaClO3+I2;(D)CCl4+I2。 64下列反应不能用于在实验室中制取氯气的是()。 (A)浓HSO与NaCl作用;(B)浓HCl与MnO作用; 242 (C)浓HCl与KCrO一起加热;(D)HCl与KMnO作用。 274 65下列混合物受热产生氯气的一组物质是() 。 (A)NaCl 与H2SO4(浓);(B)NaCl与MnO2; (C)KClO 3 与HNO;(D)HCl与KMnO。 3 4 66实验室制备的Cl2(g)需要净化以除去可能带入的杂质。 下列各物质分别装在洗气瓶中,并使Cl2(g)按规定的顺序通过,其中正确的是()。 (A)NaOH,HSO(浓);(B)HSO(浓),HO; 24242 (C)HO,HSO(浓);(D)碱石灰,HSO(浓)。 22424 67关于HClO4及其盐的叙述中,错误的是()。 (A)无水HClO4是很强的氧化剂;(B)HClO4的氧化性弱于HClO;(C)ClO4-是不良配体;(D)KClO4的溶解度大于KCl。 68下列叙述中错误的是()。 (A)HClO3的氧化性强于KClO3; (B)KClO3在酸性溶液中可氧化Cl-; (C)将Cl2(g)通入酸性溶液中可发生歧化反应; (D)常温下在碱性介质中,ClO3-不能发生歧化反应。 69下列氯的含氧酸盐在碱性溶液中不能歧化的是()。 (A)次氯酸盐;(B)亚氯酸盐;(C)氯酸盐;(D)高氯酸盐。 70某物质与二氧化锰混合后加几滴浓HSO有气体产生,将产生的气体通入 24 以得到易溶于稀氨水的白色沉淀,该物质是()。 (A)LiBr;(B)NaF;(C)KI;(D)CsCl。 AgNO(g), 3 可 71下列生成 Cl2(g) 的反应中必须用浓 HCl的是()。 (A)KMnO4+HCl;(B)P
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 元素 习题
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《雷雨》中的蘩漪人物形象分析 1.docx
《雷雨》中的蘩漪人物形象分析 1.docx
