 初三期中考试化学复习资料.docx
初三期中考试化学复习资料.docx
- 文档编号:11569758
- 上传时间:2023-03-19
- 格式:DOCX
- 页数:17
- 大小:283.41KB
初三期中考试化学复习资料.docx
《初三期中考试化学复习资料.docx》由会员分享,可在线阅读,更多相关《初三期中考试化学复习资料.docx(17页珍藏版)》请在冰豆网上搜索。
初三期中考试化学复习资料
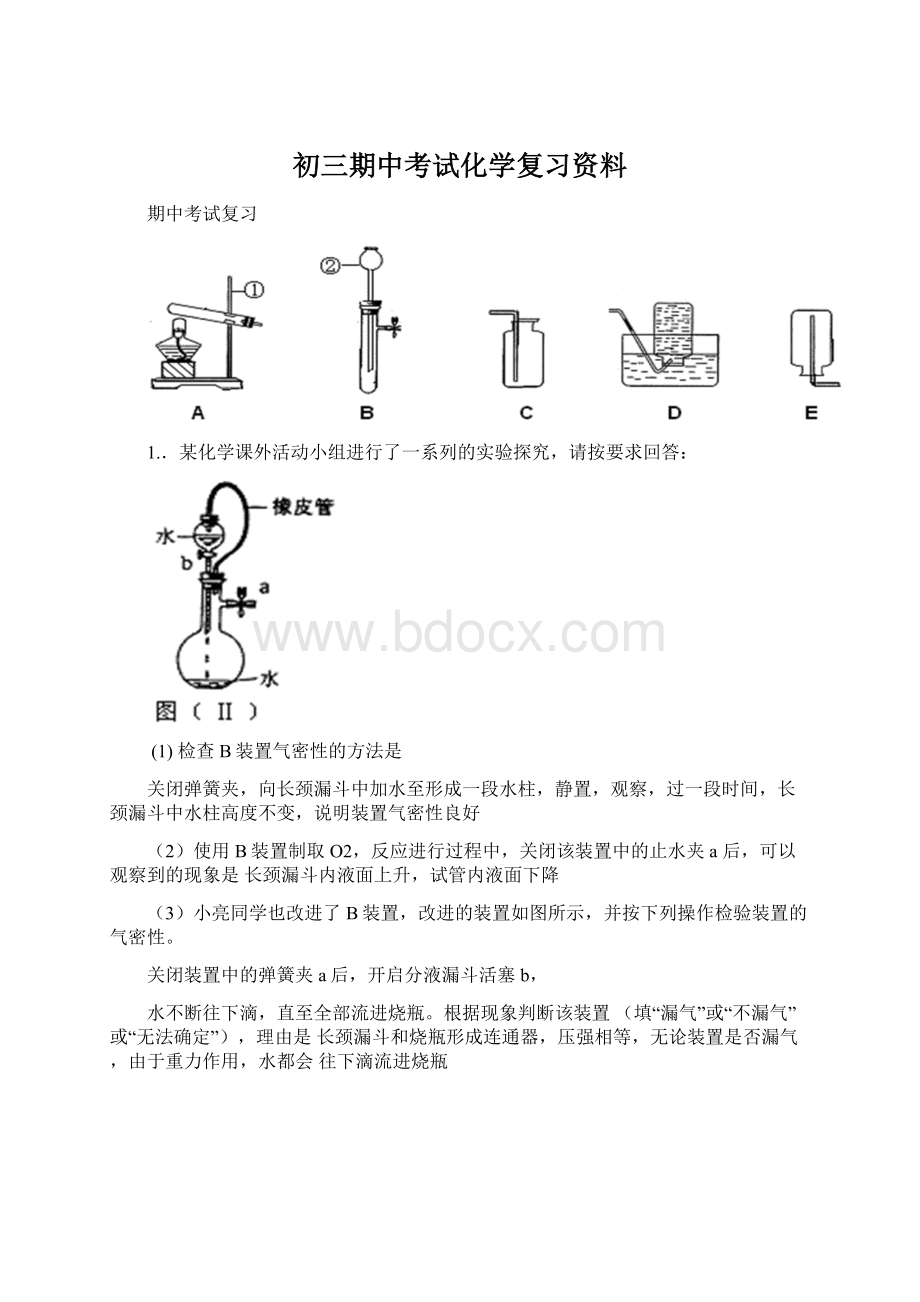
期中考试复习
1..某化学课外活动小组进行了一系列的实验探究,请按要求回答:
(1)检查B装置气密性的方法是
关闭弹簧夹,向长颈漏斗中加水至形成一段水柱,静置,观察,过一段时间,长颈漏斗中水柱高度不变,说明装置气密性良好
(2)使用B装置制取O2,反应进行过程中,关闭该装置中的止水夹a后,可以观察到的现象是长颈漏斗内液面上升,试管内液面下降
(3)小亮同学也改进了B装置,改进的装置如图所示,并按下列操作检验装置的气密性。
关闭装置中的弹簧夹a后,开启分液漏斗活塞b,
水不断往下滴,直至全部流进烧瓶。
根据现象判断该装置(填“漏气”或“不漏气”或“无法确定”),理由是长颈漏斗和烧瓶形成连通器,压强相等,无论装置是否漏气,由于重力作用,水都会往下滴流进烧瓶
23.图表是整理数据、发现其中规律的一种重要工具。
1一18号元素原子最外层电子数与原子序数的关系如下图。
试回答:
(1)第三周期11一18号元素原子最外层电子数变化的趋势是逐渐递增(或从1到8逐渐递增)
(2)图中He与Ne、Ar原子最外层电子数不一样,但都处在每周期的结尾处,从原子结构上分析其原因
最外层都达到相对稳定结构(或最外层电子已填充满)(3)原子的核外电子排布,特别是最外层的电子数目,与元素的化学性质有密切关系。
在一个化学反应中,如果有元素化合价升高,同时就有元素化合价降低。
(4)探究钾元素(原子序数为19)单质与水反应的生成物。
甲同学猜想生成物为KOH和H2;乙同学猜想生成物为KOH和O2,你认为同学的猜想不合理,请从化合价的角度解释原因
乙若生成KOH和O2,则该反应中钾元素的化合价由0价升高到十l价,氧元素的化合价由一2价升高到0价,只有元素化合价升高,没有元素化合价降低。
15.乙烯(C2H4)是石油炼制的重要产物之一。
常温常压时,乙烯是一种气体,它与另一种气体组成的混合物中碳元素的质量分数为87%,则另一种气体可能是
A.H2B.CH4C.C2H2D.CO
C
13.最近科学家制造出原子序数为112号的新元素,其相对原子质量为277,下列有关112号元素的说法正确的是
A.该元素原子的中子数为112
B.该元素原子的质子数为165
C.该元素原子的核外电子数为112
D.该元素原子的核电荷数为277
C
14.二百多年前,法国化学家拉瓦锡用定量的方法研究空气成分,其中一项实验是加热红色氧化汞粉末得到汞和氧气,该反应示意图如下:
下列说法正确的是()
A.氧化汞分解过程中,原子的个数没有发生改变
B.氧化汞分解过程中,分子的种类没有发生改变
C.氧化汞、汞、氧气都是化合物
D.氧化汞、汞、氧气都由分子构成
A
7.下列图示实验操作中,正确的是
A
30.(6分)右图是自然界中的氧循环图,请据此回答下列问题。
(1)请用合理的表达方式写出图中存在的“氧循环”任一个。
(1)氧气通过生物的呼吸作用转化为二氧化碳,二氧化碳通过光合作用转化为氧气。
(2)写出光合作用的化学方程式:
6CO2+6H2O
C6H12O6+6O2
(3)氟里昂在高空中受紫外线辐射产生Cl原子,Cl原子对臭氧层有破坏作用,其过程可表示为:
①Cl+O3→ClO+O2;②ClO+O→Cl+O2,则Cl原子在臭氧反复分解的过程中充当。
(填“反应物”、“生成物”或“催化剂”)
(4)大气中CO2含量的增加会加剧温室效应,有一种将CO2转化的实验流程如下:
实验流程中CO2转化的最终产物为
(填化学式,下同),在此过程中有一可循环利
用的物质是。
C、O2
HCl
31、新闻链接:
2005年3月19日,某校3位学生在实验操作中不慎将钠与水接触,引发火灾…………
阅读了上述新闻之后,好奇的唐唐猜测:
金属钠能与水发生反应。
她通过查找资料获得了以下信息:
①钠常温下在空气中易氧化成氧化钠(Na2O),氧化钠可与水化合生成相应的碱;
②钠能与水剧烈反应,放出大量的热,化学方程式为:
2Na+2H2O=2NaOH+H2↑。
她在老师的指导下设计并进行了实验,并做了如下实验记录:
①取一空矿泉水瓶,加入纯净水,仅留一小段空隙,如右图一所示;
②用手挤压矿泉水瓶,除去里面的空气,如右图二所示;
③在胶塞上固定一根大头针,用针扎起一块金属钠,如右图三所示;
④迅速用胶塞塞住挤瘪的瓶口,倒置,如右图四所示;
⑤待完全反应后,打开瓶塞,检验产生的气体;
⑥在矿泉水瓶中滴入数滴A试剂,溶液呈红色。
请根据唐唐的实验过程与实验记录,回答以下问题:
(1)写出试剂A的名称:
酚酞试液
(2)写出氧化钠与水反应的化学方程式:
Na2O+H2O==2NaOH
(3)为什么在实验步骤②中要除去矿泉水瓶中的空气?
避免检验气体时引起爆炸或反应时引起爆炸
;
(4)本实验中,对取用的金属钠的大小是否有要求,为什么?
有要求。
如金属钠太大,生成的气体过多,瓶内压强会冲走瓶塞,使实验失败;如金属钠太小,生成的气体过少,导致后续实验无法进行。
12某研究性学习小组设计的实验装置(如右图),既可用于制取气体,又可用于验证物质性质。
(1)写出仪器A和B的名称:
A:
;B:
。
A:
分液漏斗B:
锥形瓶
(2)当打开K1、关闭K2时,利用Ⅰ、Ⅱ装置可直接进行的实验是(填序号)。
①大理石与稀盐酸反应制取二氧化碳
②锌与稀硫酸反应制取氢气②
小颖认为在不改变Ⅰ、Ⅱ装置的仪器及位置的前提下,该装置可用于双氧水制取氧气,她的做法是;
在装置II中装满水后再进行制取
实验室还可以用高锰酸钾制取氧气,化学方程式为。
2KMnO4
K2MnO4+MnO2+O2↑
(3)当打开K2、关闭K1时,利用Ⅰ、Ⅲ装置可验证二氧化碳与水反应,生成了碳酸,此时试管中盛放的物质是,可以观察到的现象是
(C为干燥管,用于防止液体倒吸)。
紫色石蕊试液紫色石蕊试液变红
10.硝化甘油(C3H5N3O9)可用于治疗心绞痛,因为它在人体内被缓慢氧化生成A气体:
4C3H5N3O9+5O2=12A+12CO2+10H2O
则A的化学式为
A.NOB.NO2C.N2D、N2O
A
11.Y2BaCu6O10是一种高温超导材料。
该化合物中,Y、Ba、O三种元素的化合价依次为
+3、+2、-2价,则铜元素的化合价为
A.0价B.+1价
C.+2价D.+3价
C
6.下列结构示意图中表示原子的是
A.B.C.D.
B
10.水分子分解的微观过程如右图所示。
下列说法错误的是
A.原子是化学变化中的最小粒子
B.在化学反应前后,分子和原子的个数都不变
C.在化学变化中,分子可以再分,原子不能再分
D.在一定条件下,水能分解生成氢气和氧气
B
11.木糖醇(C5H12O5)是一种新型甜味剂。
下列说法错误的是
A.木糖醇属于化合物
B.木糖醇中C、H、O三种元素的原子个数比为
5:
12:
5
C.一个木糖醇分子中含有22个原子
D.一个木糖醇分子是由5个碳原子、2个氧原子和5个水分子构成的
D
9.根据下列四种粒子的结构示意图,所获取的信息不正确的是
①②③④
A.它们表示三种元素
B.②③的化学性质相同
C.②表示的元素是金属元素
D.①表示的是原子,而④表示的是阴离子
B
12.艾滋病的蔓延已经成为影响人们生活、阻碍经济发展的一大社会公害。
2005年澳大利亚科研人员发现维生素P能封住病毒的侵占途径,从而有效地抵抗HI-1病毒(艾滋病毒)、SARS病毒。
已知维生素P的化学式为C27H30O16,关于维生素P的叙述中正确的是
①维生素P是由碳、氢、氧三种元素组成的有机物
②维生素P是由27个碳原子、30个氢原子和16个氧原子构成
③维生素P中碳、氢、氧三种元素的质量比为27:
30:
④将维生素P在足量的氧气中充分燃烧,产物为CO2和H2O
A.①②B.①④
C.②③D.③④
B
14.右图是用比例模型来表示物质间发生化学
变化的微观示意图。
图中“”、“”
分别表示两种元素的原子,能用该图示表示的
一定条件
化学反应是
A
16.科学家发现在特殊条件下,水能表现出许多有趣的结构和性质。
一定条件下给水施加一个弱电场,常温常压下水结成冰,俗称“热冰”,下图为其计算机模拟图。
下列说法正确的是
A.水结成“热冰”的过程中原子个数发生变化
B.上述变化过程中分子间间隔没有发生变化
C.在弱电场下,水分子运动从无序转变为有序
D.利用该性质,人们在常温常压下可建成溜冰场水
CD
19.在化学反应A2+BC=B+A2C中,
反应物BC与生成物
B的质量关系如右图所示。
将2gA2与80gBC恰好完全反
应,则生成A2C的质量是
A.64gB.18g
C.80gD.9g
B
22.我们周围的物质世界是由100多种元素组成的,为了便于研究元素的性质和用途,也需要寻求它们之间的内在规律性。
为此,科学家根据元素的结构和性质,将它们科学有序排列成元素周期表的形式。
下表是元素周期表中的一部分,表中的元素是人体生命活动的常量元素。
族
周期
ⅠA
1
1H
氢
ⅡA
ⅢA
ⅣA
ⅤA
ⅥA
ⅦA
2
6C
碳
xN
氮
8O
氧
3
llNa
钠
12Mg
镁
15P
磷
16S
硫
17C1
氯
4
19K
钾
20Ca
钙
……
试根据上表回答下列问题:
(1)氮元素的核电荷数x=。
(2)与钠元素化学性质相似的元素为。
(3)氧、氯、硫、磷在化学反应中一般
易电子,趋向达到相对稳定结构。
(4)分析上表可发现:
每一横行元素从左向右排列所遵循的一条规律是
22.
(1)7
(2)K(或钾)(3)得到
(4)核电荷数依次增大排列
27.请结合下列实验常用装置,回答有关问题。
ABCDE
(1)写出图中标有字母的仪器名称:
a__________。
(2)若用高锰酸钾制取氧气,应选用的发生装置是__________(填“A”、“B”或“C”),在加入药品前,应首先,反应的化学方程式是。
(3)如果用E装置收集氧气,则气体从_________端进入(填“b”或“c”)。
(4)实验室如用块状固体和液体无需加热制取气体,可将B装置改进为C装置(多孔隔板用来放块状固体),其优点是。
27.
(1)长颈漏斗
(2)A检查气密性
2KMnO4K2MnO4+MnO2+O2↑
(3)b
(4)可以随时控制气体的发生
25.(5分)
(1)下列微粒模型示意图可能代表水分子的是(选填字母序号)。
ABCD
(2)利用
(1)的结论,通过观察左下图,试回答下列问题。
①框内代表的物质是
③请描述框内离子与分子结合时的特点
Na+Cl-
25.(5分)
(1)B
(2)①氯化钠溶液
(3)钠离子与水分子中氧原子相互吸引,氯离子与水分子中氢原子相互吸引
30.(6分)“化学反应条件的控制是实验灵魂”。
某校化学兴趣小组在老师指导下,进行了“影响
双氧水分解因素”的实验。
请你帮助回答下列问题。
(1)取两支大试管,分别倒入适量的6%、15%的双氧水,再加入等量的MnO2,各收集一小试气体,发现浓度大的先收集满。
该操作过程中合理的排列顺序是(选填序号)
。
①检验装置的气密性
②待有连续稳定气泡再排水集气
③将水槽中待收集气体的小试管注满水
④旋紧连有导管的单孔胶塞
⑤向大试管内倒入适量双氧水再加入少许MnO2粉末
(2)用试管进行排水法集气时,主要出现了如下图示所示的4种操作,其中合理的是。
A B C D
(3)取a、b两支试管加入等体积6%的双氧水,再分别加入少许MnO2粉末、CuO粉末,发现a中比b中产生气泡多且快。
随即用带火星的木条分别悬空伸入试管内,发现a中火星复燃,b中火星仅发亮但不复燃。
由此得出影响双氧水分解的因素是
(4)再取一支试管倒入适量6%的双氧水,仔细观察溶液内有少量细小气泡浮起;然后将该支试管浸入约80℃的热水中,溶液内气泡明显增多。
这时将带火昨星的木条悬空伸入试管内,却不能复燃。
试对比第(3)题a中火星复燃的现象,分析两者现象差异的根本
得分
原因是。
30.(6分)
(1)①③⑤④②(或③①⑤④②)
(2)AC
(3)催化剂种类不同,催化效果不同
(4)单位时间内产生氧气的浓度不同(或“产生氧气的速率不同”)
12.下列实验现象描述错误的是
A.铁丝在氧气中燃烧火星四射
B.硫在氧气中燃烧产生蓝紫色火焰
点燃
C.红磷在氧气中燃烧产生白雾
D.铝丝浸入硫酸铜溶液表面有红色物质生成
13.根据化学方程式:
2H2S+3O2====2H2O+2X,推知X的化学式是
A.SB.SO2C.SO3D.H2SO4
14.今年世界水日的主题是“应对水短缺”。
下列应对水短缺的措施:
①推广使用无磷洗衣粉;②加强工业废水的达标排放;③加快生活污水净化处理的建设;④合理使用农药和化肥;⑤提倡节约用水,合理的的是
A.①②③B.①②④⑤
C.②③④⑤D.①②③④⑤
20.分别表示X、Y、Z三种不同的气体分子,其在一定条件下
反应前后的变化如右图所示:
下列叙述错误的是
A.分子是在不断运动的
B.分子之间有间隔的
C.该反应可表示为3X+Y=2Z
D.一个Z分子由三个原子构成
21.人类生存需要清新的空气。
下列情况不会造成空气污染的是
A.绿色植物的光合作用
B.汽车排放大量的尾气
C.大量燃烧化石燃料
D.更多地利用太阳能、风能
26.用数字和化学符号填空:
⑴氯原子;⑵2个钠离子;⑶3个二氧化碳分子;
⑷-2价的硫元素;⑸保持水的化学性质的最小粒子。
-2
26.①Cl②2Na+③3CO2④S
⑤H2O
31.A、B、C、D四种元素,A元素的原子核外只有一个电子,B元素是地壳中含量最高的元素,幼儿和青少年缺少C元素会得佝偻病,D元素的单质是空气中含量最多的气体。
写出A、B、C三种元素的名称或符号A__①__、B___②____、C__③____;。
D元素单质的名称或化学式是____④___;A、B、C三种元素组成的一种化合物的化学式是__⑤_____。
31.①H(氢)②O(氧)③Ca(钙)④N2(氮气)⑤HNO3或NH4NO3
32.研究物质时常对物质进行分类,以便对同类物质的组成、性质等进行深入研究。
请从下列物质中选出一种物质,写出该物质与其他物质不同的理由(一种物质可选用一次,也可选用多次)。
物质组
选出物质
理由
CuO2N2CO
32.(4分)
选出物质
理由
Cu
常温下是固体
Cu
红色
CO
为化合物
O2
可助燃
36.某化学兴趣小组的同学利用下列装置进行实验室制取气体的探究(浓硫酸有吸水性,是干燥剂)
请你参与探究并回答下列问题。
⑴完成下表:
气体
药品
装置组合
反应的化学方程式
氧气
氯酸钾和二氧化锰
氢气
A、C
二氧化碳(干燥)
大理石和稀盐酸
⑵常温下NO是一种无色、难溶于水的气体,密度比空气略大,在空气中能与氧气迅速反应生成红棕色的NO2气体(2NO+O2==2NO2)。
为了收集纯净的NO气体,利用右图所示仪器Ⅰ、Ⅱ,用胶管将_①_(填导管口字母)与c相连组成收集装置.收集时,应先在Ⅰ中②。
36.⑴
药品
装置组合
MnO2
△
反应的化学方程式
BC/BD/BED
2KClO3=====2KCl+3O2↑
锌和稀硫酸
Zn+H2SO4===ZnSO4+H2↑
AED
CaCO3+2HCl=CaCl2+CO2↑+H2O
⑵①b②加满水
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 初三 期中考试 化学 复习资料
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
