 最新高中化学高一化学几种重要的金属化合物测试题 精.docx
最新高中化学高一化学几种重要的金属化合物测试题 精.docx
- 文档编号:1140092
- 上传时间:2022-10-17
- 格式:DOCX
- 页数:11
- 大小:48.08KB
最新高中化学高一化学几种重要的金属化合物测试题 精.docx
《最新高中化学高一化学几种重要的金属化合物测试题 精.docx》由会员分享,可在线阅读,更多相关《最新高中化学高一化学几种重要的金属化合物测试题 精.docx(11页珍藏版)》请在冰豆网上搜索。
最新高中化学高一化学几种重要的金属化合物测试题精
第二节几种重要的金属化合物
5分钟训练(预习类训练,可用于课前)
1.对下列物质按不同的分类方法进行分类。
Al2O3、Al、AlCl3、Al(OH)3、Fe2O3、FeO、Fe3O4、CaO、CuO、Fe、Cu、Ca、FeSO4、Fe2(SO4)3、Fe(OH)2、Fe(OH)3、Ca(OH)2、Cu(OH)2、CuSO4、CuCl2
思路解析:
物质的分类可以按不同的分类标准进行分类。
答案:
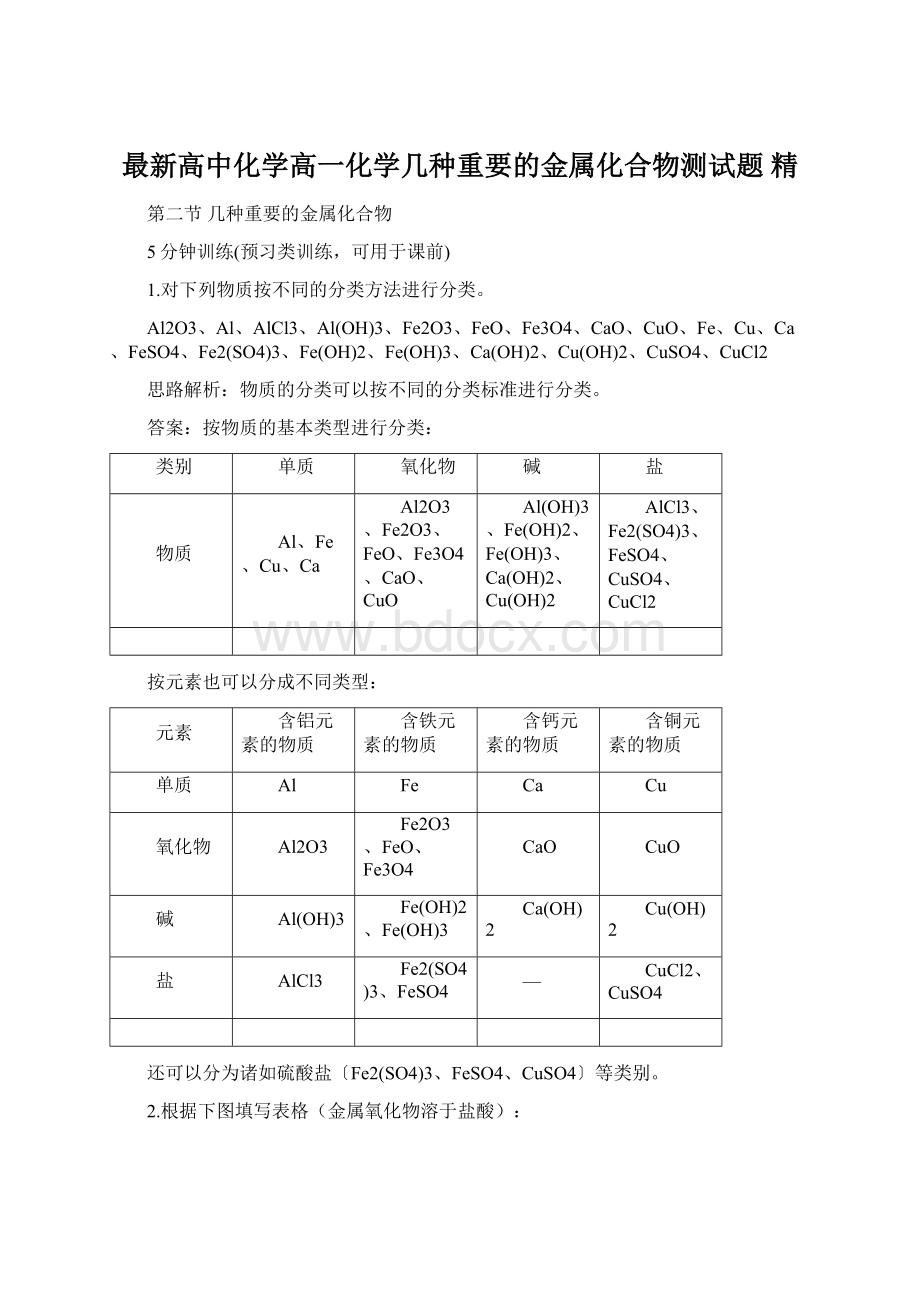
按物质的基本类型进行分类:
类别
单质
氧化物
碱
盐
物质
Al、Fe、Cu、Ca
Al2O3、Fe2O3、FeO、Fe3O4、CaO、CuO
Al(OH)3、Fe(OH)2、Fe(OH)3、Ca(OH)2、Cu(OH)2
AlCl3、Fe2(SO4)3、FeSO4、CuSO4、CuCl2
按元素也可以分成不同类型:
元素
含铝元素的物质
含铁元素的物质
含钙元素的物质
含铜元素的物质
单质
Al
Fe
Ca
Cu
氧化物
Al2O3
Fe2O3、FeO、Fe3O4
CaO
CuO
碱
Al(OH)3
Fe(OH)2、Fe(OH)3
Ca(OH)2
Cu(OH)2
盐
AlCl3
Fe2(SO4)3、FeSO4
—
CuCl2、CuSO4
还可以分为诸如硫酸盐〔Fe2(SO4)3、FeSO4、CuSO4〕等类别。
2.根据下图填写表格(金属氧化物溶于盐酸):
完成下表:
金属氧化物
颜色
化学方程式
离子方程式
固体
溶液
MgO
Fe2O3
CuO
思路解析:
几种金属氧化物固体和溶液的颜色都可以通过观察得出,而化学方程式的书写则可根据金属氧化物与酸反应的规律——生成盐和水来完成,离子方程式则将盐酸和金属的氯化物都拆开就可以了。
答案:
见下表。
金属氧化物
颜色
化学方程式
离子方程式
固体
溶液
MgO
白色
无色
MgO+2HCl====MgCl2+H2O
MgO+2H+====Mg2++H2O
Fe2O3
暗红色
浅黄色
Fe2O3+6HCl====3FeCl3+3H2O
Fe2O3+6H+====2Fe3++3H2O
CuO
黑色
蓝色
CuO+2HCl====CuCl2+H2O
CuO+2H+====Cu2++H2O
3.氢氧化亚铁与氢氧化铁都是铁的氢氧化物,它们有什么异同?
思路解析:
从它们的物理性质与化学性质的不同方面来进行比较,同时对它们之间的转化关系也应该清楚。
答案:
列表将它们的性质与变化比较如下:
氢氧化铁
氢氧化亚铁
物理性质
红褐色,难溶于水
白色,难溶于水
化学性质
具有碱的通性
具有碱的通性,易被氧化为氢氧化铁
联系
4Fe(OH)2+O2+2H2O====4Fe(OH)3(白色迅速变为灰色、绿色,最终成为红褐色)
4.氢氧化铝与其他的氢氧化物不同,既能与酸反应生成盐和水,又能与碱反应生成盐和水,试用离子方程式表示它与酸和碱反应的原理。
思路解析:
教材上既有氢氧化铝与盐酸和氢氧化钠反应的实验又有化学方程式,我们只需将化学方程式改写成离子方程式即可。
答案:
Al(OH)3+3H+====Al3++3H2O;Al(OH)3+OH-====+2H2O。
10分钟训练(强化类训练,可用于课中)
1.在食品加工或餐饮业中使用量特别要注意严加控制的物质是()
A.氯化钠B.谷氨酸钠(味精)C.碳酸氢钠D.亚硝酸钠
思路解析:
几种钠盐中,氯化钠和碳酸氢钠是学生非常熟悉的,谷氨酸钠的化学名称学生虽然不熟悉,但后面所附的俗名却是学生生活中常见的物质,只有亚硝酸钠学生可能了解不多,可用排除的方法来解答。
答案:
D
2.把水滴入下列物质中,不产生气态生成物的是()
A.过氧化钠B.金属钠C.氧化钠D.金属钾
思路解析:
与水反应的物质,是近年高考中的热点。
选项中的四种物质都可以和水发生反应。
过氧化钠与水有氧气产生;金属钠和钾与水有氢气产生。
答案:
C
3.下列叙述正确的是()
A.草木灰的主要成分是K2CO3
B.土壤中钾元素的含量较少,因此需要补充
C.钾肥宜在下雨前施用,以便溶解吸收
D.为了使农作物有效吸收N、P、K等元素,钾肥宜跟NH4H2PO4等混合施用
思路解析:
土壤中的钾元素含量并不少,只是可被植物直接吸收的部分较少;钾肥都是易溶于水的盐,雨前施用,容易被雨水淋失;钾肥特别是碳酸钾不能与铵盐混用,因为二者发生反应后,使铵盐转化为氨气,逸入空气中。
答案:
A
4.向下列溶液滴加稀硫酸,生成白色沉淀,继续滴加稀硫酸,沉淀又溶解的是()
A.Na2SiO3B.BaCl2C.FeCl3D.NaAlO2
思路解析:
硫酸与选项中物质的反应:
Na2SiO3+H2SO4====Na2SO4+H2SiO3↓;BaCl2+H2SO4====BaSO4↓+2HCl;2NaAlO2+H2SO4+2H2O====2Al(OH)3↓+Na2SO4,
2Al(OH)3+3H2SO4====Al2(SO4)3+6H2O。
答案:
D
5.下列物质中,可用于治疗胃酸过多的是()
A.碳酸钠B.氢氧化铝C.氢氧化钠D.碳酸钡
思路解析:
治疗胃酸过多,一方面要能消耗酸,另一方面必须是无毒、对人体没有强刺激性甚至腐蚀作用,也不能产生大量气体,使胃中充气过多。
答案:
B
6.在硝酸铝和硝酸镁的混合溶液中,逐滴加入稀氢氧化钠溶液,直至过量。
下列表示氢氧化钠加入量(X)与溶液中沉淀物的量(Y)的关系示意图中正确的是()
思路解析:
反应分为两个阶段:
(1)Al(NO3)3+3NaOH====Al(OH)3↓+3NaNO3,
Mg(NO3)2+2NaOH====Mg(OH)2↓+2NaNO3;
(2)Al(OH)3+NaOH====NaAlO2+2H2O。
沉淀首先是逐渐增多,达到最大值后,过量的氢氧化钠又将氢氧化铝沉淀溶解。
答案:
C
7.拉曼光谱证实溶液中不存在,实际存在[Al(OH)4]-。
200mL0.2mol·L-1Na[Al(OH)4]溶液与250mL0.2mol·L-1H2SO4混合,完全反应后,溶液中Al3+与物质的量之比为()
A.4∶5B.2∶3C.2∶5D.1∶2
思路解析:
2Na[Al(OH)4]+H2SO4====Na2SO4+2Al(OH)3↓+2H2O,
2Al(OH)3+3H2SO4====Al2(SO4)3+6H2O。
按反应方程式分两步计算:
第一步,硫酸过量,剩余硫酸为0.3mol,生成氢氧化铝0.2mol;第二步,两种反应物恰好反应,生成硫酸铝,此时溶液中Al3+为0.2mol,为0.5mol。
答案:
C
8.若将含HCl0.20mol的稀盐酸滴入0.15molNa2CO3的溶液中,经充分反应后,溶液中各溶质的物质的量为(单位:
mol)()
Na2CO3
HCl
NaCl
NaHCO3
A
0
0
0.18
0.10
B
0.5
0
0.20
0
C
0
0
0.20
0.10
D
0
0.18
0.15
0.15
思路解析:
盐酸和Na2CO3反应,与滴加顺序有关,应引起足够重视。
分析本题可知两条重要信息:
(1)因稀盐酸是滴入到Na2CO3溶液中的,所以这种情况下盐酸和碳酸钠的反应是分步进行的:
Na2CO3+HCl====NaCl+NaHCO3①
NaHCO3+HCl====NaCl+CO2↑+H2O②
(2)反应物盐酸的量相对于Na2CO3的第一步反应是过量的(余0.18mol),相对于Na2CO3的完全反应是不足量的(差0.10mol)。
这样利用题示信息进一步分析可知:
充分反应后反应物Na2CO3和HCl都已消耗完全;两步反应中的HCl都转化为NaCl,其转化关系为1∶1(物质的量之比)。
因此生成的NaCl为0.2mol;而NaHCO3的量则经一步反应生成0.15mol(按不足量),第二步反应又转化了(放CO2)0.18mol,最后剩0.10mol。
答案:
C
9.今用铝、稀硫酸和氢氧化钠溶液为原料,实验室制备一定量的氢氧化铝。
分别采用如下化学方程式所表示的两种方法:
①2Al+3H2SO4====Al2(SO4)3+3H2↑Al2(SO4)3+6NaOH====2Al(OH)3↓+3Na2SO4
②2Al+2NaOH+2H2O====2NaAlO2+3H2↑2NaAlO2+H2SO4+2H2O====2Al(OH)3↓+Na2SO4
(1)请问上述哪一种方法比较节约试剂。
(提示:
以每生产2molAl(OH)3所耗费的试剂用量予以说明)
(2)原料相同,请设计一种更为节约试剂的方法。
(以方程式表示,并说明其可以最节约试剂的根据)
思路解析:
(1)从化学方程式看出,同样是制备2mol的Al(OH)3,方法①所需原料为:
2molAl,3molH2SO4,6molNaOH;而方法②所需原样为:
2molAl,1molH2SO4,2molNaOH。
(2)①2Al+3H2SO4====Al2(SO4)3+3H2↑
②2Al+2NaOH+2H2O====2NaAlO2+3H2↑
③Al2(SO4)3+6NaAlO2+12H2O====8Al(OH)3↓+3Na2SO4
由方程式看出,制备8mol的Al(OH)3,所需原料为:
8molAl、3molH2SO4、6molNaOH。
相当于制备2molAl(OH)3,所需量为:
2molAl,3/4molH2SO4,3/2molNaOH,其用量为最少。
答案:
(1)第②种方法比较节约试剂。
(2)见解析。
(方程式①和②的顺序可交换)
10.埋藏在地下的青铜器锈蚀过程可以表示为:
(1)青铜器锈蚀过程中的产物有__________________________________________________。
(2)青铜器出土后防止青铜器继续锈蚀的关键是____________________________________。
思路解析:
青铜器锈蚀过程中的产物从图中可以清楚看出。
从图中看出锈蚀反应的条件是存在O2、水及酸性气体如CO2、HCl等,其中O2是关键。
答案:
(1)CuCl,Cu2O,Cu2(OH)2CO3,Cu4(OH)6Cl2等
(2)与H2O和O2等隔绝
快乐时光
唯一的乞丐
一群犹太人站在巷子里,每人都在为自己祝福,有的想成为富翁,有的想娶富翁的女儿,
有的祝愿妻子能生个小孩。
在这群人中间有一个乞丐,他也喃喃地对天祈祷着什么。
“喂!
”有人问他,“您为自己祈祷什么呀?
”
“我祝愿自己是这座城市里唯一的乞丐。
”
30分钟训练(巩固类训练,可用于课后)
1.向紫色石蕊溶液中加入过量Na2O2粉末,振荡,可观察到的现象为()
A.溶液仍为紫色B.溶液最终变为蓝色
C.最终溶液褪色,而无其他现象D.溶液中有气泡产生,溶液最终变为无色
思路解析:
2Na2O2+2H2O====4NaOH+O2↑,有氧气产生,故溶液中有气泡放出,又因为Na2O2有漂白性,故溶液最终变为无色。
不能只考虑反应生成NaOH,认为溶液变为蓝色,而忽略Na2O2有漂白性。
答案:
D
2.向饱和Na2CO3溶液中通入过量的CO2,将出现什么现象?
为什么?
思路解析:
CO2将与Na2CO3、H2O反应生成NaHCO3,Na2CO3+H
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 最新高中化学高一化学几种重要的金属化合物测试题 最新 高中化学 高一化学 重要 金属 化合物 测试
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 12处方点评管理规范实施细则_精品文档.doc
12处方点评管理规范实施细则_精品文档.doc
 17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
