 备战高考化学与氮及其化合物有关的压轴题.docx
备战高考化学与氮及其化合物有关的压轴题.docx
- 文档编号:11389662
- 上传时间:2023-02-28
- 格式:DOCX
- 页数:26
- 大小:277.63KB
备战高考化学与氮及其化合物有关的压轴题.docx
《备战高考化学与氮及其化合物有关的压轴题.docx》由会员分享,可在线阅读,更多相关《备战高考化学与氮及其化合物有关的压轴题.docx(26页珍藏版)》请在冰豆网上搜索。
备战高考化学与氮及其化合物有关的压轴题
备战高考化学与氮及其化合物有关的压轴题
一、氮及其化合物练习题(含详细答案解析)
1.氮的氧化物和硫的氧化物是主要的大气污染物,烟气脱硫脱硝是环境治理的热点问题。
回答下列问题:
(1)目前柴油汽车都用尿素水解液消除汽车尾气中的NO,水解液中的NH3将NO还原为无害的物质。
该反应中氧化剂与还原剂物质的量之比为___。
(2)KMnO4/CaCO3浆液可协同脱硫,在反应中MnO4-被还原为MnO42-。
①KMnO4脱硫(SO2)的离子方程式为___。
②加入CaCO3的作用是___。
③KMnO4/CaCO3浆液中KMnO4与CaCO3最合适的物质的量之比为___。
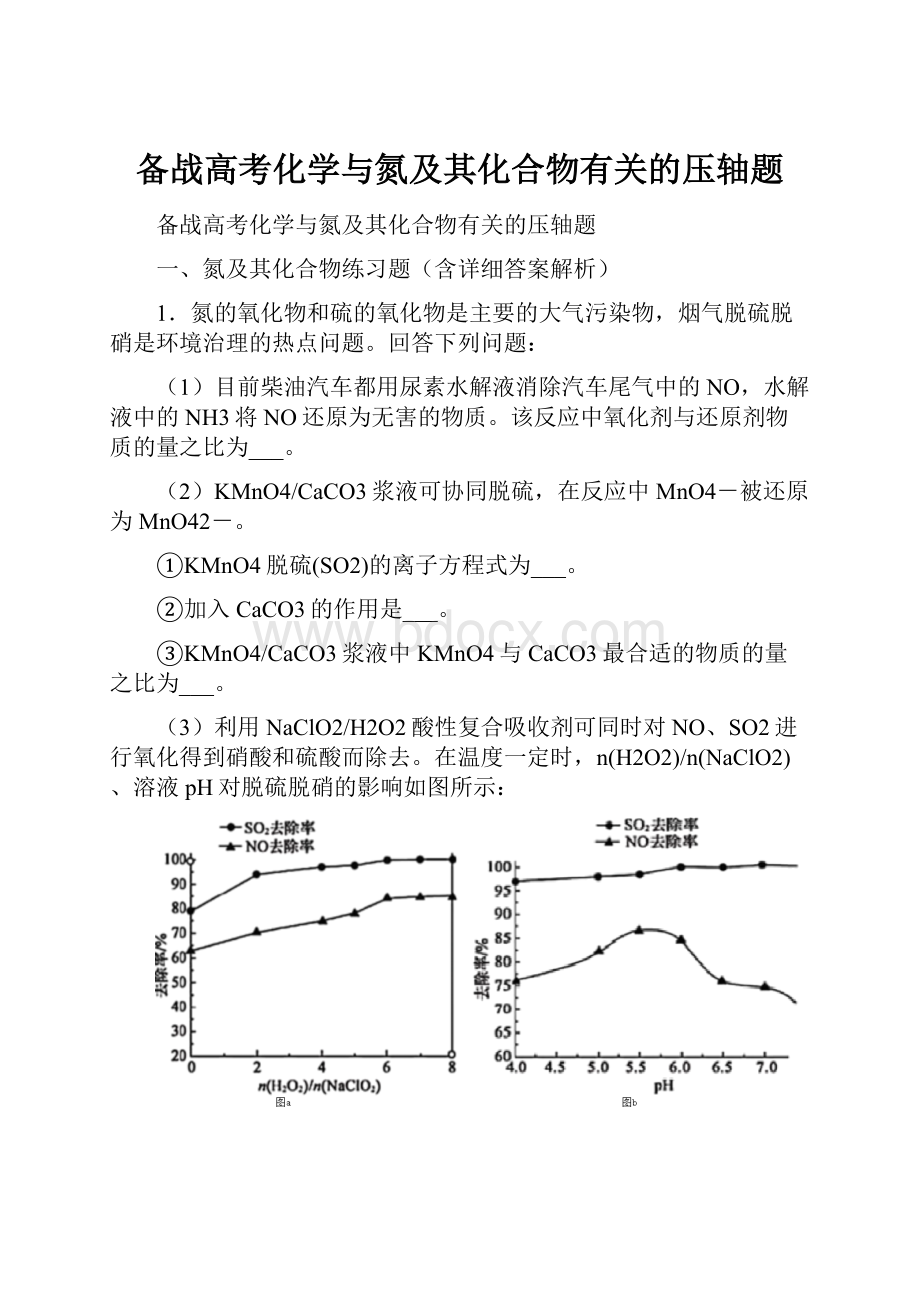
(3)利用NaClO2/H2O2酸性复合吸收剂可同时对NO、SO2进行氧化得到硝酸和硫酸而除去。
在温度一定时,n(H2O2)/n(NaClO2)、溶液pH对脱硫脱硝的影响如图所示:
图a和图b中可知脱硫脱硝最佳条件是___。
图b中SO2的去除率随pH的增大而增大,而NO的去除率在pH>5.5时反而减小,请解释NO去除率减小的可能原因是___。
【答案】2:
3SO2+2MnO4-+2H2O===SO42-+2MnO42-+4H+消耗脱硫过程中的氢离子,有利于平衡正向移动1:
1n(H2O2):
n(NaClO2)=6:
1,pH值在5.5—6.0可能NO的还原性减弱或则可能是NaClO2、H2O2的氧化性减弱
【解析】
【分析】
⑴根据氧化还原反应得出氧化剂和还原剂的比例关系。
⑵根据氧化还原反应原理写离子方程式,生成的氢离子和碳酸钙反应,消耗氢离子,利于平衡正向移动,根据比例关系得出高锰酸钾和碳酸钙的比例。
⑶根据图像信息得出脱硫脱硝最佳条件,用氧化还原反应的强弱随pH变化的影响分析减弱的原因。
【详解】
⑴水解液中的NH3将NO还原为无害的物质氮气,根据氧化还原反应原理,氨气化合价升高3个价态,为还原剂,NO化合价降低2个价态,为氧化剂,根据升降守恒配平原理,因此氨气前配2,NO前面配系数3,因此该反应中氧化剂与还原剂物质的量之比为2:
3,故答案为:
2:
3。
⑵①KMnO4脱硫(SO2)反应生成锰酸根和硫酸根,离子方程式为SO2+2MnO4-+2H2O===SO42-+2MnO42-+4H+,故答案为:
SO2+2MnO4-+2H2O===SO42-+2MnO42-+4H+。
②反应过程中生成了硫酸,加入CaCO3的作用是消耗脱硫过程中的氢离子,有利于平衡正向移动,故答案为:
消耗脱硫过程中的氢离子,有利于平衡正向移动。
③2molKMnO4反应生成4mol氢离子,4mol氢离子消耗2mol碳酸钙,因此CaCO3浆液中KMnO4与CaCO3最合适的物质的量之比为1:
1,故答案为1:
1。
⑶根据图中的转化率和去除率关系,可知脱硫脱硝最佳条件是n(H2O2):
n(NaClO2)=6:
1,pH值在5.5—6.0;NO在pH>5.5时可能NO的还原性减弱或则可能是NaClO2、H2O2的氧化性减弱,故答案为:
n(H2O2):
n(NaClO2)=6:
1,pH值在5.5—6.0;可能NO的还原性减弱或则可能是NaClO2、H2O2的氧化性减弱。
2.随着工业的发展,酸雨已经称为全球性的环境问题。
(1)当雨水的pH___________,我们称它为酸雨。
(2)用化学方程式来表示酸雨形成的主要途径之一:
_____________________,_______________。
(3)常温下测得某次酸雨样品的pH=5,该样品放置一段时间后,酸性略有增强,其原因可能是___________________________。
(4)写出一条减少二氧化硫排放的措施_________________________________。
(5)检验某无色溶液中是否存在SO42-的方法是_____________________________。
【答案】<5.6SO2+H2O
H2SO32H2SO3+O2=2H2SO4酸雨中的亚硫酸被氧化成硫酸了燃料脱硫(合理即可)取样于试管中,先滴加盐酸无现象,再滴加BaCl2溶液,出现白色沉淀,说明有SO42-,如无沉淀,则不存在SO42-
【解析】
【分析】
(1)雨水的pH<5.6时称为酸雨,据此解答;
(2)酸雨形成的主要途径有两种,一种的雨水和二氧化硫反应生成亚硫酸,亚硫酸与空气中氧气反应生成硫酸,另一种途径为二氧化硫在空气中飘尘的作用下与氧气反应生成三氧化硫,三氧化硫与雨水反应生成硫酸,据此解答;
(3)亚硫酸酸性弱,而强酸酸性强,酸雨中的亚硫酸可能被氧化成硫酸,据此解答;
(4)减少二氧化硫排放的措施有用氨水吸收尾气,双碱脱硫,燃料脱硫等,据此解答;
(5)检验某无色溶液中是否存在SO
的方法是取样于试管中,先滴加盐酸无现象,滴加盐酸主要目的是排出银离子、碳酸根、亚硫酸根等离子的干扰,再滴加BaCl2溶液,出现白色沉淀,说明有SO42-,如无沉淀,则不存在SO42-,据此解答;
【详解】
(1)由于雨水中含有溶液的二氧化硫生成亚硫酸,因此当雨水的pH<5.6,我们称它为酸雨,故答案为:
<5.6;
(2)用化学方程式来表示酸雨形成的主要途径有两种,一种的雨水和二氧化硫反应生成亚硫酸,亚硫酸与空气中氧气反应生成硫酸,另一种途径为二氧化硫在空气中飘尘的作用下与氧气反应生成三氧化硫,三氧化硫与雨水反应生成硫酸,前者的反应方程式为SO2+H2O
H2SO3,2H2SO3+O2=2H2SO4;
(3)常温下测得某次酸雨样品的pH=5,该样品放置一段时间后,酸性略有增强,亚硫酸酸性弱,而强酸酸性强,其原因可能是酸雨中的亚硫酸被氧化成硫酸了;
(4)减少二氧化硫排放的措施有:
用氨水吸收尾气,双碱脱硫,燃料脱硫等;
(5)检验某无色溶液中是否存在SO42-的方法是取样于试管中,先滴加盐酸无现象,滴加盐酸主要目的是排出银离子、碳酸根、亚硫酸根等离子的干扰,再滴加BaCl2溶液,出现白色沉淀,说明有SO42-,如无沉淀,则不存在SO42-。
【点睛】
亚硫酸酸性弱,而强酸酸性强,酸雨中的亚硫酸可能被氧化成硫酸而酸性增强。
3.某港口化学品堆场发生火灾,消防队在未被告知着火可燃物类别的情况下,用水灭火时,发生了剧烈爆炸。
事后有关部门初步认定危化品部分清单:
钾、钠、氯酸钾、烧碱、氯化铵。
试回答:
⑴请你分析用水灭火时,随后发生了剧烈爆炸的原因是_____________________________。
⑵请写出氯化铵中NH4+的检验方法____________________________(简要说明操作步骤)。
⑶钠燃烧产物中可作为消防员呼吸面具供氧剂的是_________________(写化学式)。
⑷硝酸钾受热分解产生KNO2和O2,写出该反应的化学方程式______________________。
【答案】钠、钾能与水发生剧烈的放热反应,并释放出氢气。
氯酸钾受热分解产生氧气,氢气和氧气混合受热发生爆炸将氯化铵溶于水,取少量溶液于试管中,滴入浓氢氧化钠溶液并加热,在试管口上方用湿润的红色石蕊试纸检验,若发现试纸变蓝,则说明该溶液中含有NH4+Na2O22KNO3
2KNO2+O2↑
【解析】
【分析】
钠、钾等物质遇水会发生剧烈反应并产生氢气,而氯酸钾分解会产生氧气,氢氧混合受热后会发生爆炸,后面再根据要求来作答即可。
【详解】
(1)根据分析,钠、钾与水发生剧烈反应并放出氢气,而氯酸钾受热产生氧气,氢气和氧气混合后发生剧烈的爆炸;
(2)铵离子可以通过加水溶解后,加入浓碱并加热的方法来检验,因为高中阶段只有氨气这一种碱性气体;实验操作为:
将氯化铵溶于水,取少量溶液于试管中,滴入浓氢氧化钠溶液并加热,在试管口上方用湿润的红色石蕊试纸检验,若发现试纸变蓝,则说明该溶液中含有NH4+,
(3)过氧化钠可以作呼吸面具中的供氧剂,化学式为Na2O2;
(4)硝酸钾受热分解产生
和
的过程是一个自身氧化还原反应,氮从+5价降低到+3价,得2个电子,氧从-2价升高到0价,失2个电子,据此来写出氧化还原方程式即可:
。
4.2016年10月17日7时30分,我国“神舟十一号”载人飞船顺利升入太空。
此次火箭的主要燃料是偏二甲肼(C2N2H8)和一种氮的氧化物(用R表示),当火箭发射时,这两种燃料会剧烈反应产生大量气体,并释放出大量的热,化学方程式如下(已配平):
C2N2H8+2R=3N2↑+4H2O+2CO2↑
(1)R的化学式是___;已知偏二甲肼中N元素显-2价,H元素显+1价,由此推断,C元素的化合价是___。
(2)该反应的还原剂是___,被还原的元素是___。
(3)若反应生成22.4LCO2(标准状况),则反应转移电子___mol。
(4)火箭发射时,尾部向下喷出的气体会有明显的红棕色,该红棕色气体的化学式可能是___。
(5)高铁酸钠(Na2FeO4)是一种多功能、高效无毒的新型绿色水处理剂。
Na2FeO4能给水消毒利用的是___性。
用Na2FeO4给水消毒、杀菌时得到的Fe3+可以净水,其净水原理与明矾相同,Fe3+净水原理是___(用简要的文字叙述)。
【答案】N2O4-2C2N2H8N2O48NO2氧化性Fe3+是弱碱阳离子,能结合水电离出的氢氧根生成Fe(OH)3胶体,可以吸附水中悬浮物并凝聚沉降
【解析】
【分析】
(1)化学方程式C2N2H8+2R=3N2↑+4H2O+2CO2↑,由原子守恒可得R的化学式;
(2)该反应中N2O4中的N元素从+4价下降到0价,C2N2H8中C和N的化合价升高,可以判断出氧化剂和还原剂;
(3)标准状况下22.4LCO2的物质的量是1mol,生成1molCO2时,有1molN2O4被还原,可以求出转移电子数;
(4)火箭的燃料是两种组分,偏二甲肼和四氧化二氮,四氧化二氮是无色的气体,四氧化二氮在温度升高时会很快的分解为红棕色的二氧化氮气体;
(5)Na2FeO4中铁是铁元素的最高价态,有很强的氧化性。
【详解】
(1)化学方程式C2N2H8+2R=3N2↑+4H2O+2CO2↑,由原子守恒可知,R的化学式为:
N2O4;已知偏二甲肼C2N2H8中N元素显-2价,H元素显+1价,设C的化合价为x,则有2x+8-2×2=0,解得x=-2,C元素的化合价是-2;
(2)该反应中N2O4中的N元素从+4价下降到0价,C2N2H8中C和N的化合价升高,故该反应的还原剂是C2N2H8,氧化剂是N2O4;
(3)标准状况下22.4LCO2的物质的量是1mol,生成1molCO2时,有1molN2O4被还原,N2O4被还原为N2,得8个电子,1molN2O4得8电子,故转移8mol电子;
(4)火箭的燃料是两种组分,偏二甲肼和四氧化二氮,四氧化二氮是无色的气体,四氧化二氮在温度升高时会很快的分解为红棕色的二氧化氮气体,故该红棕色气体的化学式可能是NO2;
(5)化合物中化合价的代数和为0,Na2FeO4中钠元素为+1价,氧元素为-2价,故铁元素为+6价;+6价的铁是铁元素的最高价态,有很强的氧化性,可用于杀菌消毒;杀菌时得到的Fe3+是弱碱阳离子,能结合水电离出的氢氧根生成Fe(OH)3胶体,可以吸附水中悬浮物并凝聚沉降。
5.硝酸是重要的化工原料,在工农业生产和国防上有重要用途。
(1)实验室利用硝石(NaNO3)和浓硫酸共热制取硝酸。
①该反应利用了浓硫酸的_______性;
②该反应的温度不宜太高,原因是(用化学方程式表示)______;
(2)工业上用氨气的催化氧化法制取硝酸,再利用硝酸和氨气反应生产NH4NO3。
①写出氨气的电子式_____;
②写出氨气催化氧化的化学方程式_______;
③在生产过程中,氨催化氧化生成氮氧化物的利用率是80%,氮氧化物被吸收得到硝酸的利用率是85%,则制取80t的NH4NO3需要氨气______t;
(3)某混合酸1L中含1mol的硝酸和2mol的硫酸。
取该混合酸100mL,加入5.6g铁粉充分反应。
①反应中可以生成NO____L(标准状况);
②向反应后的溶液再加入铁粉,能继续溶解铁粉____g。
【答案】高沸点性(或不挥发性)4HNO3=4NO2↑+O2↑+2H2O
4NH3+5O2
4NO+6H2O422.245.6
【解析】
【分析】
(1)利用浓硫酸的高沸点分析;
(2)根据硝酸不稳定能分解分析;
(3)根据氨气转化为硝酸的一系列反应分析氨气的质量。
(4)注意硝酸具有强氧化性,硫酸具有酸性,同时注意铁离子能与铁反应。
【详解】
(1)①浓硫酸制取硝酸时利用浓硫酸的高沸点性(或不挥发性);
②硝酸在温度高时能分解生成二氧化氮和氧气和水,方程式为:
4HNO3=4NO2↑+O2↑+2H2O;
(2).①氨气的电子式为:
;
②氨气和氧气反应生成一氧化氮和水,方程式为:
4NH3+5O2
4NO+6H2O;
③NH3-NO-HNO3-NH4NO3,80t的NH4NO3需要转化为硝酸的的氨气的质量为
=25t,另外需要和硝酸反应的氨气的质量为
=17t,总共氨气的质量为25+17=42t;
(3).①反应的离子方程式为Fe+4H++NO3-=Fe3++NO
+2H2O,根据铁的物质的量为0.1mol,溶液中的氢离子为0.5mol,硝酸根离子为0.1mol分析,铁反应生成0.1mol一氧化氮,标况下的体积为2.24L;
②反应中消耗0.4mol氢离子,和0.1mol硝酸根离子,还剩余0.1mol氢离子和0.1mol铁离子,0.1mol氢离子能反应0.05mol铁,0.1mol铁离子能反应0.05mol铁,故总共反应0.1mol铁,质量为5.6g。
【点睛】
铁和硝酸和硫酸的混合酸反应时,硝酸尽可能表现氧化性,硫酸表现酸性,所以根据离子方程式计算,同时注意反应后的溶液中含有铁离子,同样也能溶解铁。
6.下图中的每一个方格表示有关的一种反应物或生成物,其中X为正盐,A、C、D均为无色气体。
(1)写出有关的物质化学式。
X:
_______C:
_______E:
_______F:
_____
(2)写出反应①的化学方程式_____________________________________
(3)写出反应②的离子方程式_____________________________________
【答案】NH4)2CO3NH3NONO22Na2O2+2CO2=2Na2CO3+O28H++2NO3—+3Cu==3Cu2++2NO↑+4H2O
【解析】
【分析】
X为正盐,A为无色气体,能与Na2O2反应生成无色气体D,则A为CO2,D为氧气,X能与强碱反应生成无色气体C,C与氧气在催化剂的条件下反应生成E,则C为NH3,E为NO,所以X为(NH4)2CO3,碳酸铵受热分解生成氨气、CO2和水,则B为水,NO和氧气反应生成F,F为NO2,F与水反应生成G,则G为硝酸,硝酸与木炭反应生成CO2、NO2和水,硝酸与铜反应生成硝酸铜、NO和水,以此分析解答。
【详解】
(1)根据上述推断,X为(NH4)2CO3,C为NH3,E为NO,F为NO2,故答案:
(NH4)2CO3;NH3;NO;NO2;
(2)根据分析和框图可知反应①是过氧化钠与CO2反应生成碳酸钠和氧气,其化学方程式为2Na2O2+2CO2=2Na2CO3+O2,故答案:
2Na2O2+2CO2=2Na2CO3+O2。
(3)根据分析和框图可知反应②是铜与稀硝酸反应生成硝酸铜、NO和水,反应的离子方程式为8H++2NO3-+3Cu==3Cu2++2NO↑+4H2O,故答案:
8H++2NO3-+3Cu==3Cu2++2NO↑+4H2O。
7.非金属单质A经下图所示的过程可转化为含氧酸D,已知D为强酸,请回答下列问题:
(1)若A在常温下是固体,B是能使品红溶液褪色的有刺激性气味的无色气体:
①D的化学式:
_________;
②在工业生产中,B气体大量排放,被雨水吸收后形成____________污染环境。
(2)若A在常温下为气体,C是红棕色气体。
①C的化学式为:
_________;
②D的浓溶液在常温下可与铜反应并生成C气体,该反应的化学方程式为:
___________,该反应___(填“属于”或“不属于”)氧化还原反应。
【答案】H2SO4酸雨NO2Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O属于
【解析】
【分析】
根据框图,非金属单质A能发生连续氧化,含氧酸D为强酸,对应的是硫和氮等元素的转化。
(1)A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体,则A为S单质,B为SO2,C为SO3,D为H2SO4;
(2)A在常温下为气体,C是红棕色的气体,则A应为N2,B为NO,C为NO2,D为HNO3,根据氧化还原反应的特点判断,据此分析解答。
【详解】
(1)A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体,则A为S单质,B为SO2,C为SO3,D为H2SO4。
①由以上分析可知D是硫酸,化学式为H2SO4,故答案为:
H2SO4;
②在工业生产中大量排放的SO2气体被雨水吸收后形成了酸雨而污染了环境,故答案为:
酸雨;
(2)若A在常温下为气体,C是红棕色的气体,则A应为N2,B为NO,C为NO2,D为HNO3。
①由以上分析可知C为NO2,故答案为:
NO2;
②D的浓溶液在常温下可与铜反应并生成C气体,反应的化学方程式为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,该反应中Cu的化合价升高,N的化合价降低,属于氧化还原反应,故答案为:
Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O;属于。
【点睛】
解答本题的关键是物质的颜色和框图中的“连续氧化”特征,也是解答本题的突破口。
本题的易错点为A的判断,要注意A属于非金属单质。
8.已知A、B、C、D为气体,其中A为黄绿色,D极易溶于水,形成的溶液可使酚酞变红,它们之间的转化关系如下图①所示:
(1)将气体B点燃,把导管伸入盛满气体A的集气瓶,反应过程中的实验现象有_________(填序号)
①放热②黄绿色褪去③瓶口有白雾④瓶口有白烟⑤安静燃烧,发出黄色火焰⑥安静燃烧,发出苍白色火焰
(2)实验室制D的化学方程式为__________________________________。
(3)实验室可用如上图②所示装置收集D,下列叙述正确的是__________(填序号)。
①D气体不能用排水法收集
②干燥管里盛有碱石灰
③图②中的a为干棉花团,其作用是防止氨气逸出
(4)气体D催化氧化的化学方程式为_________________________________。
(5)物质E的化学式是_______;E在下列物质分类中所属的物质种类是_______(填序号)。
①电解质②化合物③混合物④纯净物⑤非电解质⑥盐
检验物质E中阳离子的操作方法______________________________________
【答案】①②③⑥Ca(OH)2+2NH4Cl
CaCl2+H2O+2NH3↑①②4NH3+5O2
4NO+6H2ONH4Cl①②④⑥取E少许于试管,加入浓NaOH溶液,加热,生成无色有刺激性气味的气体,用湿润的红色石蕊试纸检验,试纸变为蓝色,证明E中有NH4+
【解析】
【分析】
为黄绿色气体,应为Cl2,D极易溶于水,形成的溶液可使酚酞变红,应为NH3,A、B、C、D为气体,则B是H2,C是HCl,所以E是NH4Cl,结合对应物质的性质以及题目要求可解答该题。
【详解】
(1)氢气在氯气中安静的燃烧,火焰苍白色,黄绿色逐渐褪去,瓶口有白雾(氯化氢气体与空气中的小水滴结合)出现,燃烧反应都是放热反应,所以选①②③⑥;
(2)实验室制氨气的化学方程式为:
Ca(OH)2+2NH4Cl
CaCl2+H2O+2NH3↑;
(3)氨气极易溶于水,不能用排水法收集,氨气溶于水显碱性,可用碱石灰干燥,图②中的a应为湿润红色石蕊试纸,检验氨气是否收集满,所以答案选①②;
(4)氨气发生催化氧化的化学方程式为:
4NH3+5O2
4NO+6H2O;
(5)E是氯化铵,化学式为NH4Cl,它是化合物,是纯净物,是盐,是电解质,所以答案选①②④⑥,检验铵根离子的操作方法:
取E少许于试管,加入浓NaOH溶液,加热,生成无色有刺激性气味的气体,用湿润的红色石蕊试纸检验,试纸变为蓝色,证明E中有NH4+。
9.A、B、C、D、E各物质的关系如下图所示:
已知:
X能使湿润的红色石蕊试纸变蓝。
(1)无色液体A是_____,A与B反应的化学方程式是____________。
(2)由X转化为N2的化学方程式为______________。
(3)白色固体C的化学式为 _____。
由D转化为E的离子方程式为___。
【答案】浓氨水NH3·H2O+CaO=Ca(OH)2+NH3↑2NH3+3CuO
3Cu+N2+3H2OCa(OH)2CaCO3+CO2+H2O=Ca2++2HCO3-
【解析】
【分析】
X能使湿润的红色石蕊试纸变蓝,X为气体,则X为NH3,由C能与CO2生成白色沉淀D,CO2过量时又转化为无色溶液E,说明C可能是Ca(OH)2,D是CaCO3,E是Ca(HCO3)2。
常温下,产生氨气,以及根据X和C,推出A为氨水,B为生石灰,利用生石灰遇水放出热量,促使氨水分解,据此进行分析推断。
【详解】
(1)根据上述分析可知,A为氨水,氨水和氧化钙反应可以生成氨气,发生的反应是NH3·H2O+CaO=Ca(OH)2+NH3↑;
(2)利用氨气的还原性,发生的反应方程式为:
2NH3+3CuO
3Cu+N2+3H2O;
(3)根据上述分析可知,白色沉淀是Ca(OH)2,D转化成E的离子反应方程式为CaCO3+CO2+H2O=Ca2++2HCO3-;
【点睛】
本题的突破口是X,X为气体,能使湿润的红色石蕊试纸变蓝,说明是X是氨气,因为氨气是中学阶段,学过的唯一一种能使湿润的红色石蕊试纸变蓝的气体,然后根据常温下,制备氨气,利用反应物的状态,推测A为氨水,B为生石灰,进一步进行推测。
10.下列框图涉及到的物质所含元素中,除一种元素外,其余均为1~18号元素。
已知:
A、F为无色气体单质,B为具有刺激性气味的气体,C为黑色氧化物,E为红色金属单质(部分反应的产物未列出)。
请回答下列问题:
(1)D的化学式为__;F的结构式为__。
(2)A与B生成D的反应在工业上是生产__的反应原理之一。
(3)E与G的稀溶液反应的离子方程式为__。
(4)B和C反应的化学方程式为__。
(5)J、K是同种金属的不同氯化物,K为白色沉淀。
写出SO2还原J生成K的离子方程式:
__。
【答案】NON≡N硝酸3Cu+8H++2NO3−=3Cu2++2NO↑+4H2O3CuO+2NH3
3Cu+N2+3H2O2Cu2++2Cl-+SO2+2H2O=2CuCl↓+4H++SO42−
【解析】
【分析】
E为红色金属单质,应为Cu,则C为CuO,B为具有刺激性气味的气体,应为NH3,可与CuO在加热条件下发生氧化还原反应生成单质Cu,生成的气体单质F为N2,可与氧气在放电条件下反应生成N
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 备战 高考 化学 及其 化合物 有关 压轴
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 1212中级汽车维修工考试试题三.docx
1212中级汽车维修工考试试题三.docx
