 一般医疗器械企业审核重点关注项.docx
一般医疗器械企业审核重点关注项.docx
- 文档编号:10674916
- 上传时间:2023-02-22
- 格式:DOCX
- 页数:7
- 大小:17.96KB
一般医疗器械企业审核重点关注项.docx
《一般医疗器械企业审核重点关注项.docx》由会员分享,可在线阅读,更多相关《一般医疗器械企业审核重点关注项.docx(7页珍藏版)》请在冰豆网上搜索。
一般医疗器械企业审核重点关注项
一般医疗器械企业审核重点关注项
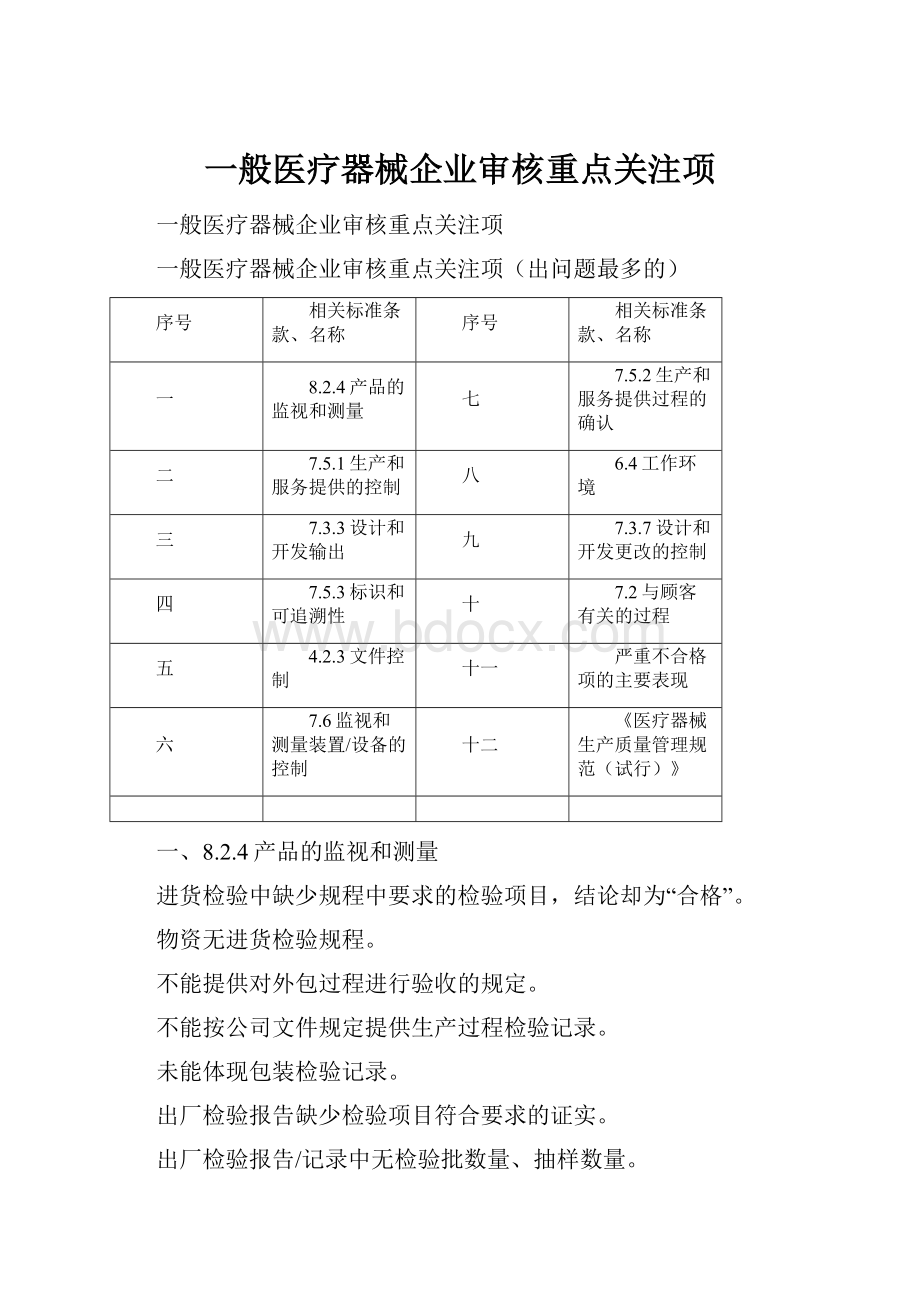
一般医疗器械企业审核重点关注项(出问题最多的)
序号
相关标准条款、名称
序号
相关标准条款、名称
一
8.2.4产品的监视和测量
七
7.5.2生产和服务提供过程的确认
二
7.5.1生产和服务提供的控制
八
6.4工作环境
三
7.3.3设计和开发输出
九
7.3.7设计和开发更改的控制
四
7.5.3标识和可追溯性
十
7.2与顾客有关的过程
五
4.2.3文件控制
十一
严重不合格项的主要表现
六
7.6监视和测量装置/设备的控制
十二
《医疗器械生产质量管理规范(试行)》
一、8.2.4产品的监视和测量
进货检验中缺少规程中要求的检验项目,结论却为“合格”。
物资无进货检验规程。
不能提供对外包过程进行验收的规定。
不能按公司文件规定提供生产过程检验记录。
未能体现包装检验记录。
出厂检验报告缺少检验项目符合要求的证实。
出厂检验报告/记录中无检验批数量、抽样数量。
二、7.5.1生产和服务提供的控制
没有建立生产过程记录。
没有建立产品高温老化记录。
注塑工艺文件给出的工艺参数不完整,缺少各段温度参数要求。
未提供过程参数的记录。
未能提供首件检验和生产记录。
生产现场未能提供工艺文件。
三、7.3.3设计和开发输出
设计开发输出采购物资分类不明确。
无外包技术要求或外包接收准则。
缺少产品铭牌图。
外包装缺少产品编号、注册号、产品标准号。
未提供电路图、电原理图、绝缘图、包装图。
设计输入的资料中缺少风险管理的报告。
未能提供输入资料的评审记录。
未能提供设计更改由此可能导致风险的评价以及设计更改批准的证实。
设计输出机械部件图纸无材料标注。
设计输出机械部件图纸无自由公差及表面处理技术要求。
设计输出图纸无规格型号、尺寸及相关技术要求。
无仪器外壳图纸。
无外包装标志图纸。
四、7.5.3标识和可追溯性
外包装箱标识缺少产品标准号、易碎、堆码层数极限等内容。
来料批号和实际批号不一致。
出厂包装箱未标识产品注册证号和产品标准号。
自制软件无版号标识。
说明书中执行标准和产品注册号与产品铭牌印刷的不一致。
五、4.2.3文件控制
外来文件收集不全。
例如:
受控文件清单中缺少局令10号《医疗器械说明书、标签和包装标识管理规定》、12号《医疗器械生产监督管理办法》、15号《医疗器械经营企业许可证管理办法》、以及《医疗器械生产质量管理规范(试行)》、《不良事件监测和再评价管理办法》、YY/T0316-2008、GB/T191—2008等。
受控文件清单中相关作废版本标准未能及时更新。
质量手册、程序文件无发放记录。
未对删减条款和YY/T0287-2003中不适用条款进行说明。
未明确与产品有关的作废文件的保存期和质量记录的保存期。
未明确外来文件的控制分发。
文件未按照新版标准进行修改。
例如设计开发的更改描述不符合GB/T19001-2008要求。
记录控制程序文件和公司记录清单中均未明确各类记录具体的保持期限。
六、7.6监视和测量装置/设备的控制
未能提供设备的自校规程。
未能提供校准或检定的证实。
对自校方法,校验基准,量值的允许误差等均未作出规定。
使用现场已经通过检定的监视和测量设备,不能满足出厂检测要求。
监视和测量设备未纳入台帐管理,
七、7.5.2生产和服务提供过程的确认
确认的工艺参数与相应的作业指导书不一致。
未能提供吹塑、挤塑、注塑、小包装封口过程确认的证实。
电镀/电解未对电解时间、电流、电压等参数做出规定结论。
未包括对不同规格的焊接件进行工艺参数确认。
八、6.4工作环境
现行体系文件中,缺少对返回产品防止污染其他产品、工作环境或人员要求。
(补充:
对照产品标准中使用时的环境温、湿度等要求,控制生产现场环境。
)
九、7.3.7设计和开发更改的控制
提供的评审记录缺少对已交付产品影响的评审。
《设计开发控制程序》中未明确对设计更改进行适当的评审、验证和确认的要求。
所提供的设计开发进度表中未对设计更改的验证和确认做出安排。
未能提供进行评审的证实。
未能针对库存产品及售出产品做出处理的决定。
未提供对其更改的评审、验证和确认记录。
涉及到软件的更改,未提供软件更改后测试合格的证据。
未能提供相关设计更改控制记录证实。
未能提供对该软件的测试记录,也未对可能引入的产品风险进行识别。
未能提供修改后的产品图,未提供设计更改评审、验证及通知单等必要的记录。
未能提供设计更改由此可能导致风险的评价以及设计更改批准的证实。
自行更改了产品使用说明书内容,未能提供该设计更改的相应记录。
未能提供对更改进行评审、验证、和确认的证实。
十、7.2与顾客有关的过程
在公司手册中,没有规定签订合同之前、参加投标之前、电话或传真订货确定之前等情况下的评审方式。
未能提供对抱怨与顾客进行有效沟通或已有效安排的证实。
未提供标书评审流程等相关要求文件和对标书进行评审的证实。
产品销售合同在前,评审记录在后。
没有提供合同评审的证实。
审核中未能提供经销商档案和资质。
代理商经营许可证,其经营范围缺少本公司产品类别。
合同中未明确代理商保持销售记录以便于追溯的要求。
未明确不良事件上报、信息反馈等要求。
产品宣传样本中适用范围的描写有超出该产品注册证范围的内容。
十一、严重不合格项的主要表现
7.5.1/8.2.4未能提供对应的生产批记录和出厂检验报告。
8.2.4未按产品注册标准要求提供检验证实。
8.2.4未提供连续漏电流单一故障状态检测和患者漏电流直流分量的检测证实。
8.2.4未提供电介质强度进行了网电源与已保护接地外壳之间1500V、与应用部分之间4000V电压的检测证实。
7.5.1/7.5.2提供不出关键、特殊工序的控制要求,也提供不出以上工序的生产记录。
8.2.4未能提供产品出厂检验的证实。
7.6设备不能完成规定的项目检验。
8.2.4成品检验记录,与检验规程要求不一致。
7.5.3产品标识不符合相关要求。
7.5.2未能提供特殊过程焊接的确认报告。
8.3没有提供对不合格品进行评审和重新检验的证实。
8.2.4缺少尺寸、电气测试等项目的检测记录证实。
8.5.2不合格项重复发生。
十二、2011年1月1日开始施行的《医疗器械生产质量管理规范(试行)》
(再次关注点)
第五条 生产企业负责人应当具有并履行以下职责:
……
(三)确保质量管理体系有效运行所需的人力资源、基础设施和工作环境;……
(五)指定专人和部门负责相关法律法规的收集,确保相应法律法规在生产企业内部贯彻执行。
第七条 生产、技术和质量管理部门的负责人应当熟悉医疗器械相关法规,具有质量管理的实践经验,有能力对生产和质量管理中的实际问题作出正确的判断和处理。
第八条 从事影响产品质量工作的人员,应当经过相应的技术培训,具有相关理论知识和实际操作技能。
第二十五条 ……当采购产品有法律、行政法规和国家强制性标准要求时,采购产品的要求不得低于法律、行政法规的规定和国家强制性标准的要求。
第三十条 生产企业应当编制生产工艺规程、作业指导书等,并明确关键工序和特殊过程。
第三十二条 在生产过程中必须进行清洁处理或者从产品上去除处理物时,生产企业应当将对产品进行清洁的要求形成文件并加以实施。
……
第三十三条 ……生产企业应当鉴定过程确认人员的资格。
第三十四条 生产企业应当建立和保持每批产品的生产记录。
生产记录应当满足医疗器械可追溯性要求,并标明生产数量和入库数量。
第四十条 ……对有存放期限或特殊贮存条件要求的医疗器械和材料应当按照规定条件贮存,并保存相关记录。
第四十一条 ……
(二)应当规定在搬运、维护、贮存期间对监视和测量装置的防护要求,防止检验结果失准;……
第四十九条 生产企业选择医疗器械经营企业,应当符合医疗器械相关法规要求。
第五十九条 生产企业应当建立数据分析程序并形成文件,规定收集与产品质量、不良事件和质量管理体系运行有关的数据,包括反馈、产品质量、市场信息及供方情况。
(END)
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 一般 医疗器械 企业 审核 重点 关注
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 1212中级汽车维修工考试试题三.docx
1212中级汽车维修工考试试题三.docx
 记叙文表现手法.pptx
记叙文表现手法.pptx
