 物质构成的奥秘.docx
物质构成的奥秘.docx
- 文档编号:10478124
- 上传时间:2023-02-13
- 格式:DOCX
- 页数:25
- 大小:1.78MB
物质构成的奥秘.docx
《物质构成的奥秘.docx》由会员分享,可在线阅读,更多相关《物质构成的奥秘.docx(25页珍藏版)》请在冰豆网上搜索。
物质构成的奥秘
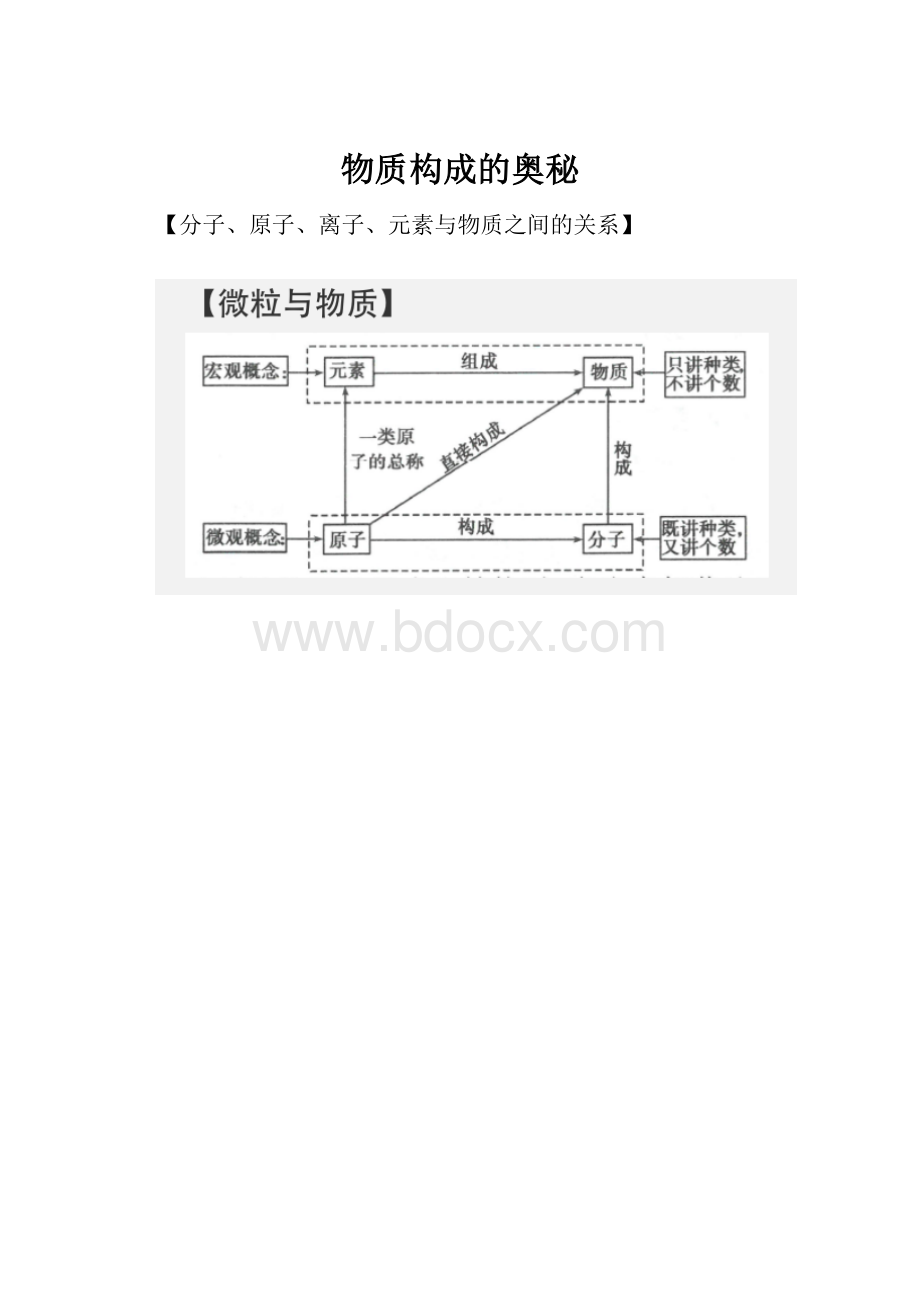
【分子、原子、离子、元素与物质之间的关系】
【例1】以下对
四种物质组成的说法中,正确的是( )
A.都含有氧分子 B.都含有2个氧原子
C.都含有氧元素 D.都是氧化物
【解析】A、氧气是由氧分子构成的,、、分别是由二氧化碳分子、二氧化硫分子、二氧化锰分子构成的,故选项说法错误。
B、由、、、四种物质的化学式可知,它们的一个分子中均含有2个氧原子,而不是四种物质中都含有2个氧原子,故选项说法错误。
C、由、、、四种物质的化学式可知,四种物质中均含有氧元素,故选项说法正确。
D、是由一种元素组成的纯净物,属于单质,故选项错误。
故选:
C。
【例2】回答下列问题:
(1)二氧化碳是由___________(填“原子”、“分子”或“离子”,)构成的。
(2)某粒子的结构示意图为
,当a=8时,该粒子是___________(填“原子”、“阳离子”或“阴离子”)。
【解析】
(1)二氧化碳是由二氧化碳分子构成的。
故填:
分子;
(2)在原子中,核内质子数=核外电子数,当a=8时,该粒子核内质子数<核外电子数,所以属于阴离子,故填:
阴离子。
该考点的命题方向主要是通过创设相关问题情景或图表信息等,来考查学生对分子、原子、离子、元素与物质之间的关系的理解和掌握情况;以及阅读、分析、推断 能力和对知识的迁移能力。
并且经常将其与物质的组成和构成、化合物的分类和类别辨析、化学反应的实质、元素在概念和分类、分子(或原子、离子)的概念等 相关知识联系起来,进行综合考查。
题型有选择题、填空题。
中考的重点是考查学生阅读、分析问题情景或图表信息的能力,对分子、原 子、离子、元素与物质之间的关系等相关知识的理解和掌握情况,以及运用它们来分析、解答相关的实际问题的能力等。
有时还会根据所给的有关的表达,进行科学地评价、判断正误等。
由于这部分内容是揭开物质组成和构成的神秘面纱的抽象而重要的知识,既可以考查学生对宏观概念和微观粒子的理解及表达能力,又可以考查学生的思考分析能力和抽象思维能力等,所以,该考点倍受命题人的青睐,而且是近几年中考命题的热点和重点。
要想解答好这类题目,首先要理解和熟记分子、原子、离子、元素与物质之间的关系,以及与之相关的知识。
然后根据所给的问题情景或图表信息等,结合所学的相关知识和技能,以及自己的生产或生活经验所得,细致地分析题意(或图表信息)等各种信息资源,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可。
还要注意以下几点:
1.不要将分子、原子和离子与物质之间的构成关系和元素与物质之间的组成关系隔离开来,其实它们(即物质的构成和组 成)之间也是相互联系的。
(1)由非金属元素组成的气态非金属单质和非金属元素与非金属元素组成的化合物,一般是由分子构成的;如氧气和二氧化碳等。
(2)由非金属元素组成的固态非金属单质,由金属元素组成的金属单质和由稀有气体元素组成的稀有气体单质,一般是由原子构成的;如硫、铝和氦气等。
(3) 由金属元素与非金属元素组成的化合物,一般是由离子构成的(金属元素的原子容易失去电子,变成阳离子;非金属元素的原子容易获得电子,变成阴离子);如氯化钠、氯化钙等。
2.根据物质的构成关系(或组成关系),可以推得它的组成关系(或构成关系)。
即知道物质的构成粒子可以推得其组成元素;反过来,知道物质的组成元素也可以推得其构成粒子。
【分子和原子的区别和联系】
【基本概念】
【例1】物质是由微观粒子构成的,用分子、原子等相关知识回答下列问题
(1)分子和原子的主要区别是:
在化学反应中_________发生变化,________不发生变化,只能重新组合成新的____________。
(2)从微观上解释混合物和纯净物。
对于由分子构成的物质,混合物是由__________(填“同种分子”或“不同种分子”下同)构成的,纯净物是由________构成的。
【解析】
(1)在化学变化中,分子可以再分,原子不可以再分,原子重新组合成新物质的分子,故填:
分子,原子,分子;
(2)混合物中含有多种分子,纯净物质含有的是同种物质的分子,故填:
不同种分子,同种分子。
【例2】下列有关分子和原子的说法中,正确的是( )
A.分子可以再分,原子不能再分
B.分子可直接构成物质,而原子要先构成分子后才能构成物质
C.分子能保持物质的化学性质,原子不能保持物质的化学性质
D.分子在化学变化中可分解产生原子,这些原子又重新组合构成别的分子
【解析】A、分子可以再分,原子也可以再分,但在化学变化中原子是最小微粒,故A错误;
B、分子可直接构成物质,原子也可以直接构成物质,如金属单质是由金属原子直接构成的,故B错误;
C、分子、原子都可以保持物质的化学性质,关键取决于该物质的构成微粒,故C错误;
D、化学变化的实质是分子分解为原子,原子重新结合生成新的分子,故D正确;
故选D。
该考点的命题方向主要是通过创设相关问题情景或图表信息等,来考查学生对分子和原子的区别和联系的理解和掌握情况;以及阅读、分析、推断能力和对知识的迁移能力。
并且经常将其与物质的组成和构成、物质的分类和类别辨析、化学反应的实质、微观观点及模型图的应用等相关知识联系起来,进行综合考查。
题型有选择题、填空题。
中考的重点是考查学生阅读、分析问题情景或图表信息的能力,对分子和原子的区别和联系等相关知识的理解和掌握情况,以及运用它们来分析、解答相关的实际问题的能力等。
有时还会根据所给的有关的表达,进行科学地评价、判断正误等。
特别是对分子和原子的概念、性质及其本质区别等相关问题的考查,以及对有关知识的迁移能力的考查,是近几年中考命题的热点,并且还是中考考查这块知识的重中之重。
要想解答好这类题目,首先,要理解和熟记分子和原子的区别和联系,以及与之相关的知识。
然后,根据所给的问题情景或图表信息等,结合所学的相关知识和技能,以及自己的生产或生活经验所得,细致地分析题意(或图表信息)等各种信息资源,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.同时,还要注意以下几点:
1.我们不能简单地说“分子大(或重),原子小(或轻)”。
当然,分子确实比构成的它的任何一个原子都要大(或重)。
例如,水分子比构成它的氢原子或氧原子都要大(或重),但水分子与其它原子相比就不一定了。
2.我们也不能笼统地说“分子能直接构成物质,原子不能”。
当然,构成分子的哪些原子确实不能直接构成该分子构成的物质,但是它们也可能直接构成其它的物质。
例如,水是水分子构成的,而构成水分子的氢原子和氧原子是不能直接水的;但是,氢原子可以直接构成氢气,氧原子也可以直接构成氧气(或臭氧)。
3.这种说法:
“分子能保持物质的化学性质,原子不能”也是错误的。
当然由分子构成的物质的化学性质确实是该分子保持的,而构成该分子的原子是不能保持该物质的化学性质的。
但是,由原子直接构成的物质中是没有分子存在的,此时该物质的化学性质就是由构成它的原子所保持的。
例如,水的化学性质就是由构成它的水分子保持的,构成水分子的氢原子和氧原子是不能保持水的化学性质的;而对金属(如铁、铜等)、固态非金属(如碳、硫)、稀有气体(如氦气、氖气等)这三类物质来说,它们都是由原子直接构成的物质,其中是不含分子的,所以它们的化学性质也就不是由分子保持的了,而是由构成它的原子保持的。
4.分子和原子的最本质的区别是在化学反应中,分子能够分解,而原子不能够再分。
【利用分子与原子的性质分析和解决问题】
【基本概念】
1.分子和原子都在不断运动;
2.分子和原子之间都有间隔;
3.分子和原子质量校、体积小;
4.同种分子和原子性质相同,不同种分子和原子性质不相同;
5.分子是保持物质化学性质的最小微粒,原子是化学变化中最小的微粒,也就是说,分子在化学变化中可以再分,而原子在化学变化中不可再分。
【例1】下列相关说法用粒子的知识解释错误的是( )
相关说法解释
A品红在水中扩散分子不断运动
B酒精和水混合后体积小于二者之和分子之间有间隔
C盐酸、硫酸溶液显酸性溶液中都含有酸根离子
D一氧化碳和二氧化碳化学性质不同分子构成不同
【解析】A、品红在水中扩散,是因为品红中含有的分子是在不断运动的,向水中扩散,故选项解释正确。
B、酒精和水混合后体积小于二者之和,是因为分子之间有间隔,一部分水分子和酒精分子会互相占据分子之间的间隔,故选项解释正确。
C、盐酸、硫酸溶液显酸性是因为酸中都含有氢离子,故选项解释错误。
D、一氧化碳和二氧化碳化学性质不同是因为一氧化碳和二氧化碳分子的构成不同,故选项解释正确。
故选C。
【例2】化学与我们的生活有着密切的联系,请用化学知识对下列现象进行解释.
(1)水银温度计受热液柱升高的原因是_______________________;
(2)硫酸铜溶液为蓝色,硫酸亚铁溶液为浅绿色的原因_______________________;
(3)木炭燃烧能生成二氧化碳或一氧化碳说明______________________________。
【解析】
(1)水银是金属汞的俗称,水银温度计受热液柱升高,是因为温度升高,汞原子间的间隔变大。
(2)硫酸铜溶液为蓝色,硫酸亚铁溶液为浅绿色,是因为硫酸铜、硫酸亚铁溶液中的阳离子分别是铜离子、亚铁离子,即阳离子的种类不同。
(3)木炭燃烧能生成二氧化碳或一氧化碳,即碳在氧气中充分燃烧生成二氧化碳,不充分燃烧生成一氧化碳,说明反应物的质量不同,生成物可能不同。
故答案为:
(1)温度升高,汞原子间的间隔变大;
(2)阳离子的种类不同; (3)反应物的质量不同,生成物可能不同。
命题方向:
该考点的命题方向主要是通过创设相关问题情景或图表信息等,来考查学生对利用分子与原子的性质分析和解决问题的理解和掌握情况;以及阅读、分析、推断能力和对知识的迁移能力。
并且经常将其与物质的组成和构成、物质的分类和类别辨析、物质的性质和变化、分子与原子的概念和本质区别、溶解现象与溶解的原理等相关知识联系起来,进行综合考查。
题型有选择题、填空题。
中考的重点是考查学生阅读、分析问题情景或图表信息的能力,利用分子与原子的性质分析和解决问题的能力等。
有时还会根据所给的有关的表达,进行科学地评价、判断正误等。
特别是对分子与原子的彼此之间有间隔,总是在不停的运动;同种分子(或原子)性质相同,不同种分子(或原子)性质不同;以及它们的概念和本质区别等相关问题的考查。
解题方法点拨:
要想解答好这类题目,首先要理解和熟记利用分子与原子的性质分析和解决问题的方法和技巧,以及分子与原子的概念和本质区别等相关的知识。
然后根据所给的问题情景或图表信息等,结合所学的相关知识和技能,以及自己的生产或生活经验所得,细致地分析题意(或图表信息)等各种信息资源,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可。
同时要注意以下几点:
1.分子与原子的性质可以简记为“两小运间,同同不不”八个字。
在利用它们来分析和解决问题时,要先看看与哪种粒子(即分子还是原子)有关,然后再联系着该粒子的有关性质进行分析解答之。
2. 在解释有关物质的性质或变化等问题时,一定要联系着分子与原子的概念和本质区别来进行思考、分析。
但是,不能认为“分子能保持物质的化学性质,原子不能”。
当然由分子构成的物质的化学性质确实是该分子保持的,而构成该分子的原子是不能保持该物质的化学性质的。
可是,由原子直接构成的物质中是没有分子存在的,此时该物质的化学性质就是由构成它的原子所保持的。
例如,水的化学性质就是由构成它的水分子保持的,构成水分子的氢原子和氧原子是不能保持水的化学性质的;而对金属(如铁、铜等)、固态非金属(如碳、硫)、稀有气体(如氦气、氖气等)这三类物质来说,它们都是由原子直接构成的物质,其中是不含分子的,所以它们的化学性质也就不是由分子保持的了,而是由构成它的原子保持的。
【原子的定义与构成】
【基本概念】
原子的定义是化学变化中的最小粒子。
原子的构成:
原子是由居于原子中心带正电的原子核和核外带负电的电子构成,原子核是由质子和中子两种粒子构成的,电子在核外的较大空间做高速运动。
原子内的微粒与原子的关系:
(1)原子一般是由质子、中子、核外电子三种粒子构成的,但不是绝对的,一个氢原子中只有一个质子和一个核外电子,没有中子;
(2)在原子中,质子所带的正电荷总数等于核外电子所带的负电荷总数,中子不带电,所以整个原子不显电性;
(3)在原子中,质子数=核外电子数=核电荷数,核电荷数是原子核所带的正电荷数。
(4)质子数不一定等于中子数。
【例1】下列叙述正确的是①原子由质子和中子构成 ②原子不显电性 ③原子不能再分 ④原子的质子数决定元素种类 ⑤原子可以构成分子,也可直接构成物质( )
A.①②④ B.②④⑤ C.③④ D.①②③⑤
【解析】①原子核由质子和中子构成,错误;
②原子不显电性,正确;
③原子能再分为原子核和核外电子,错误;
④原子的质子数决定元素种类,正确;
⑤原子可以构成分子,也可直接构成物质,正确;
故选B。
【例2】考古学上通过碳-14原子测定文物年代。
碳-14和碳-12原子在原子结构上的不同之处是_____________,它们的原子质量比是___________。
【解析】碳-12原子的核内有6个质子和6个中子,碳-14原子的核内有6个质子和8个中子,两种原子中中子数不同;根据相对原子质量=质子数+中子数,可知碳14原子的质量与碳12原子的质量之比为14:
12=7:
6。
故答案为:
中子数不同;7:
6。
命题方向:
该考点的命题方向主要是通过创设相关问题情景或图表信息等,来考查学生对原子的定义与构成的理解和掌握情况;以及阅读、分析、推断能力和对知识的迁移能力。
并且经常将其与物质的构成、分子和原子的本质区别、相对原子质量及其计算、元素的定义和种类、原子结构示意图等相关知识联系起来,进行综合考查。
题型有选择题、填空题。
中考的重点是考查学生阅读、分析问题情景或图表信息的能力,对原子的定义与构成等相关知识的理解和掌握情况,以及运用它们来分析、解答相关的实际问题的能力等。
当然,有时还会根据所给的有关的表达,进行科学地评价、判断正误等。
特别是,对原子的可分性、电中性、有关的等量关系等相关问题的考查,以及对有关知识的迁移能力的考查,是近几年中考命题的热点,并且还是中考考查这块知识的重中之重。
解答技巧:
要想解答好这类题目,首先要理解和熟记原子的定义与构成,以及与之相关的知识。
然后,根据所给的问题情景或图表信息等,结合所学的相关知识和技能,以及自己的生产或生活经验所得,细致地分析题意(或图表信息)等各种信息资源,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可。
同时要注意以下几点:
1.原子定义为是化学变化中的最小粒子,只是说在化学变化中它是最小的粒子,不代表它本身不能再分;其实原子确实是可以再分为原子核和核外电子的。
2.在原子中,核电荷数等于核内质子数等于核外电子数;可是当它不是原子(即有得失电子而变成了阴、阳离子)时,核电荷数等于核内质子数,但是不再等于核外电子数(在阳离子中,核电荷数等于核内质子数大于核外电子数;在阴离子中,核电荷数等于核内质子数小于核外电子数)。
【元素的概念】
【基本概念】
元素的概念是具有相同核电荷数(即核内质子数)的一类原子的总称。
例如,氧气分子和水分子中都含有氧原子,它们的核电荷数都是8,即核内都含有8个质子,就把它们统称为氧元素。
同样,把核电荷数为1的所有的氢原子统称为氢元素,把核电荷数为6的所有的碳原子统称为碳元素,等等。
【例1】碳元素与氧元素的本质区别是( )
A.质子数不同 B.电子数不同
C.中子数不同 D.最外层电子数不同
【解析】根据不同种元素之间的本质区别是质子数不同,因此碳元素与氧元素的本质区别是质子数不同。
故选:
A。
【例2】决定元素种类的是____________(即___________),不同种元素的本质区别是___________。
决定元素化学性质的是____________。
在化学变化中,铝原子易___________,变成带有__________个单位______________电荷的离子,符号是_______;氯原子易____________,变成带有__________个单位___________电荷的离子,符号是_________;二者形成化合物的化学式为__________。
【解析】元素是质子数相同的同一类原子的总称,决定元素种类的是质子数,即核电荷数,不同种元素的本质区别是质子数不同;决定元素化学性质的是原子的最外层电子数;在化学变化中,铝原子易失电子,变成带有3个单位正电荷的离子,符号可书写为:
;氯原子易得电子,变成带有1个单位负电荷的离子,符号是:
;二者形成化合物的化学式为:
;
故答案为:
质子数;核电荷数;质子数不同;原子的最外层电子数;失电子;3;正;;得;1;负;;。
命题方向:
该考点的命题方向主要是通过创设相关问题情景或图表信息等,来考查学生对元素的概念的理解和掌握情况;以及阅读、分析、推断能力和对知识的迁移能力。
并且经常将其与物质的组成和构成、物质的分类和类别辨析、原子的构成及其结构示意图或离子结构示意图、质量守恒定律及其应用、化学式的书写及意义等相关知识联系起来,进行综合考查。
题型有选择题、填空题。
中考的重点是考查学生阅读、分析问题情景或图表信息的能力,对元素的概念等相关知识的理解和掌握情况,以及运用它们来分析、解答相关的实际问题的能力等。
有时还会根据所给的有关的表达,进行科学地评价、判断正误等。
特别是对元素种类的判断、元素与原子的关系、物质的元素组成等相关问题的考查,以及对有关知识的迁移能力的考查,是近几年中考命题的热点。
解题技巧:
要想解答好这类题目,首先要理解和熟记元素的概念,以及与之相关的知识。
然后根据所给的问题情景或图表信息等,结合所学的相关知识和技能,以及自己的生产或生活经验所得,细致地分析题意(或图表信息)等各种信息资源,并细心地探究、推理后,按照题目要求进行认真地选择或解答。
同时要注意以下几点:
1.解答有关元素概念的问题时,要抓住这样几个关键词。
(1)相同核电荷数(即核内质子数);
(2)一类(即无数个,所以元素只能讲种类,不能讲个数);
(3)原子(即元素的概念是建立在原子的基础上的);
(4)总称(即元素是同类原子的集合体)。
2.当原子通过得失核外电子,而变成阴、阳离子时,核内的质子数是没有改变的,因此,该离子与其原来的原子都属于同一种元素。
也可以说,元素概念中的原子其实也是包括离子的,实际上离子只是带电的特殊的原子罢了;不过,这里只是指一部分离子而已,不包括哪些形式为“带电的原子团”的离子(因为原子团相对来说比较复杂,实际上其中含有多种元素的原子)。
【地壳中元素的分布与含量】
【基本概念】
地壳中元素的分布与含量,如图所示:
对于它们含量高低顺序来说,识记起来比较麻烦;不过,采用谐音编成这样的小故事:
“养(氧)闺(硅)女(铝),贴(铁)给(钙)那(钠)家(钾)美(镁)青(氢)(年)”,来导记地壳中元素的含量高低顺序,将会是事半功倍。
并且,这个顺序是比较重要,也比较关键的;特别是,其中的氧、硅、铝、铁、钙一定要熟练地记住它们。
【例1】地壳中含量最高的元素是______;人体中含量最高的金属元素是______;常用作软包装食品“保护气”的单质是__________。
【解析】地壳中含量最高的元素是;人体中含量最高的金属元素是;的性质稳定,常用作软包装食品“保护气”的单质。
故答为:
O,Ca,N2。
【例2】地壳中含量最多的非金属元素是( )
A.铝 B.硅 C.氧 D.铁
【解析】地壳中含量最多的非金属元素是氧元素,观察选项,故选C。
命题方向:
该考点的命题方向主要是通过创设相关问题情景或图表信息等,来考查学生对地壳中元素的分布与含量的理解和掌握情况;以及阅读、分析、推断能力和对知识的迁移能力。
经常将其与有关化学之最、物质的组成和构成、物质和元素的分类和类别辨析、原子的构成及其结构示意图或离子结构示意图、常见元素或原子团的化合价、化学式的书写及意义等相关知识联系起来,进行综合考查。
题型有选择题、填空题。
中考的重点是考查学生阅读、分析问题情景或图表信息的能力,对地壳中元素的分布与含量及其高低顺序等相关知识的理解和掌握情况,以及运用它们来分析、解答相关的实际问题的能力等。
有时还会根据所给的有关的表达,进行科学地评价、判断正误等。
特别是对地壳中的元素含量居于前五位的元素及其顺序和种类判断、由这些元素组成的物质及其化学式的书写和意义等相关问题的考查,以及对有关知识的迁移能力的考查,是近几年中考命题的热点。
解题方法点拨:
要想解答好这类题目,首先要理解和熟记地壳中元素的分布与含量及其高低顺序,以及与之相关的知识。
然后根据所给的问题情景或图表信息等,结合所学的相关知识和技能,以及自己的生产或生活经验所得,细致地分析题意(或图表信息)等各种信息资源,并细心地探究、推理后,按照题目要求进行认真地选择或解答。
同时要注意以下几点:
1.地壳中的元素含量居于前五位的元素顺序可以简记为“洋(氧)鬼(硅)--吕(铝)铁钙”。
2.涉及到的有关化学之最有:
(1)地壳中含量最多的元素是氧元素;
(2)地壳中含量最多的金属元素是铝元素;
(3)地壳中含量最多的非金属元素是氧元素。
【元素的符号及其意义】
【元素符号】
元素的符号是指用来表示元素的特有符号。
它是化学学科所特有的一种用语,是化学科学研究物质组成、结构和变化规律的一种重要工具。
现在国际上,统一常用元素的拉丁文名称的第一个大写字母来表示,如果几种元素的第一个字母相同时,可再附加一个小写字母来区别.例如,用C表示碳元素,Ca表示钙元素,S表示硫元素,Si表示硅元素,N表示氮元素,Na表示钠元素,等等。
【元素符号意义】
(1)表示一种元素
(2)表示这种元素的一个原子.例如,H既表示氢元素,还表示一个氢原子;等等。
注意:
如果元素符号前面加数字,则只表示该原子的个数,只具有微观意义。
【例1】元素符号“N”可以表示( )
A.氮气的化学式 B.1个氮原子
C.1个氮元素 D.氮的相对原子质量
【解析】A、元素符号“N”不能表示氮气的化学式,氮气的化学式为,故选项错误。
B、元素符号可表示一种元素、一个原子,元素符号“N”可表示1个氮原子,故选项正确。
C、元素只讲种类、不讲个数,故选项错误。
D、元素符号可表示一种元素、一个原子,不能表示氮的相对原子质量,故选项错误。
故选:
B。
【例2】规范书写是我们学习中必须遵循的原则,小明在元素周期表中查找到如图所示的一格后,明白了不能把一氧化碳写成“Co”的原因。
(1)“Co”表示_________元素(填名称);
(2)“CO”是由___________两种元素(填名称)组成的_______(填“单质”或“化合物”)。
【解析】
(1)由图示可知“Co”表示 钴 元素;
(2)一氧化碳的化学式为CO,是由 碳和氧 两种元素组成,属于纯净物中的化合物。
故答案为:
(1)钴;
(2)碳和氧;化合物。
命题方向:
该考点的命题方向主要是通过创设相关问题情景或图表信息等,来考查学生对元素的符号及其书写和意义的理解和掌握情况;以及阅读、分析、推断能力和对知识的迁移能力。
并且经常将其与物质的组成和构成、物质和元素的分类和类别辨
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 物质 构成 奥秘
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《Java程序设计》考试大纲及样题试行.docx
《Java程序设计》考试大纲及样题试行.docx
