 届暑假人教版高三一轮复习化学《水溶液中的离子平衡》选择专题训练含答案.docx
届暑假人教版高三一轮复习化学《水溶液中的离子平衡》选择专题训练含答案.docx
- 文档编号:10422737
- 上传时间:2023-02-11
- 格式:DOCX
- 页数:12
- 大小:407.67KB
届暑假人教版高三一轮复习化学《水溶液中的离子平衡》选择专题训练含答案.docx
《届暑假人教版高三一轮复习化学《水溶液中的离子平衡》选择专题训练含答案.docx》由会员分享,可在线阅读,更多相关《届暑假人教版高三一轮复习化学《水溶液中的离子平衡》选择专题训练含答案.docx(12页珍藏版)》请在冰豆网上搜索。
届暑假人教版高三一轮复习化学《水溶液中的离子平衡》选择专题训练含答案
2020届暑假人教版高三一轮复习化学《水溶液中的离子平衡》选择专题训练
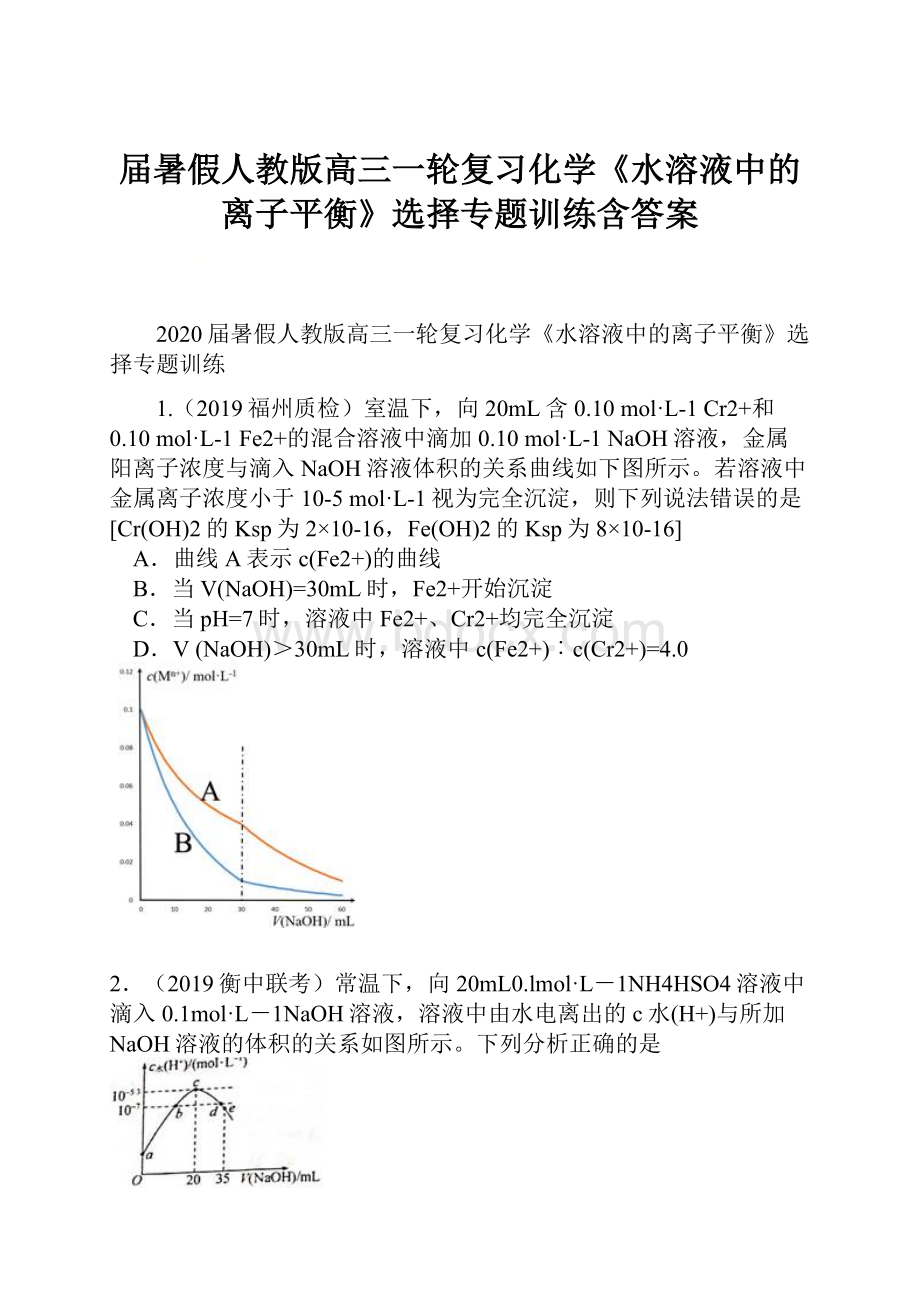
1.(2019福州质检)室温下,向20mL含0.10mol·L-1Cr2+和0.10mol·L-1Fe2+的混合溶液中滴加0.10mol·L-1NaOH溶液,金属阳离子浓度与滴入NaOH溶液体积的关系曲线如下图所示。
若溶液中金属离子浓度小于10-5mol·L-1视为完全沉淀,则下列说法错误的是
[Cr(OH)2的Ksp为2×10-16,Fe(OH)2的Ksp为8×10-16]
A.曲线A表示c(Fe2+)的曲线
B.当V(NaOH)=30mL时,Fe2+开始沉淀
C.当pH=7时,溶液中Fe2+、Cr2+均完全沉淀
D.V(NaOH)>30mL时,溶液中c(Fe2+)︰c(Cr2+)=4.0
2.(2019衡中联考)常温下,向20mL0.lmol·L-1NH4HSO4溶液中滴入0.1mol·L-1NaOH溶液,溶液中由水电离出的c水(H+)与所加NaOH溶液的体积的关系如图所示。
下列分析正确的是
A.b点时,溶液的pH=7
B.常温下,Kb(NH3·H2O)=1.0×10-5.3
C.Vd<30mI
D.e点溶液中粒子浓度由大到小的顺序为c(Na+)>c(SO42-)>c(NH4+)>c(NH3·H2O)>c(OH-)>c(H+)
3.(2019福建质检)常温下,用0.1mol·L-1MgSO4和0.05mol·L-1Al2(SO4)3溶液进行实验:
①各取25mL,分别滴加0.5mol·L-1NaOH溶液,测得溶液的pH与V(NaOH)的关系如图1所示;②将两种溶液等体积混合后,取出25mL,逐滴加入上述NaOH溶液,观察现象。
下列判断正确的是
A.图1中的曲线II表示MgSO4与NaOH反应的关系
B.根据图1可得Ksp[Al(OH)3]的值大于1.0×10-32
C.实验②中Al(OH)3完全溶解前,溶液中c(Mg2+)/c(Al3+)逐渐变大
D.图2可以表示实验②中n(沉淀)与V(NaOH)的关系
4.(2019广州)常温下,用0.10moI/LNaOH溶液滴定0.10mol/LHA溶液,滴定曲线如图a所示,混合溶液的pH与离子浓度变化的关系如图b所示。
下列叙述错误的是
A.Ka(HA)的数量级为10-5
B.N点,
C.P—Q过程中,水的电离程度逐渐增大
D.当滴定至溶液呈中性时,c(A-)>c(HA)
5.(2019潍坊一模)常温下,将NaOH溶液滴入二元弱酸H2X溶液中,混合溶液中的粒子浓度与溶液pH的变化关系如图所示。
下列叙述正确的是
A.曲线M表示lgc(X2-)/c(HX-)与pH的变化关系
B.NaHX溶液显碱性
C.当混合溶液呈中性时,c(Na+)>c(X2-)>c(HX-)>c(H+)=c(OH−)
D.Ka2(H2X)的数量级为10-9
6.(2019武汉二月)常温下.向10m0.1mol/LCuCl2溶液中滴加0.1mol/LNa2S溶液滴加过程中-lgc(Cu2+)与Na2S溶液体积(V)的关系如图所示。
下列说法错误的是
A.Ksp(CuS)的数量级为10-35
B.曲线上各点的溶液均满足关系式c(S2-)·e(Cu2+)=Ksp(CuS)
C.a、b、c三点中,由水电离的c(H+)和c(OH-)的积最小的为b点
D.c点溶液中:
c(Na+)>c(Cl-)>c(S2-)>c(OH-)>c(H+)
7.(2019北京海淀一模)HA为一元弱酸。
已知溶液中HA、A-的物质的量分数δ随溶液pH变化的曲线如右图所示。
向10mL0.1mol/LHA溶液中,滴加0.1mol/LNaOH溶液xmL。
下列说法中,不正确的是
A.pH=9时,c(A-)=c(HA) B.x=0时,1
C.x=5时,c(A-)=c(HA) D.x=10时,c(A-)+c(HA)=c(Na+)=0.05mol/L
8.(2019龙岩质检)已知:
pKa=-lgKa。
25℃时,H2A的pKal=1.85,pKa2=7.19。
常温下,用0.1mol·L-1NaOH溶液滴定20mL0.1mol·L-1H2A溶液的滴定曲线如图所示。
下列说法不正确的是
A.a点溶液中:
c(HA-)=c(H2A)
B.b点溶液中:
A2-水解平衡常数Khl=10-6.81
C.c点溶液中:
V0=30
D.a、b、c、d四点中,d点溶液中水的电离程度最大
9.(2019广州调研)一定温度下,三种碳酸盐MCO3(M:
Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示。
下列说法错误的是
A.Ksp(MnCO3)的数量级为10-11
B.MgCO3的悬浊液中加入少量水充分振荡,c(Mg2+)不变
C.a点表示的溶液中,c(Ca2+)>c(CO32-)
D.向浓度均为0.01mol·L-1的Mg2+、Ca2+、Mn2+混合溶液中逐滴加入Na2CO3溶液,最先形成MgCO3沉淀
10.(2019深圳一研)室温下,将尿酸钠(NaUr)悬浊液静置,取上层清液,再通入HCl,溶液中尿酸的浓度c(HUr)与pH的关系如右图所示。
已知:
Ksp(NaUr)=4.9×10-5,Ka(HUr)=2.0×10-6。
下列说法正确的是
A.上层清液中,c(Ur-)=7.0×10-2mol·L-1
B.在M→N的变化过程中,c(Na+)c(Ur-)将逐渐减小
C.当c(HUr)=c(Ur-)时,c(Cl-)>c(Ur-)
D.当pH=7时,2c(Na+)=c(Ur-)+c(Cl-)
11.(2019福建质检)常温下,用0.1mol·L-1NaOH溶液滴定新配制的25.0mL0.02mol·L-1FeSO4溶液,应用手持技术测定溶液的pH与时间(t)的关系,结果如图所示。
下列说法错误的是
A.ab段,溶液中发生的主要反应:
H++OH-=H2O
B.bc段,溶液中c(Fe2+)>(Fe3+)>c(H+)>c(OH-)
C.d点,溶液中的离子主要有Na+、SO42-、OH-
D.滴定过程发生了复分解反应和氧化还原反应
12.(2019郑州一测单科)25℃时,向一定浓度的Na2X溶液中滴入盐酸,溶液的pH与离子浓度变化关系如图所示。
已知:
H2X是二元弱酸,Y表示
或
,pY=-lgY。
下列叙述不正确的是
A.曲线n表示pH与p
的变化关系
B.Ka2(H2X)=1.0×10-10.3
C.NaHX溶液中c(H+)>c(OH-)
D.当溶液呈中性时,c(Na+)=c(HX-)+2c(X2-)+c(Cl-)
13.(2019西城上期末)为了研究Mg(OH)2溶于铵盐溶液的原因,进行如下实验:
①向2mL 0.2mol•L-1 MgCl2溶液中滴加1mol•L-1NaOH溶液至不再产生沉淀,将浊液分为2等份。
②向一份中逐滴加入4mol•L-1 NH4Cl溶液,另一份中逐滴加入4mol•L-1 CH3COONH4溶液(pH≈7),边滴加边测定其中沉淀的量,沉淀的量与铵盐溶液的体积的关系如图。
③将①中的NaOH溶液用氨水替换,重复上述实验。
下列说法不正确的是( )
A.Mg(OH)2浊液中存在:
Mg(OH)2 (s) ⇌Mg2+(aq)+2OH- (aq)
B.②中两组实验中均存在反应:
Mg(OH)2 +2NH4+=Mg2++2NH3•H2O
C.H+可能参与了NH4Cl溶液溶解Mg(OH)2的过程
D.③中获得的图象与②相同
14.(2019泉州3月质检)常温下,0.2mol•L-1Na2CrO4溶液中,H2CrO4、CrO42-、Cr2O72-和HCrO4-的分布曲线如图所示。
下列叙述错误的是
(已知:
2CrO42-+2H+
Cr2O72-+H2O)
A.曲线M表示pH与CrO42-的变化关系
B.Ka2(H2CrO4)的数量级为10-6
C.HCrO4-的电离程度大于水解程度
D.pH=2和pH=5时,2HCrO4-
Cr2O72-+H2O的平衡常数相等
15.(2019泉州二检)向0.1mol·L-1的NaClO溶液中滴加稀硫酸,HClO和ClO-所占分数(α)随pH变化的关系如右图所示。
下列表述不正确的是
A.曲线b代表ClO-
B.HClO的电离平衡常数Ka=10-7.47
C.pH=7时,c(Na+)>c(HClO)>c(ClO-)
D.向pH=6的该溶液中加入少量的Na2SO3固体,c(ClO-)增大
16.(2019郑州一模)常温下,将NaOH溶液滴加到某一元酸(HA)宿液中,测得混合溶液的pH与离子浓度变化关系如下图所示[已知:
]。
下列叙述不正确的是
A.Ka(HA)的数量级为10-5
B.滴加NaOH溶液过程中,
保持不变
C.m点所示溶液中:
c(H+)=c(HA)+c(OH-)-c(Na+)
D.n点所示溶液中:
c(Na+)=c(A-)+c(HA)
17.(2019莆田一检)乙二胺(H2NCH2CH2NH2),无色液体,有类似氨的性质。
已知:
25℃时,Kb1=10-4.07 Kb2=10-7.15;乙二氨溶液中各含氮微粒的分布分数δ(平衡时某含氮微粒的浓度占各含氮微粒浓度之和的分数)随溶液pH的变化曲线如右图。
下列说法错误的是
A.H2NCH2CH2NH2在水溶液中第一步电离的方程式为:
H2NCH2CH2NH2+H2O
H2NCH2CH2NH3++OH-
B.曲线Ⅰ代表的微粒符号为[H2NCH2CH2NH3]2+
C.曲线Ⅰ与曲线Ⅱ相交点对应pH=4.07
D.在0.1mol·L-1H2NCH2CH2NH3Cl溶液中各离子浓度大小关系为
c(Cl-)>(H2NCH2CH2NH3+) >c(OH-)>c(H+)
18.(2019泉州一检)常温下,向浓度均为0.1mol·L-1、体积均为10mL的两种一元酸(HX、HY)溶液中,分别滴入0.1mol·L-1NaOH溶液,pH的变化曲线如图所示。
下列说法错误的是
A.N点:
c(Na+)=c(Y-)+c(HY)
B.M点:
c(X-)>c(Na+)
C.滴至pH=7时,消耗NaOH溶液的体积:
HX>HY
D.滴入10mLNaOH溶液时,溶液中水的电离程度:
HX<HY
19.(衡中九模)T℃,分别向10ml浓度均为1mol/L的两种弱酸HA、HB中不断加水稀释,并用pH传感器测定溶液pH。
所得溶液pH的两倍(2pH) 与溶液浓度的对数(1gc) 的关系如图所示。
下列叙述正确的是
己知:
(1)HA的电离平衡常数Ka=[c(H+)·c(A-)]/[c(HA)-c(A-)]≈c2(H+)/c(HA);
(2) pKa=-lgKa
A.弱酸的Ka随溶液浓度的降低而增大
B.a 点对应的溶液中c(HA)=0.1mol/L,pH=4
C.酸性:
HA<HB
D.弱酸HB的 pKa=5
20.(2019河北衡中)25℃时,Ka(CH3COOH)=1.7×10-5。
该温度下,用0.1mol/L的醋酸滴定10.00 mL0.1mol/L的碱MOH,滴定过程中加入醋酸的体积(V)与溶液中lg[C(H+)/c(OH-)]的关系如图所示。
下列说法正确的是
A.MOH的电离方程式为MOH
M++OH-
B.a 点:
V(CH3COOH)= 10.00 Ml
C.b点:
c(CH3COO-)>c(H+ )>c(M+)>c(OH-)
D.25℃,时,CH3COO-的水解平衡常数为(10/17)×10-9
2020届暑假人教版高三一轮复习化学《水溶液中的离子平衡》选择专题训练答案
1.C
2.C
3.C
4.B
5.C
6.A
7.C
8.C
9.D
10.C
11.B
12.C
13.D
14.B
15.D
16.D
17.C
18.A
19.B
20.D
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 水溶液中的离子平衡 暑假 人教版高三 一轮 复习 化学 水溶液 中的 离子 平衡 选择 专题 训练 答案
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《Java程序设计》考试大纲及样题试行.docx
《Java程序设计》考试大纲及样题试行.docx
