 实验四 氨气的吸收与解吸实验.docx
实验四 氨气的吸收与解吸实验.docx
- 文档编号:10287607
- 上传时间:2023-02-09
- 格式:DOCX
- 页数:21
- 大小:103.95KB
实验四 氨气的吸收与解吸实验.docx
《实验四 氨气的吸收与解吸实验.docx》由会员分享,可在线阅读,更多相关《实验四 氨气的吸收与解吸实验.docx(21页珍藏版)》请在冰豆网上搜索。
实验四氨气的吸收与解吸实验
实验四氨气的吸收与解吸实验
一、实验目的
1.了解填料吸收装置的基本流程及设备结构;
2.了解气体流速与压强降的关系;
3.了解气体空塔气速和喷淋密度对总吸收系数的影响;
4.掌握吸收总系数K的测定方法;
5.掌握测定填料塔的流体力学性能的方法。
二、实验装置的特点
测量流体力学性能是吸收实验的一项重要内容
,填料塔流体力学特性包括压强降和液泛规律。
计算填料塔需用动力时,必须知道压强降的大小。
而确定吸收塔的气、液负载量时,则必须了解液泛的规律。
实验用空气与水进行,在各种喷淋量下,逐步增大气速,记录必要的数据直至刚出现液泛时止。
必须注意,不要使气速过分超过泛点,避免冲跑和冲破填料。
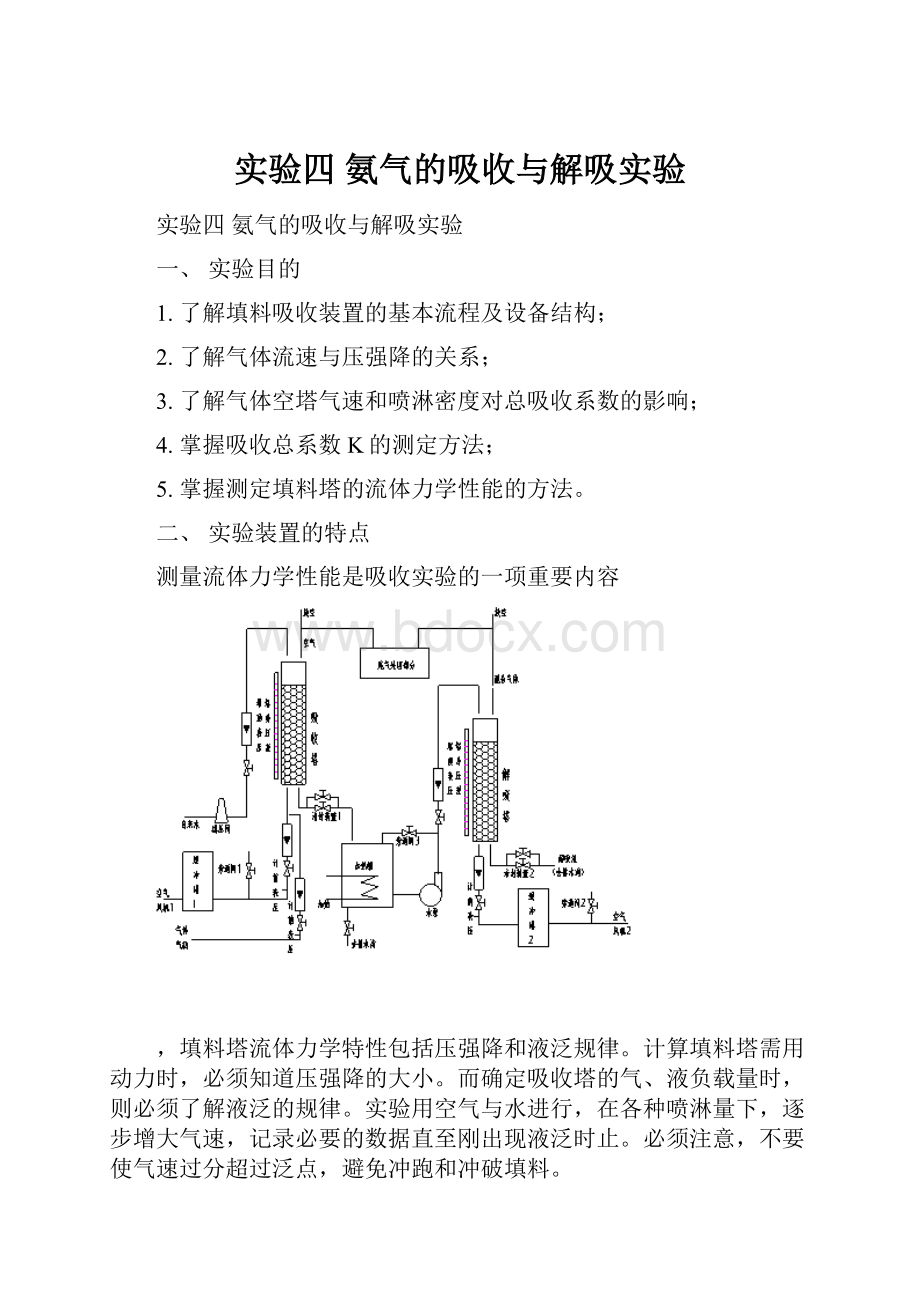
三、实验装置流程如图
图1XSGX—1吸收与解吸实验装置流程图
四、实验内容与步骤
(一)填料塔流体力学特性的测定
本项实验操作不要开动氨气系统,仅用水对空气进行操作。
1.先开动供水系统。
首先打开出水端阀门,再慢慢打开进水阀,开动供水系统中的滤水器。
注意:
如果在出水端阀门关闭情况下开进水阀,则滤水器可能超压。
2.开动空气系统。
开动时要首先全开叶氏风机的旁通阀,然后再启动叶氏风机,风机启动后再通过关小旁通阀的方法调节空气流量。
否则风机一开动,系统内气速突然上升可能碰坏空气转子流量计。
3.慢慢加大气速到接近液泛,使填料全面润湿一次,然后回复到预定气速再进行正式测定。
4.正式测定时,固定某一喷淋量,测定某一气速下填料的压降,按实验记录表格记录数据。
5.实验完毕,停机。
先全开旁通阀,待转子转速降下来以后再停机。
否则突然停机,气流突然停止,转子就会猛然摔下,打坏流量计。
(二)传质系数的测定
1.确定好操作条件(氨气流量、空气流量、喷淋量),准备好尾气分析器。
2.开动水系统和空气系统,一切准备就绪后开动氨气系统。
3.开动氨气系统。
弄清氨气自动减压阀的构造,开动时首先将自动减压阀的弹簧放松,使自动减压阀处于关闭状态,然后打开氨瓶瓶顶阀,此时自动减压阀的高压压力表应有示值。
接下来先关好氨气转子流量计前的调节阀,再缓缓压紧减压阀的弹簧,使阀门打开,同时注视低压氨气压力表,至压力表的示值达到5×104Pa或8×104Pa时即可停止。
4.然后用转子流量计前的调节阀调节氨气流量,按照设计的参数进行实验,做好数据记录工作。
5.实验完毕,随即关闭氨气系统,尽可能节约氨气,关闭氨气系统的步骤和开动步骤相反。
关闭空气系统,先全开旁通阀,待转子转速降下来以后再停机。
(三)尾气浓度的测定
尾气分析法
要应用在这里是有一定困难的。
所以我们仍沿用灵敏度高而准确的化学法。
我们还改革了一下,可免除滴定操作的麻烦,仪器可以直接读出结果,简单可行,我们曾用已知成份的样品气体进行核对,证实仪器是准确的。
(2)、仪器工作原理
请参看图10,预先往吸收管(8)装入稀硫酸作为吸收液,加入指示剂,(两滴甲基红)分析开始,打开考克(5),被测气体通过吸收管后其中的氨被吸收而空气则由湿式气体流量计计量所流过的总体积,当吸收液到达终点时
1—尾气管2—尾气调压阀3—取样管(管口对正气流方向)4—定压器
5—玻璃考克6—快装接头7—吸收盒8—吸收管9—湿式气体流计
图2分析仪流程图
(由红变黄)立即关闭考克5,因为吸收液是已知量,被吸收的氨量也就固定,所以湿式气体流量计所计量的空气总体积就直接反映出被测气的浓度(见例题2)
吸收管装在透明的吸收盒内,每分析一个气样换一个盒子。
如果加入吸收液后液面未到达刻线,应加蒸馏水补足,使吸收液能正常循环,测量时注意控制考克5的开度,太大气流夹带吸收液,太小拖延时间,要求不夹带前提下尽可能大。
(1)、分析方法的选用:
成份分析现时最流行是色谱,但在本实验中,被分析的是氨和空气混合气,这两种气体导热系数很接近,而尾气中氨的浓度本来就很低,更加和空气没有什么区别,因此,基于导热系数差异而进行分析的色谱法(3)、仪器刻度的制作
尾气通过吸收器,当其中的硫酸被尾气中的氨刚好完全中和时,若所能过的空气体积为V0空[毫升](标准状态)被吸收的氨的体积为V0氨[毫升](标准状态),则尾气浓度Y2为:
Y2=
[比分子分数](6-1)
Vo空——由湿式气体流量计测量,再换算为标准状态,换算公式:
Vo空=
(6-2)
式中:
——湿式气体流量计所量得的体积[毫升]
P1,T1空气流经湿式气体流量计时的压强和温度[毫米汞柱]、[K]
Po,To[760毫米汞柱]、[273K]
在我们的具体装置中P1实际上等于大气压强,因此可取本地区平均大气压Pm,
令Cp=
则Vo空=
(6-3)
Vo氨的数值可根据加入吸收管的硫酸溶液体积和浓度求出:
Vo氨=22.1VsNs(6-4)
式中:
Vs————加入吸收管中的硫酸溶液体积[毫升]
Ns————硫酸液的当量浓度
注:
N——是当量浓度的单位1N=1(克当量/升)=1[毫克当量/毫升]
(6-4)式的推导见附录。
合并(6-4),(6-3),(6-1)式:
Y2=22.1(
)(6-5)
Cp、Vs、To均为给定量,
T1温度时:
Y2=
(6-6)
C=22.1VsNs
=Const.
例题1:
某次尾气分析:
加入吸收管的硫酸液Vs=1[毫升]
Ns=0.04637[N]到吸收液刚中和时湿式气体流量计示值:
=1.5[升]气温30[oC]问尾气浓度多少?
解:
广州地区平均大气压760.4mmHg,Cp
1
Y2=22.1×
=0.000758[比分子分数]
例题2:
试制作10oC和30oC温度下,湿式气体流量计示值与尾气浓度的关系线,加入吸收管的硫酸液同例题1。
体积分别为1、2毫升。
2毫升,10oC时:
Y2(10)=22.1×
30oC时:
Y2(30)=0.227×10-2
图11
—湿式气体流量计所示的空气体积[升]
(4)附录:
式(6-4)的推导过程:
式(6-4):
Vo氨=22.1VsNs
其中22.1是1毫克分子氨在标准状态下的体积。
[毫升/毫克分子]这是因为标准状态下氨的重度=0.7708[克/升]或[毫克/毫升]
又:
1毫克分子氨的重量是17.03毫克
1毫克分子氨在标准状态下的体积:
17.03(
)=22.1[毫升/毫克分子]
硫酸吸收氨时反应方程如下:
2NH3+H2SO4=(NH4)2SO4(6-7)
NH3的分子量=17H2SO4分子量=98
H2SO4的当量=98/2=49
由方程(6-7)知2×17的氨与98硫酸反应完全,即17的氨与49硫酸反应完全,因为1毫克分子氨重17毫克,1毫克当量的硫酸重49毫克,故亦即1毫克分子氨与1毫克当量硫酸反应完全。
也就是说当吸收管中的硫酸到达中和时参与反应的氨的毫克分子数在数值上与所加入的硫酸的毫克当量数相等。
加入吸收管中的硫酸的毫克当量数为:
VsNsVs—[毫升]Ns—[毫克当量/毫升]所以,Vo氨=22.1VsNs[毫升]
七、实验记录
填料塔流体阻力实验记录表
实验设备编号:
;实验日期年月日
1.基本数据
实验介质:
空气、水;填料种类:
拉西坏;填料层高度:
m;塔内径:
m填料规格:
12mm×12mm×1.3mm.
2.操作记录
大气压强
序号
空气流量
水流量
填料层压强降(Pa)
塔内现象
流量计示值
流量计前压强(Pa)
温度(℃)
流量(标态)(m3/h)
流量计示值
流量(L/min)
水温(℃)
注:
塔内现象栏用以记录“塔顶积液”、“雾沫夹带严重”等现象。
传质系数测定记录表
实验设备编号:
XS型填料吸收塔;实验日期:
年月日
1.基本数据
气体种类:
氨、空气混合气;吸收剂:
水;填料种类:
瓷环(拉西环);填料装填高度
m;自由体积:
;填料规格(外径×高×壁厚);比表面积m2/m3;塔内径m。
2.操作记录
大气压强Pa
序号
项目
1
2
3
4
5
6
空
气
流
量
流量计前压强(Pa,表压)
空气温度(℃)
流量计指示值
标定状态下空气的温度(K)
标定状态下空气压强(Pa)
按标定状态计的流量(m3/h)
按标准状态计的流量(m3/h)
氨
气
流
量
流量计前压强(Pa,表压)
氨气温度(℃)
流量计指示值
标定状态下空气的温度(K)
标定状态下空气压强(Pa)
按标定状态计的流量(m3/h)
按标准状态计的流量(m3/h)
氨气含纯氨百分数
水
流量
温度(℃)
流量计示值
实际流量(L/min)
尾气浓度
吸收液(硫酸)浓度(mol/L)吸收液量(mL)
尾气体积(L)
尾气摩尔分数(%)
塔内压强
塔顶压强(Pa,表压)
塔顶塔底压强差(Pa)
塔内平均压强(Pa,绝对压)
备注
八、思考题
预习思考题
1.简述本次实验中空气系统的启动流程及实验结束时空气系统的关闭流程。
2.本次实验中,空气系统、水系统、氨气系统的开启顺序如何?
3.逆流操作的吸收塔,若其他条件不变,增大液相流量,气液出口浓度如何变化?
最小液汽比如何变化?
操作线斜率如何变化?
4.逆流操作的吸收塔,若其他条件不变,增大气相中溶质的体积分数,气液出口浓度如何变化?
最小液汽比如何变化?
操作线斜率如何变化?
实验报告思考题
附录:
吸收与解吸计算
一、吸收系数的测定
1.原理
吸收过程可用下列方程表示:
G=KyαVp△Ym(3-1)
式中Kyα——以气相为推动力的体积吸收系数。
[kmol/h·m3]
显然,要知道具体某个吸收过程的吸收系数,只需设法测量出上式中其他各项即可求出吸收系数。
上式其他各项的意义如下:
G——单位时间吸收的组分量[kmol/h]
Vp——填料体积[m3]
△Ym——平均传质推动力
(1)G,可以通过测量气相进、出口浓度和隋性气体流量计得:
G=V(Y1—Y2)(3-2)
V——惰性气体流量,[kmol/s]本装置中由空气转子流量计测量。
Y1、Y2——进、出塔的气相组成。
(2)△Ym求取
△Ym=
(3-3)
式中Y*表示平衡时的气相浓度
下标1,2分别表示塔底和塔顶,见图3。
2、数据整理过程示例
下面用具体数据举例说明,用表1序号1数据做例子。
(1)求空气流量:
(Qo)
转子流量计示值15.5(米3/时)
转子流量计标定压强760mmHg
转子流量计标定温度:
20oC
使用状态:
流量计前表压:
26.4mmHg
大气压:
760mmHg
流量计前温度:
32oC
标准状态下空气流量(Qo)按附录1式(5-6)计算:
Q1=15.5To=273Po=760P1=760
P2=760+26.4=786.4T1=273+20=293T2=273+32=305
Qo=14.4(米3/时)
(2)求氨气流量
转子流量计示值:
1.18(米3/时)
转子流量计标定介质:
空气
标定压强:
760mmHg标定温度:
20oC(293k)
使用状态:
计前表压:
18.5mmHg即绝对压:
778.5mmHg温度:
31oC
标准状态下氨流量按附录式(5-8)计算
Q20=Q1
Q1=1.18To=273Po=760P1=760
P2=778.5T1=293T2=304
标定介质在标准状态下重度r10=1.2928
被测介质是含氨98%的气体,标准状态下的重度
(详见附录例题),所以
Q20=1.45[标准米3/时]
因为氨含量为98%,故纯氨流量为1.45×0.98=1.42[标准米3/时]
表1吸收实验数据
项目
序号
1
2
空
气
流量计示值
[m3/h]
15.5
16.5
计前表压
[mmHg]
26.4
26
温度
[oC]
32
32
氨
气
流量计示值
[m3/h]
1.18
1.25
计前表压
[mmHg]
18.5
18.5
温度
[oC]
31
31
水
流量计示值
[升/时]
115
102
温度
[oC]
31
31
浓
度
空气体积[升]
53
11.4
温度[oC]
31
31
吸收液:
硫酸体积0.04391N
2ml
1ml
压
强
大气压[mmHg]
塔顶表压[cmH2O]
8.8
8.5
填料层压差[cmH2O]
13.6
13.2
(3)计算Y1、Y2
Y1=Q20/Qo=1.42/14.4=0.099
由附录式6-5得:
Y2=0.00004
(4)计算V
V=V×1.293/28.96=14.4×1.293/28.96=0.65(kmol/h)
空气分子量:
28.96
空气密度:
1.293
(5)计算G
G=V(Y1-Y2)=0.65×(0.099-0.00004)=0.0640[kmol/h]
(7)亨利系数
当溶液浓度不大于10%时,平衡关系服从亨利定律:
y*=mx
用摩尔比表示:
Y*=
当浓度很低时:
Y*=mX(3-4)
式中相平衡常数m=
P——混合气体总压[大气压](绝对)
E——亨利系数[大气压](绝对)(见图2)
温度:
取水温31oCE=1.23
m=E/P=1.23
(8)求L和X1
L=
Q水=115升/时
水=999公斤/米3M水=18
L=6.4[kmol/h]
图2NH3的亨利系数
出塔液相浓度X1,可由物料衡算式计算:
L(X1—X2)=V(Y1—Y2)
因进塔为清水,X2=0,代入前面已计出的其他各项数值:
X1=
=0.064/6.4=0.01
(9)计算△Ym
以X1代入式(3-10)得
Y1*=mX1=1.23×0.01=0.0123
代入式(3—3)
△Ym=0.01
填料体积
Vp=0.8×0.111×0.111×3.14/4=0.00774立方米
体积吸收系数
Kyα=G/Vp/△Ym=813(kmol/h/m3)
二、解吸系数的测定
1.原理
图3解吸过程
解收过程可用下列方程表示:
G=KyαVp△Ym(3-5)
式中Kyα——以气相为推动力的体积解吸系数。
[kmol/h·m3]
显然,要知道具体某个解吸过程的解吸系数,只需设法测量出上式中其他各项即可求出解吸系数。
上式其他各项的意义如下:
G——单位时间解吸的组分量[kmol/h]
Vp——填料体积[m3]
△Ym——平均传质推动力
(1)G,可以通过测量气相进、出口浓度和隋性气体流量计得:
G=V(Y1—Y2)(3-5)
V——惰性气体流量,[kmol/s]本装置中由空气转子流量计测量。
Y1、Y2——进、出塔的气相组成(见图3)。
(2)△Ym求取
△Ym=
(3-6)
式中Y*表示平衡时的气相浓度
下标1,2分别表示塔底和塔顶(见图3)。
表2解吸实验记录
项目
序号
1
2
空
气
流量计示值
[m3/h]
16
20
计前表压
[mmHg]
28.3
23.5
温度
[oC]
32
32
氨
气
流量计示值
[m3/h]
计前表压
[mmHg]
温度
[oC]
水
流量计示值
[升/时]
150
106
温度
[oC]
31
31
浓
度
吸收液:
硫酸空气体积[升]
5.9
0.5
0.04391N
温度[oC]
31
31
体积:
1毫升
尾气浓度Y2
2ml,
2ml,
压
强
大气压
[mmHg]
塔顶表压
[cmH2O]
8
9.5
填料层压差
[cmH2O]
18.3
15
2、数据整理示例
用表2序号1数据做例子。
(1)求空气流量:
(Qo)
Qo=14.9米3/时(计算过程同吸收)
(2)计算Y1,Y2
Y1=0
由附录式6-5得:
Y2=0.000365
(3)计算空气流量V
V=14.9×1.293/28.96=0.67(kmol/h)
空气分子量:
28.96
空气密度:
1.293
(4)计算解吸量G
G=V(Y2-Y1)=0.67(0.000365-0)=0.000244[kmol/h]
(5)亨利系数
当溶液浓度不大于10%时,平衡关系服从亨利定律:
y*=mx(3-7)
用摩尔比表示:
Y*=
当浓度很低时:
Y*=mX
式中相平衡常数m=
P——混合气体总压[大气压](绝对)
E——亨利系数[大气压](绝对)(见图2)
温度:
取水温31oCE=1.23
m=E/P=1.23
(6)求L和X1
L=
Q水=150升/时
水=999公斤/米3M水=18
L=8.33[kmol/h]
出塔液相浓度X1,可由物料衡算式计算:
L(X2—X1)=V(Y2—Y1)=G
代入前面已计出的其他各项数值:
X1=0.00997
(7)计算△Ym
以X1代入式(3-10)得
Y1*=mX1=1.23×0.00997=0.01226
Y2*=mX2=1.23×0.01=0.0123
代入式(3—6)
△Ym=0.012
填料体积
Vp=0.8×0.111×0.111×3.14/4=0.00774立方米
体积解吸系数
Kyα=G/Vp/△Ym=2.63kmol/h/m3
可见,体积解吸系数(2.63)比体积吸收系数(813)小很多。
预习报告思考题
1.简述本次实验中空气系统的启动流程及实验结束时空气系统的关闭流程。
2.本次实验中,空气系统、水系统、氨气系统的开启顺序如何?
3.逆流操作的吸收塔,若其他条件不变,增大液相流量,气液出口浓度如何变化?
最小液汽比如何变化?
操作线斜率如何变化?
4.逆流操作的吸收塔,若其他条件不变,增大气相中溶质的体积分数,气液出口浓度如何变化?
最小液汽比如何变化?
操作线斜率如何变化?
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 实验四 氨气的吸收与解吸实验 实验 氨气 吸收 解吸
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《城市规划基本知识》深刻复习要点.docx
《城市规划基本知识》深刻复习要点.docx
