 人教版学年九年级上学期期末考试化学试题C卷精编.docx
人教版学年九年级上学期期末考试化学试题C卷精编.docx
- 文档编号:10156347
- 上传时间:2023-02-08
- 格式:DOCX
- 页数:12
- 大小:228.32KB
人教版学年九年级上学期期末考试化学试题C卷精编.docx
《人教版学年九年级上学期期末考试化学试题C卷精编.docx》由会员分享,可在线阅读,更多相关《人教版学年九年级上学期期末考试化学试题C卷精编.docx(12页珍藏版)》请在冰豆网上搜索。
人教版学年九年级上学期期末考试化学试题C卷精编
人教版2019-2020学年九年级上学期期末考试化学试题C卷
姓名:
________班级:
________成绩:
________
一、单选题
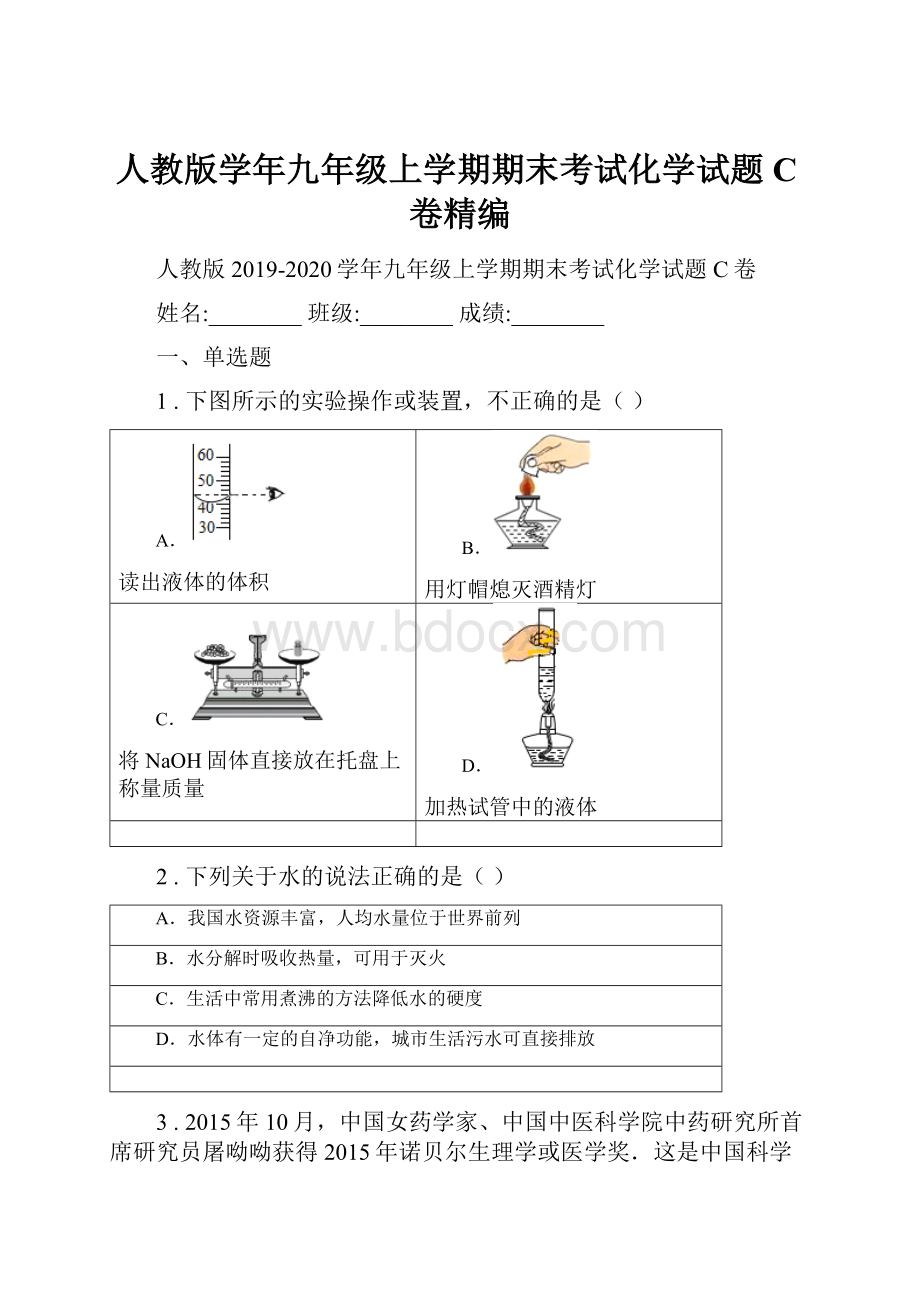
1.下图所示的实验操作或装置,不正确的是()
A.
读出液体的体积
B.
用灯帽熄灭酒精灯
C.
将NaOH固体直接放在托盘上称量质量
D.
加热试管中的液体
2.下列关于水的说法正确的是()
A.我国水资源丰富,人均水量位于世界前列
B.水分解时吸收热量,可用于灭火
C.生活中常用煮沸的方法降低水的硬度
D.水体有一定的自净功能,城市生活污水可直接排放
3.2015年10月,中国女药学家、中国中医科学院中药研究所首席研究员屠呦呦获得2015年诺贝尔生理学或医学奖.这是中国科学家因为在中国本土进行的科学研究而首次获诺贝尔科学奖.屠呦呦从中医古籍里得到启发,通过对提取方法的改进,首先发现中药青蒿的提取物有高效抑制疟原虫的成分,她的发现,在抗疟疾新药青蒿素的开发过程中起到关键性的作用.下列有关青蒿素(Artemisinin,化学式为C15H22O5)的说法不正确的是
A.青蒿素的相对分子质量是282
B.青蒿素中碳元素、氧元素的质量比是9:
4
C.青蒿素中氢元素的质量分数最大
D.青蒿素由碳、氢、氧三种元素组成
4.下列物质的用途与其化学性质无关的是
A.氧气供给呼吸
B.用一氧化碳冶炼金属
C.用活性炭除去冰箱异味
D.用二氧化碳灭火
5.下列各项:
①原子数目②原子的种类③分子数目④分子的种类 ⑤元素的种类⑥物质的总质量 ⑦物质的种类 中,在化学反应前后一定不会发生变化的是
A.①③⑤⑦
B.②③④⑤
C.①②⑤⑥
D.②④⑥⑦
6.下列有关水的说法中正确的是
A.硬水是指含有较多可溶性钙、镁化合物的水
B.水的蒸发和水通电分解过程中,分子均发生变化
C.通过过滤和吸附净化后的水为纯水
D.水沸腾时可冲起壶盖,说明温度升高分子会变大
7.某同学书写的试剂标签如下图所示,其中错误的是
A.
B.
C.
D.
8.下列鉴别方案正确的是()
A.用水鉴别NH4NO3、NaOH、CuSO4三种固体
B.用燃着的木条鉴别O2、CO2、N2三种气体
C.用灼烧的方法鉴别木炭粉、CuO、Fe3O4三种黑色粉末
D.用NaCl溶液鉴别H2SO4、Ca(OH)2、Na2CO3三种无色溶液
9.化学与人体健康密切相关。
下列说法不科学的是
A.在密闭房间内燃煤取暖
B.进入溶洞前做灯火实验
C.人体缺钙会引起骨质疏松、佝偻病
D.遇到火灾时,可用湿毛巾捂着口鼻,低下身子或贴近地面跑出火灾区
10.下列有关物质燃烧现象的叙述中,正确的是()
A.铁丝在氧气中燃烧:
火星四射,生成红色固体
B.硫粉在空气中燃烧:
产生淡蓝色火焰,生成一种有刺激性气味的气体
C.木炭在空气中燃烧:
发出白光,生成一种能使澄清石灰水变浑浊的气体
D.红磷在空气中燃烧:
发出白光,生成大量的白色烟雾
11.有下列五种粒子的结构示意图:
则下列说法不正确的是
A.②④可形成稳定的化合物
B.②⑤化学性质相似
C.①的化学性质不活泼
D.①③属于同种元素
12.下列反应中属于化合反应的是()
A.3Fe+2O2
Fe3O4
B.CaCO3
CaO+CO2↑
C.Zn+2HCl═ZnCl2+H2↑
D.CO2+2NaOH═Na2CO3+H2O
13.物质的鉴别和除杂是重要的实验技能。
下列实验方法能达到目的的是
选项
实验目的
实验方法
A
鉴别氧气和氢气
闻气味
B
鉴别软水和硬水
观察颜色
C
除去自来水中的色素和异味
加入活性炭,搅拌、静置、过滤
D
除去FeSO4溶液中的少量CuSO4
加足量锌粉、充分反应后过滤
A.A
B.B
C.C
D.D
14.以下是固体和液体反应的装置,其中能控制反应的发生和停止的是
A.
B.
C.
D.
15.下列现象和应用中,所包含的主要变化有一项与其他三项有本质区别,该项是 ()
A.利用沸点不同分离液态空气制得氧气
B.酸雨腐蚀铁制栏杆
C.利用熟石灰改良酸性土壤
D.黄豆霉变
16.空气的成分中,化学性质不活泼且含量最多的是()
A.氧气
B.氮气
C.二氧化碳
D.稀有气体
17.如图为某元素原子的结构示意图。
下列有关叙述不正确的是()
A.该元素的原子序数为17
B.在该结构示意图中x=7
C.该元素的原子在化学反应中容易得到电子
D.该元素为硫,是一种非金属元素
18.某同学查阅资料得知:
①Cu与稀硫酸不反应,但Cu可与浓硫酸在加热的条件下反应,化学方程式为:
Cu+2H2SO4(浓)
CuSO4+SO2↑+2R。
②有元素化合价升降的反应是氧化还原反应。
下列说法不正确的是()
A.该反应是氧化还原反应
B.R为相对分子质量最小的氧化物
C.硫酸铜是由铜离子和硫酸根离子构成的化合物
D.反应中,SO2和R的质量比是32:
9
19.甲物质是一种重要的有机化工原料.甲和乙反应生成丙和丁的微观示意图如图.则下列说法中正确的是()
A.反应前后分子的种类、个数不变
B.乙是氧化物
C.生成的丙、丁两物质的质量比是1:
1
D.甲的化学式可能为CH2O
20.下列有关物质用途的说法中,正确的是()
①用稀硫酸清除钢铁表面的铁锈②用碳酸氢钠作焙制糕点的发酵粉③用氢氧化钠中和胃中过多盐酸④用熟石灰中和硫酸工厂的污水
A.①②④
B.①②③
C.②③④
D.①②③④
二、科学探究题
21.请按照要求完成下列金属性质的探究:
探究一:
铝片与盐酸反应过程中的能量及反应速率的变化。
(1)实验时需将铝片进行打磨,其目的是_____。
(2)反应中试管外壁发烫,说明铝与盐酸反应是_____(填“吸热”或“放热”)反应,化学方程式为_____。
(3)实验测得铝片产生气体的速率(v)与时间(t)的关系如图所示,t1~t2时间内反应逐渐加快的主要原因是_____。
(查阅资料)铁、铜均能与氯化铁溶液反应,化学方程式分别为:
2FeC13+Fe==3FeCl2、2FeCl3+Cu=2FeCl2+CuCl2
(4)向氯化铁和氯化铜的混合溶液中,加入一定量的铁粉,充分反应后过滤。
取少量滤渣加入稀盐酸,有气泡产生。
则滤液中的溶质是_____,滤渣中一定含有_____。
22.某固体粉末由Mg、MgO、Mg(OH)2中的一种或几种组成。
某化学小组为了探究该固体粉末的成分,设计如图所示的装置(固定装置省略)。
(信息资料)
(1))本实验条件下,氢气密度为0.09g/L。
(2)Mg,MgO,Mg(OH)2均能与硫酸反应
(3)MgSO4+2NaOH===Na2SO4+Mg(OH)2↓
(实验过程)
步骤Ⅰ:
检查装置气密性,装入药品并连接仪器。
步骤Ⅱ:
倾斜Y形管,使样品充分反应,测的生成气体的体积为55.6mL。
步骤Ⅲ:
拆下装置,往Y形管内残余液中加入氢氧化钠溶液,至不再生成沉淀。
经过滤、洗涤和干燥后,称得沉淀质量为2.90g。
(回答问题)
(1)该套装置气密性的检验方法是____________________。
(2)用冷水浴的原因是___________
(3)①使样品与硫酸充分反应的正确操作是_________(填标号)。
A.硫酸溶液转移到样品中 B.样品转移到硫酸溶液中
②判断样品完全反应的现象是___________________________。
③样品与硫酸反应中可能存在属置换反应的反应方程式为___________
(4)根据实验结果分析:
①通过步骤Ⅱ推断,样品中一定含有的物质是______________。
步骤Ⅲ中有沉淀生成的方程式为MgSO4+2NaOH===Na2SO4+Mg(OH)2↓,经计算,样品中镁元素的总质量为_____________克。
②结论:
该样品中的成分是________________________。
(反思)
(5)该化学小组同学经过讨论得出以下结论,正确的是_________(填标号)。
A.利用该实验方案,能计算出样品中各物质的质量
B.实验前可通过样品的质量估算硫酸溶液的质量,确保样品完全反应
A.仅称量步骤Ⅱ中Y形管内药品减轻的质量,即能计算出样品中各物质的质量
(6)从该实验中得出制取硫酸镁的三种方法,得出这三个反应中消耗等量等浓度的硫酸,生成的硫酸镁质量_______________(相等或不同)
(7)若本实验中把硫酸换为浓盐酸,你的看法是_________
三、综合题
23.请根据下列装置回答问题:
(1)写出标号仪器名称:
a________________;b________________.
(2)实验室用高锰酸钾制取并收集较纯净的氧气时,装置应选用______________(填字母),该发生装置不足之处是____________所发生反应的化学方程式为_________________氧气收集完毕后,测得其纯度明显偏低,原因可能是:
____________________(填字母,可多选)。
a.高锰酸钾中混入了二氧化锰
b.收集前,集气瓶中未注满水
c.收集后,集气瓶中仍有少量水
d.加热前就将导管伸入集气瓶
若用C装置收集,判断氧气已收集满的方法是__________________
(3)实验室用一定量的氯酸钾和二氧化锰的固体混合物装入试管中,加热制取氧气。
待反应完全后,得到4.8g氧气。
请计算原固体混合物中氯酸钾的质量________________。
24.探究小组欲从含有FeCl3、CuCl2的废液中回收金属铜,取一定量的废液样品加入少量铁粉,一段时间后铁粉完全溶解,但未发现红色固体沉积,出现这种现象的可能原因是_____________________;
经查阅资料,铁粉在废液中发生两个化学反应:
①2FeCl3+Fe=3FeCl2②CuCl2+Fe=FeCl2+Cu
(2)探究小组另取废液,向废液中加入一定且足量的铁粉至充分反应,溶液变为浅绿色,过滤、干燥,称得固体沉积物质量与加入铁粉质量相等.
①固体沉积物质量与加入铁粉质量相等的原因是_____________________________;
②经测定,反应后得到铜的质量为1.6g,其中,反应①消耗铁粉的质量是____,反应②消耗铁粉的质量是____(计算结果精确到0.1)。
参考答案
一、单选题
1、
2、
3、
4、
5、
6、
7、
8、
9、
10、
11、
12、
13、
14、
15、
16、
17、
18、
19、
20、
二、科学探究题
1、
2、
三、综合题
1、
2、
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 人教版 学年 九年级 学期 期末考试 化学试题 精编
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《JAVA编程基础》课程标准软件16级.docx
《JAVA编程基础》课程标准软件16级.docx
